Clear Sky Science · es
Hidrólisis catalítica eficiente y estable de perfluorocarbonos habilitada por el suministro de protones mediado por SO2
Por qué importa este persistente gas de efecto invernadero
Algunos gases industriales son tan estables que, una vez liberados, permanecen en la atmósfera durante decenas de miles de años. El tetrafluorometano (CF4), un tipo de perfluorocarbono usado y emitido en la fundición de aluminio y la fabricación de semiconductores, es uno de los peores infractores: atrapa el calor unas 7.400 veces más eficazmente que el dióxido de carbono. Este estudio explora una nueva forma de descomponer el CF4 de manera eficiente y fiable, transformando un contaminante casi indestructible en productos más seguros bajo condiciones realistas para las fábricas.
Una molécula difícil que se niega a romperse
El CF4 pertenece a la familia más amplia de los PFAS, sustancias químicas famosas por su persistencia en el medio ambiente. Lo que hace que el CF4 sea especialmente desafiante son sus enlaces carbono–flúor extremadamente fuertes y su vida atmosférica muy larga, estimada en más de 50.000 años. Los métodos tradicionales para destruir CF4 requieren temperaturas muy altas y con frecuencia provocan un desgaste rápido y pérdida de actividad en los catalizadores que impulsan la reacción. Sin embargo, las nuevas políticas climáticas, como el Mecanismo de Ajuste en Frontera del Carbono de la Unión Europea, están ejerciendo una presión creciente sobre las industrias pesadas para que reduzcan estas emisiones sin aumentar mucho su consumo energético.
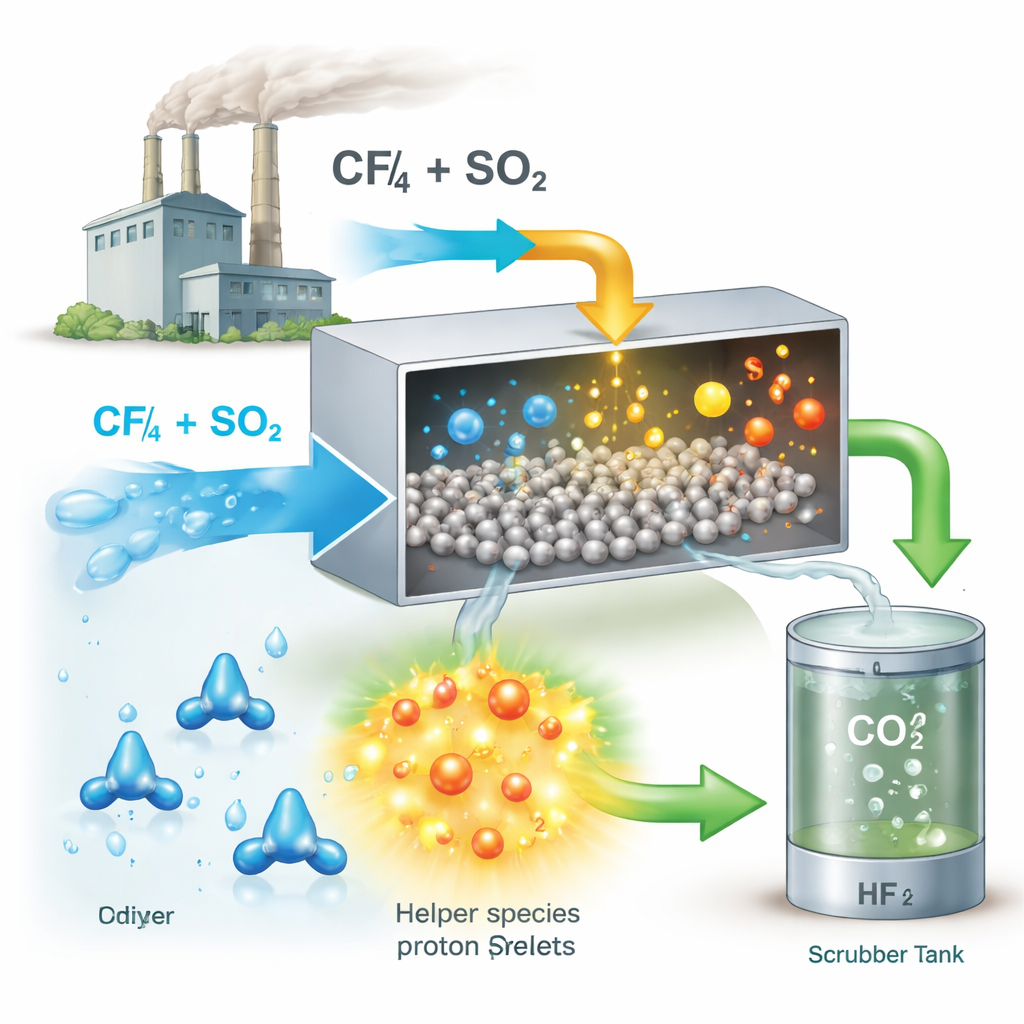
Convertir un contaminante común en un aliado
Sorprendentemente, los autores hallaron que otro contaminante familiar, el dióxido de azufre (SO2), puede utilizarse para resolver el problema del CF4. El SO2 se libera con frecuencia junto al CF4 en la producción de aluminio. Aunque el SO2 por lo general daña los catalizadores al adsorberse en sus superficies, el equipo demostró que en las condiciones adecuadas puede hacer lo contrario: remodelar la superficie del catalizador para que el agua se disocie más fácilmente y aporte más iones de hidrógeno reactivos (protones). Estos protones son esenciales para debilitar los enlaces persistentes en el CF4 y para limpiar el flúor del catalizador, de modo que pueda seguir funcionando.
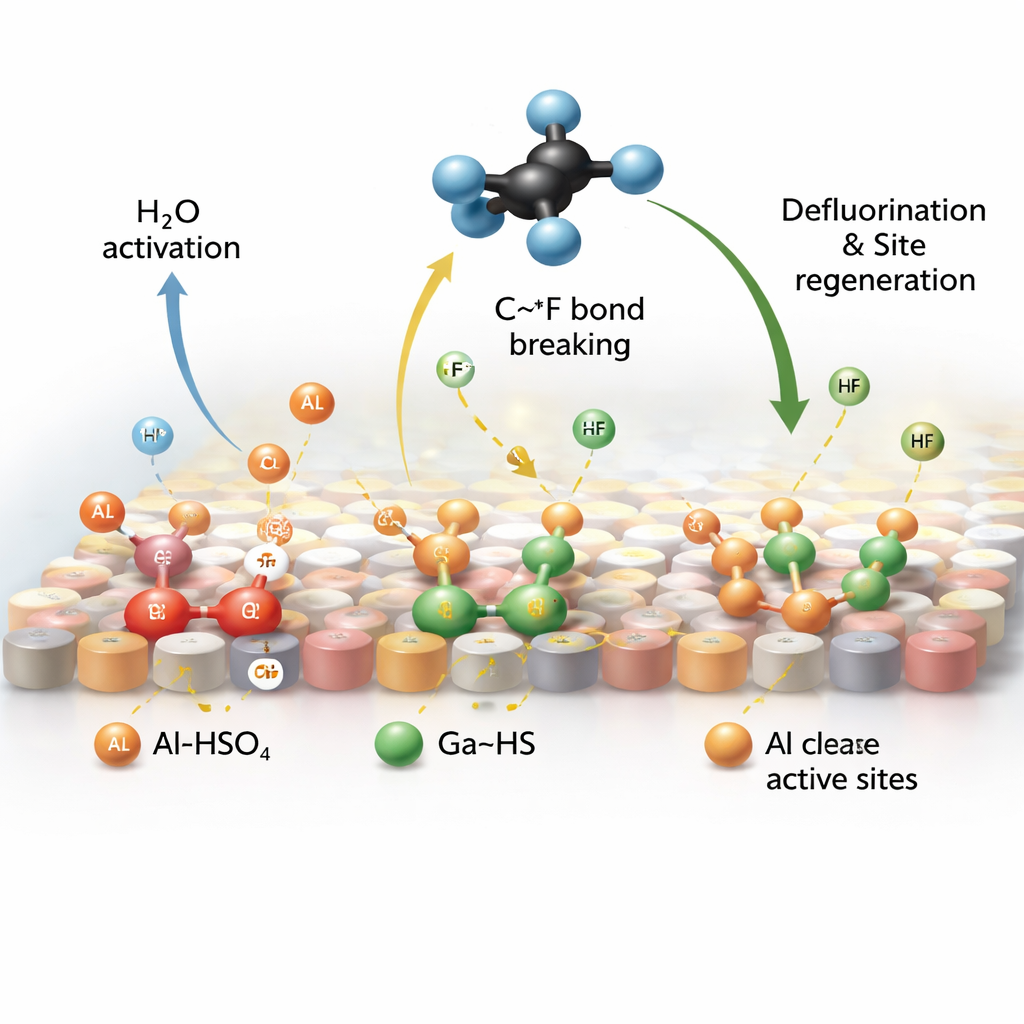
Construir “estaciones de suministro” de protones en la superficie
El avance clave es la creación de sitios especiales ricos en protones directamente en el catalizador, que se basa en óxido de aluminio dopado con galio. Cuando SO2, vapor de agua y CF4 fluyen sobre este material a alta temperatura, el SO2 se transforma en grupos ácidos fuertemente ligados en la superficie. Aparecen dos familias de dichos grupos: una principalmente ligada al aluminio (Al–HSO4) y otra al galio (Ga–HS). Mediante herramientas espectroscópicas sensibles y simulaciones por ordenador, los autores muestran que los grupos basados en aluminio atraen el CF4 y ayudan a escindir el agua para liberar protones, mientras que los grupos basados en galio emplean esos protones para arrancar el flúor de sitios envenenados y liberarlo como fluoruro de hidrógeno, restaurando la actividad del catalizador.
Rendimiento récord en condiciones del mundo real
Dado que estas “estaciones de suministro” de protones están fuertemente ancladas y se mantienen estables a altas temperaturas, proporcionan hidrógeno reactivo con mucha más eficacia que los aditivos tradicionales. El estudio encuentra que la activación del agua aumenta alrededor de seis veces y la disponibilidad de protones aproximadamente diez veces en comparación con la operación sin SO2. Como resultado, la descomposición completa del CF4 se logra a 550 °C en lugar de los habituales 700 °C, reduciendo la demanda energética del proceso. Igualmente importante, el catalizador opera durante más de 2.500 horas—más de tres meses de funcionamiento continuo—sin pérdida apreciable de rendimiento, y funciona en un amplio rango de niveles de SO2 que coinciden con los de los gases de escape industriales.
Una nueva vía para limpiar contaminantes atmosféricos persistentes
Para el público general, el resultado puede verse como enseñar a un catalizador un nuevo truco: usar un gas no deseado (SO2) para construir pequeños y robustos sitios ácidos que le suministren los protones necesarios para atacar uno de los gases de efecto invernadero más resistentes conocidos. Al facilitar tanto la destrucción del CF4 como la longevidad del catalizador, esta estrategia apunta a depuradores prácticos que podrían acoplarse a las chimeneas de plantas de aluminio y semiconductores. Más en general, el mismo concepto de regulación localizada de protones podría adaptarse para desmantelar otros PFAS en fase gaseosa, ofreciendo una herramienta prometedora para reducir la huella climática y ambiental a largo plazo de la fabricación avanzada.
Cita: Zhang, H., Luo, T., Chen, Y. et al. Efficient and stable catalytic hydrolysis of perfluorocarbon enabled by SO2-mediated proton supply. Nat Commun 17, 597 (2026). https://doi.org/10.1038/s41467-026-68386-4
Palabras clave: tetrafluorometano, destrucción de PFAS, hidrólisis catalítica, promoción por dióxido de azufre, control de emisiones industriales