Clear Sky Science · es
Excisión precisa de repeticiones GGC expandidas en NOTCH2NLC mediante CRISPR/Cas9 para el tratamiento de la enfermedad de inclusiones intranucleares neuronales
Editar el ADN para abordar un trastorno cerebral misterioso
La enfermedad de inclusiones intranucleares neuronales (NIID) es un trastorno cerebral poco frecuente pero devastador que puede provocar demencia, problemas de movimiento e incluso muerte prematura. Actualmente no existe cura. Este estudio explora si una potente herramienta de edición genética, CRISPR, puede utilizarse para recortar un tramo diminuto pero tóxico de ADN que impulsa la NIID, ofreciendo una visión de cómo futuros tratamientos podrían reescribir nuestros genes para combatir las enfermedades cerebrales. 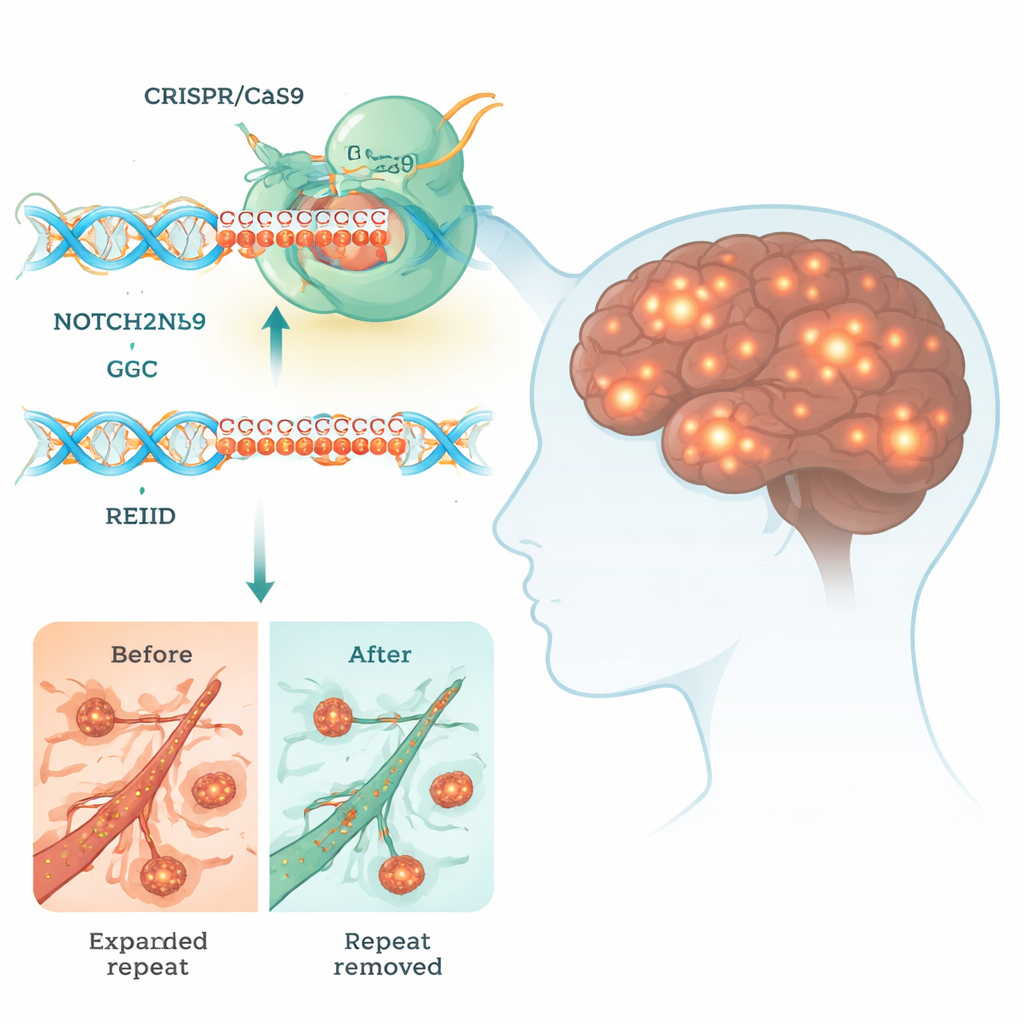
Un culpable genético oculto
Muchos trastornos cerebrales hereditarios son causados por secuencias cortas de ADN que han crecido mucho más allá de su longitud normal. En la NIID, el problema es una corrida sobredimensionada de unidades de tres letras, "GGC", en un gen llamado NOTCH2NLC. Aunque este tramo se encuentra en una región que no codifica directamente una proteína clásica, todavía puede ser leído por la maquinaria celular para producir cadenas anómalas de poliglicina (polyG). Estas cadenas pegajosas se agregan en bultos dentro del núcleo de las neuronas y otros tejidos, alterando procesos vitales como la producción de energía, el procesamiento del ARN y el tráfico de moléculas entre el núcleo y el citoplasma.
El reto de una cirugía génica precisa
Diseñar un tratamiento de edición génica para la NIID es inusualmente difícil porque NOTCH2NLC tiene varios genes hermanos casi idénticos que son importantes para el desarrollo cerebral humano. Si CRISPR corta el equivocado, podría causar más daño que beneficio. Los investigadores examinaron cuidadosamente el ADN alrededor de la repetición GGC y encontraron pequeñas diferencias de secuencia que distinguen a NOTCH2NLC de sus parientes. Luego diseñaron pares de ARN guía de CRISPR que dirigen a la Cas9, las “tijeras moleculares”, para cortar justo antes y justo después de la repetición expandida. Esta estrategia de doble corte permite que el sistema de reparación celular elimine el segmento tóxico dejando intacta el resto de la familia génica.
De células en placa a neuronas derivadas de pacientes
El equipo probó primero su diseño CRISPR en células humanas estándar y en células modificadas para portar una gran repetición de NOTCH2NLC. En estos modelos, el editor recortó eficientemente la repetición y los niveles de agregados de polyG se redujeron aproximadamente a la mitad o más. Luego pasaron a células madre pluripotentes inducidas (iPSCs) obtenidas de un paciente con NIID y convirtieron estas células en progenitores neuronales, una etapa temprana de las células cerebrales. Usando CRISPR, o bien eliminaron la repetición expandida o la reemplazaron por una versión de longitud normal. Secuenciados detallados del ADN y del genoma completo mostraron que la edición fue altamente precisa, con poca evidencia de cortes no deseados, y las células editadas continuaron dividiéndose y madurando con normalidad. 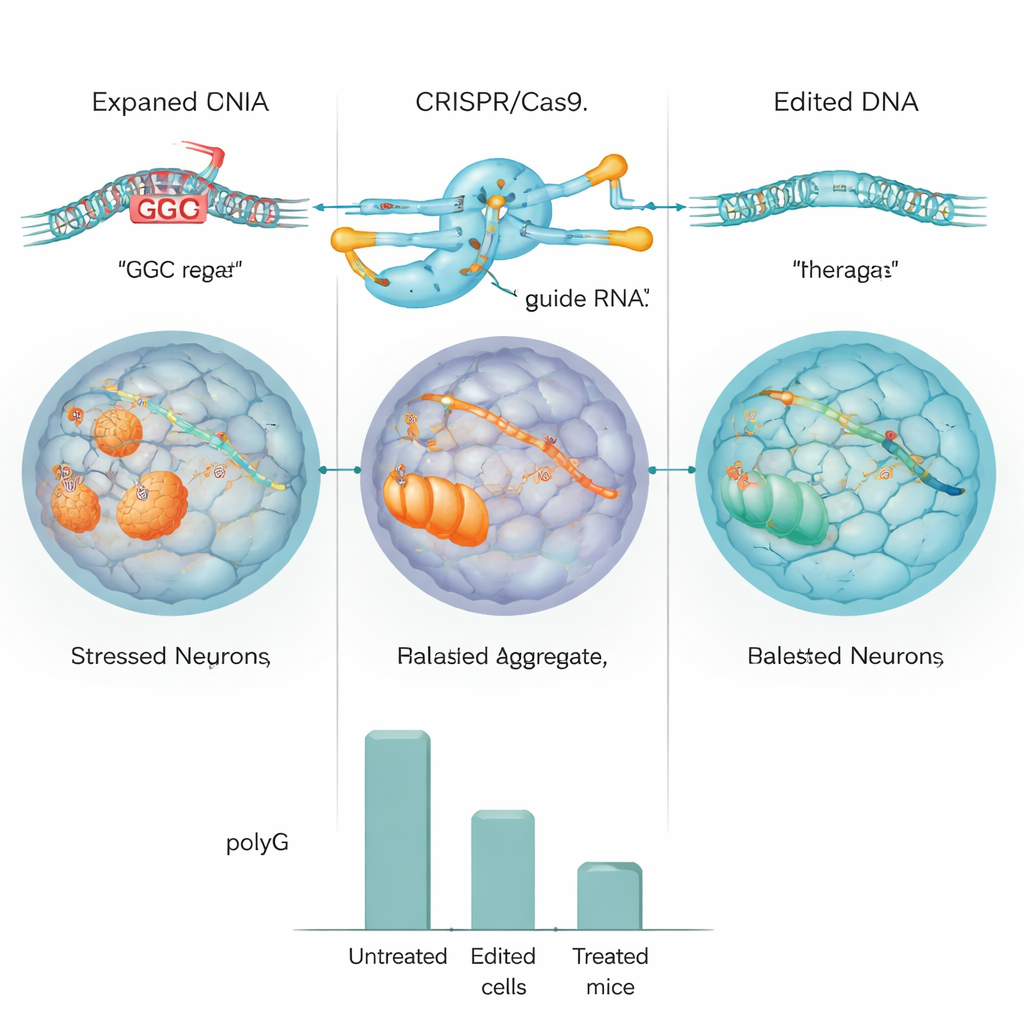
Rescatando el cerebro y el cuerpo en un modelo de ratón
Para comprobar si este enfoque podía mejorar la enfermedad, los investigadores acudieron a ratones diseñados para portar la repetición humana de NOTCH2NLC y desarrollar rasgos similares a la NIID, incluidas inclusiones nucleares, problemas de movimiento y vida útil acortada. Empaquetaron el sistema CRISPR en un virus modificado que puede distribuirse por todo el cerebro tras una inyección sencilla en el torrente sanguíneo de recién nacidos. En los animales tratados, la repetición expandida fue eliminada con éxito en tejido cerebral. Como resultado, los niveles tóxicos de polyG cayeron bruscamente, mejoraron los marcadores de salud neuronal y se redujo la activación anómala de las células gliales de sostén. Las pruebas de comportamiento mostraron que los ratones tratados se movían más, mantenían mejor el equilibrio y vivieron más que sus compañeros no tratados. Se observaron beneficios similares en el corazón, que también acumula polyG en este modelo.
Qué podría significar esto para tratamientos futuros
Para un público general, el mensaje principal es que la NIID parece estar impulsada en gran medida por una única repetición de ADN sobredimensionada, y que eliminarla con precisión puede revertir muchos signos de la enfermedad en células y en ratones. Este trabajo aún no se traduce en una terapia lista para usar en humanos: los investigadores deben refinar la seguridad a largo plazo, mejorar los métodos de entrega y probar en animales más grandes y más parecidos a los humanos. Pero el estudio ofrece una sólida prueba de concepto de que la edición génica cuidadosamente dirigida puede silenciar de manera segura una repetición tóxica sin afectar a genes estrechamente relacionados. Esa estrategia podría adaptarse algún día no solo para la NIID, sino también para otros trastornos cerebrales y musculares causados por expansiones de repeticiones similares.
Cita: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Palabras clave: Edición génica CRISPR, enfermedad de inclusiones intranucleares neuronales, trastornos por expansión de repeticiones, NOTCH2NLC, neurodegeneración