Clear Sky Science · es
Diseño mediante IA generativa basada en secuencias de sintasas de triptófano versátiles
Enseñar nuevas habilidades a las enzimas con IA
La sociedad moderna funciona gracias a moléculas —medicamentos, materiales y productos químicos especializados— que a menudo se fabrican con procesos que consumen mucha energía y contaminan. Los catalizadores de la naturaleza, las enzimas, pueden realizar trabajos similares de forma limpia y eficiente, pero encontrar o construir la enzima adecuada para una tarea industrial nueva es lento e incierto. Este estudio muestra que la inteligencia artificial generativa, la misma clase de tecnología detrás de los chatbots que escriben texto, puede usarse para diseñar enzimas totalmente nuevas que no solo funcionan bien en el laboratorio, sino que en ocasiones superan a las mejores que la evolución y años de ingeniería han producido.
Por qué las enzimas importan en la vida cotidiana
Las enzimas son pequeñas máquinas proteicas que aceleran reacciones químicas en células vivas. Los químicos han aprendido a reutilizarlas para fabricar fármacos, ingredientes alimentarios y otros productos valiosos usando menos energía y menos reactivos tóxicos que la química tradicional. El problema es que cada nueva aplicación suele requerir una enzima con un rendimiento preciso: capaz de aceptar determinados materiales de partida, sobrevivir a las condiciones de procesamiento y producir altos rendimientos. La “evolución dirigida” convencional mejora enzimas creando y probando muchas versiones mutadas, generación tras generación. Esto funciona bien, pero depende de una enzima inicial razonable y puede llevar meses o años de ensayo y error, dejando muchas reacciones útiles sin explorar.
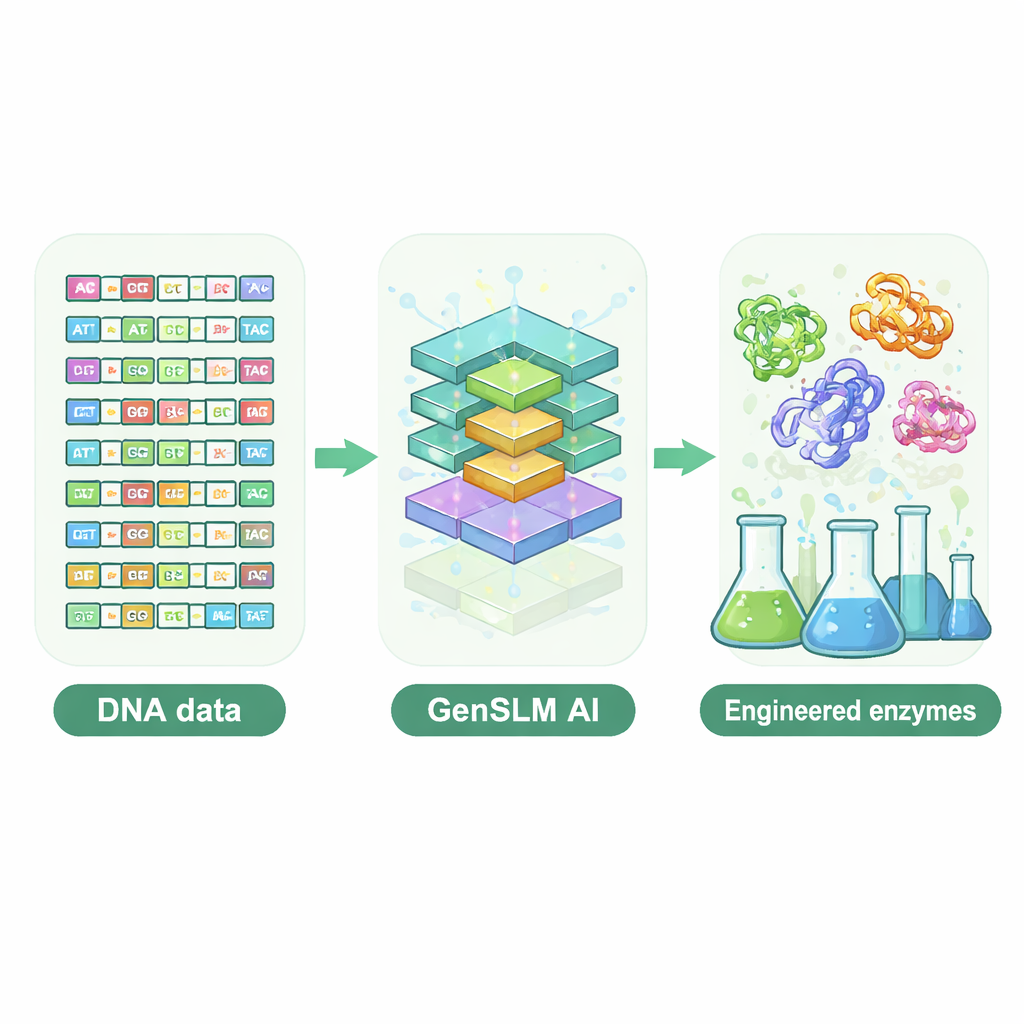
Permitir que un modelo de lenguaje escriba ADN
Los investigadores recurrieron a un modelo de lenguaje a escala genómica llamado GenSLM, que aprende patrones en el ADN de la misma manera que un modelo de lenguaje aprende gramática y estilo en texto. En vez de trabajar con secuencias proteicas acabadas, GenSLM lee y escribe ADN en codones de tres letras, reflejando cómo las células traducen genes en proteínas. El equipo afinó primero a GenSLM con decenas de miles de genes naturales de una subunidad en particular, compleja, llamada TrpB, que ayuda a construir el aminoácido triptófano. A continuación pidieron al modelo que generara miles de genes trpB completamente nuevos. Filtros computacionales sencillos eliminaron secuencias demasiado cortas o largas, poco probables de plegarse correctamente o casi idénticas a enzimas naturales conocidas, dejando 105 candidatos diversos para pruebas experimentales en bacterias.
De los diseños computacionales a catalizadores funcionales
Cuando estas 105 enzimas TrpB diseñadas por IA se produjeron en E. coli, muchas se plegaron bien y se expresaron en cantidades elevadas. Docenas pudieron realizar su función principal: convertir indol y el aminoácido compañero natural, serina, en triptófano. Algunas funcionaron de forma robusta incluso a temperaturas elevadas, pese a que no se diseñaron explícitamente para resistencia al calor. En pruebas comparativas, un subconjunto de GenSLM‑TrpBs igualó o superó a una enzima de referencia que había sido evolucionada cuidadosamente en el laboratorio durante años para funcionar por sí sola a 75 °C. Un diseño destacado, etiquetado 230, produjo más triptófano que este referente industrial tanto a temperatura ambiente como a alta temperatura, demostrando que un modelo entrenado solo con datos de secuencia puede pasar directamente a un rendimiento de primer nivel.
Nueva flexibilidad más allá de lo que construyó la naturaleza
El equipo sometió luego a las enzimas a un panel de sustratos no naturales: derivados del indol, un compañero tipo alcohol distinto y un compuesto fluorinado usado en la fabricación de fármacos. Las versiones naturales de TrpB suelen ser exigentes: favorecen fuertemente sus sustratos nativos y muestran poca actividad sobre tales alternativas. De forma notable, las enzimas generadas por IA fueron con frecuencia más atrevidas. Para cada sustrato no natural probado, al menos un diseño de GenSLM mostró actividad mensurable, y muchos funcionaron mejor que las enzimas naturales. De nuevo, la variante 230 se destacó, convirtiendo los siete sustratos alternativos con rendimientos que iban de modestos a casi completos, una amplitud de “promiscuidad” no vista previamente en esta familia enzimática. Sin embargo, al comparar 230 con su pariente natural más cercano —que difiere en solo 78 de los 400 aminoácidos— los investigadores encontraron que la enzima natural carecía de esa versatilidad a pesar de que su estructura global y los residuos clave del sitio activo eran casi idénticos.
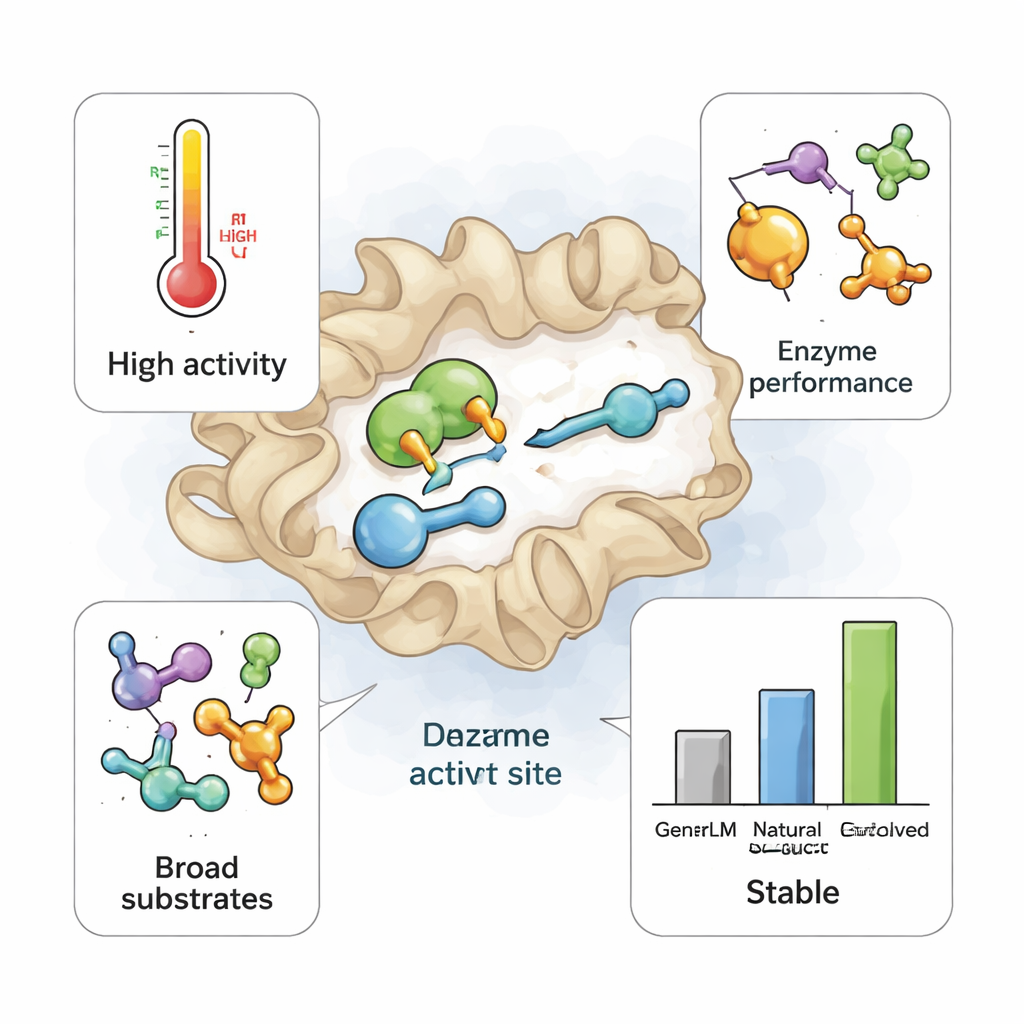
Qué significa esto para la futura química verde
Para un no especialista, el mensaje clave es que un modelo de IA entrenado solo con secuencias de ADN existentes puede imaginar enzimas nuevas y realistas que la naturaleza nunca probó, algunas de las cuales son herramientas mejores para la química que las que usamos ahora. Estas variantes de TrpB diseñadas por IA conservan la forma y función esenciales de sus parientes naturales pero adquieren una capacidad inusual para manejar muchos materiales de partida distintos. Esa flexibilidad podría reducir drásticamente la cantidad de trabajo de laboratorio necesario para descubrir rutas enzimáticas a nuevos medicamentos y otros productos. A medida que el diseño, la síntesis de ADN y las pruebas se vuelvan más rápidos y baratos, modelos generativos similares podrían convertir el descubrimiento de enzimas de una búsqueda lenta de tesoros en una tarea de diseño rápida y rutinaria, ayudando a desplazar más química industrial hacia procesos más limpios impulsados por enzimas.
Cita: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Palabras clave: ingeniería de enzimas, IA generativa, diseño de proteínas, sintasa de triptófano, biocatálisis