Clear Sky Science · es
Tmem110 regula la conformación de TRPML1 para mantener la homeostasis endolisosomal y prevenir la fuga de ADN mitocondrial y el procesamiento patológico de ADN propio
Por qué importa el ADN vertido tras una lesión
Cuando sufrimos un trauma grave, como un fuerte golpe en la cabeza, el daño no se limita al punto de la lesión. Muchos pacientes desarrollan una reacción sistémica peligrosa en la que los pulmones, el hígado, los riñones y otros órganos empiezan a fallar. Este estudio revela cómo pequeñas estructuras dentro de las células —lisosomas, mitocondrias y sensores inmunitarios— se comunican para decidir si el organismo limpia silenciosamente los restos o entra en una respuesta inmune autodestructiva. Entender este sistema de limpieza oculto podría abrir nuevas vías para prevenir la insuficiencia orgánica tras un trauma y para tratar enfermedades autoinmunes e inflamatorias.
De la lesión craneal a la crisis multisistémica
La lesión cerebral traumática (LCT) puede desencadenar una tormenta inflamatoria potente llamada síndrome de disfunción multiorgánica (SDMO), pero no estaba claro cómo el daño en el cerebro se propaga a órganos distantes. Los autores se centran en monocitos y macrófagos, células inmunitarias que patrullan la sangre y los tejidos y actúan como recogedores profesionales de desechos. Tras la LCT, las células mueren de forma descontrolada y liberan mitocondrias enteras —pequeñas fábricas de energía que llevan su propio ADN— a la circulación. Este ADN mitocondrial (ADNmt) resulta sospechoso para el sistema inmune, ya que se asemeja al ADN bacteriano, y puede activar defensas antivirales intensas si no se elimina rápidamente. Normalmente, las células internalizan estas mitocondrias errantes en compartimentos ácidos llamados lisosomas, donde enzimas digieren el ADN antes de que se filtre al citosol. 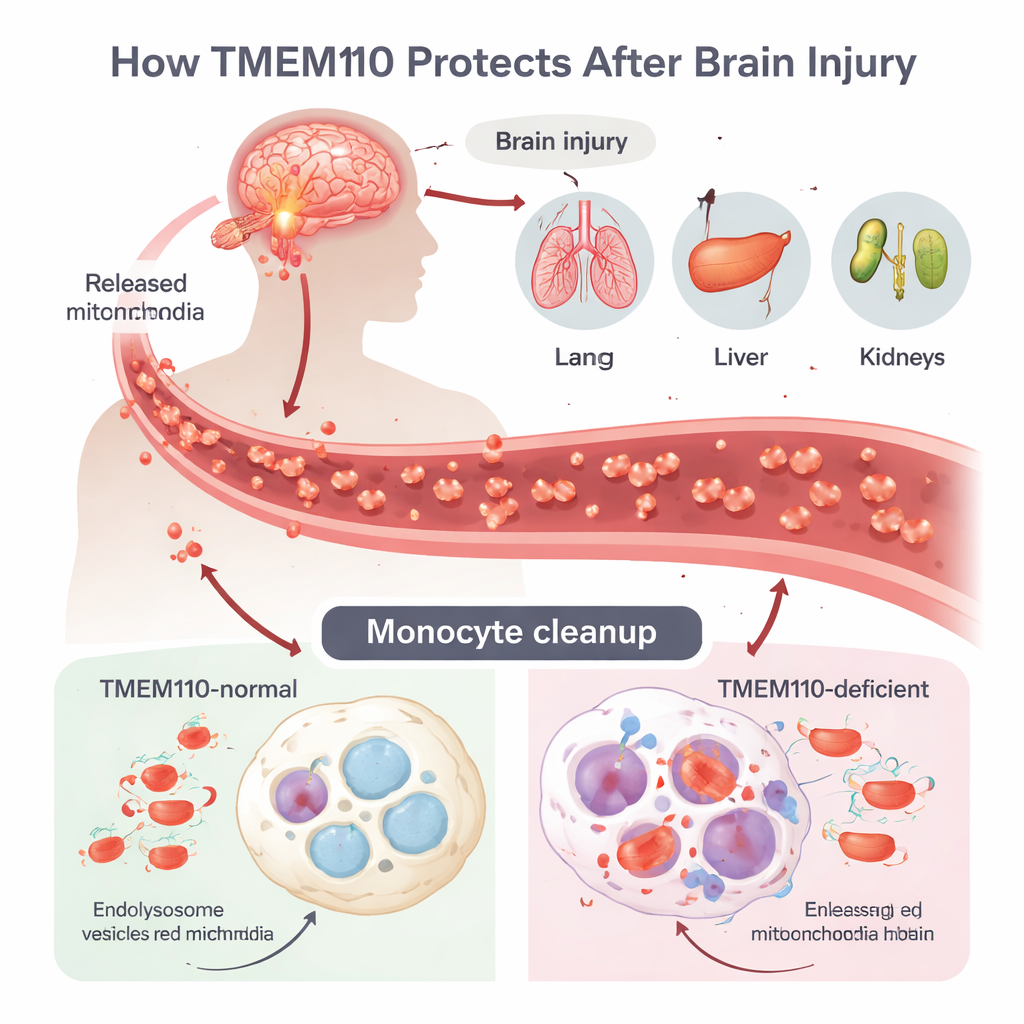
Una proteína centinela que mantiene estables los lisosomas
El equipo identificó a TMEM110, una proteína que atraviesa la membrana del retículo endoplásmico (una gran red membranosa intracelular), como un centinela crucial en este proceso. Usando ratones modificados genéticamente que carecían de TMEM110 únicamente en monocitos y macrófagos, crearon un modelo controlado de lesión cerebral. En comparación con ratones normales, los animales deficientes en TMEM110 desarrollaron niveles mucho más altos de interferones tipo I —potentes moléculas de señalización antiviral— en sangre y en líquido cefalorraquídeo. Sus pulmones, hígado, riñones y ganglios linfáticos mostraron daños más severos, y su supervivencia a largo plazo tras la LCT fue considerablemente peor. Cuando los investigadores bloquearon el receptor de interferones tipo I, o reemplazaron la médula ósea mutante por células normales, la lesión de órganos y las tasas de muerte disminuyeron, lo que demuestra que la señalización excesiva de interferón procedente de monocitos periféricos es un motor clave del SDMO en este contexto.
Cómo un manejo iónico defectuoso permite la fuga de ADN
Al profundizar en estas células inmunitarias, los autores encontraron que los lisosomas deficientes en TMEM110 estaban químicamente descompensados: eran menos ácidos y presentaban una sobrecarga de calcio. En estas condiciones, la enzima DNasa II —que normalmente fragmenta el ADN en los lisosomas— perdió actividad, las membranas lisosomales se volvieron frágiles y el ADNmt escapó al citosol circundante. Experimentos en el laboratorio con monocitos humanos que engullían mitocondrias marcadas confirmaron que, sin TMEM110, más ADNmt se filtraba al citosol y desencadenaba un aumento de genes estimulados por interferón. El estudio muestra que TMEM110 actúa controlando otra proteína, el canal iónico lisosomal TRPML1. Cuando TMEM110 está presente, contacta físicamente con TRPML1 y lo desplaza hacia una conformación “abierta” que crea pequeños puntos de liberación de calcio en la superficie lisosomal. Estas salidas controladas de calcio ayudan a mantener la acidez adecuada, favorecen la reparación de membranas y mantienen el ADNmt atrapado y degradado en el interior.
Un bucle de realimentación con el sistema de alarma de ADN de la célula
Una vez que el ADNmt se filtra al citosol, es reconocido por la vía cGAS–STING, el principal sistema de alarma celular para ADN ajeno. Curiosamente, TMEM110 también se une a STING en reposo y lo mantiene secuestrado en el retículo endoplásmico, evitando alarmas innecesarias. Cuando el ADN citosólico se acumula, STING se activa y afloja su interacción con TMEM110. Eso, a su vez, expone una región distinta de TMEM110 que se une a TRPML1 y aumenta el eflujo lisosomal de calcio, creando un bucle de retroalimentación: la detección de ADN propio activa un mecanismo que mejora la eliminación del mismo. Mutaciones en STING asociadas a enfermedades humanas autoinflamatorias interrumpen esta transferencia, atrapando a TMEM110 en un estado inhibido y contribuyendo a la activación crónica de interferón. En ratones portadores de tal mutación en STING, la LCT provocó daños orgánicos más graves y mayor mortalidad, pero la entrega de un pequeño fragmento de TMEM110 a los lisosomas mediante una terapia con ARNm en nanopartículas lipídicas restauró parcialmente el control del ADNmt y mejoró la supervivencia.
Pistas de pacientes y vías hacia nuevos tratamientos
Los autores analizaron a continuación una cohorte clínica de 143 personas con lesión cerebral traumática y SDMO. Los pacientes cuyos monocitos mostraban niveles más altos de TMEM110 en las fases iniciales tras la lesión tenían más probabilidad de recuperar la función orgánica y sobrevivir. Aquellos con TMEM110 más bajo presentaban más ADNmt circulante y mitocondrias descelularizadas, respuestas de interferón más fuertes, puntuaciones más altas de fallo orgánico y perfiles de autoanticuerpos más amplios, incluyendo anticuerpos contra ADN y proteínas nucleares. Estos patrones reflejaron de cerca los hallazgos en ratones, apoyando la idea de que el control por TMEM110 de la estabilidad lisosomal y la eliminación del ADNmt es un mecanismo compartido en la enfermedad humana.
Qué significa esto para pacientes con traumatismos graves
En términos cotidianos, este trabajo sugiere que tras una lesión grave nuestro sistema inmune se enfrenta a una elección delicada: digerir silenciosamente la avalancha de ADN propio liberada por las células moribundas, o interpretarla como una invasión viral y lanzar un ataque total que puede dañar nuestros propios órganos. TMEM110, al ajustar un canal iónico lisosomal y coordinarse con el sensor de ADN STING, ayuda a las células a elegir la vía más segura. Cuando este sistema falla —porque falta TMEM110, STING está mutado o los lisosomas se ven desbordados— el ADNmt se escapa, la alarma no cesa y se produce daño multiorgánico. Apuntar a este eje TMEM110–TRPML1–STING, por ejemplo con terapias de ARNm dirigidas a los lisosomas, podría ofrecer una nueva forma de prevenir o tratar la insuficiencia orgánica y las complicaciones de tipo autoinmune tras un trauma severo.
Cita: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Palabras clave: lesión cerebral traumática, ADN mitocondrial, lisosomas, interferón tipo I, vía cGAS-STING