Clear Sky Science · es
Microneedles con nanomotores activados por luz de infrarrojo cercano para la terapia activa del acné infectado por bacterias
Por qué importa esta investigación sobre el acné
El acné a menudo se minimiza como una molestia estética, pero para adolescentes y adultos puede ser doloroso, dejar cicatrices y afectar emocionalmente. Los tratamientos estándar, especialmente los antibióticos, pueden provocar efectos secundarios y favorecer bacterias resistentes a los fármacos. Este estudio describe un parche de microneedles impulsado por una luz de infrarrojo cercano inocua que libera diminutos "nanomotores" directamente en las lesiones de acné. Estas partículas inteligentes generan su propio oxígeno, se desplazan activamente a través de las capas de baba bacteriana y se calientan lo justo para matar gérmenes y calmar la inflamación, ofreciendo una visión de futuros cuidados del acné más dirigidos y menos dependientes de antibióticos.
Cómo el acné se convierte en una protuberancia inflamada
La mayoría de los casos de acné comienzan cuando los poros y folículos pilosos se tapan con grasa y células muertas de la piel. Dentro de estos folículos obstruidos, una bacteria llamada Cutibacterium acnes (anteriormente Propionibacterium acnes) se multiplica en un entorno con poco oxígeno. Los microbios forman biófilms protectores —comunidades pegajosas envueltas en una matriz densa— que los protegen de los fármacos. Al alimentarse de los aceites de la piel, liberan ácidos grasos que reducen aún más el oxígeno e irritan las células cercanas. La piel responde produciendo señales inflamatorias como TNF‑α e interleuquinas, y las células inmunitarias locales que normalmente mantienen el equilibrio microbiano se agotan. En conjunto, estos cambios provocan el enrojecimiento, la hinchazón y, a veces, las cicatrices que se observan en el acné resistente.
Por qué las cremas y pastillas suelen quedarse cortas
Las cremas y geles tópicos tienen dificultades para atravesar la barrera externa de la piel, y los antibióticos orales exponen todo el organismo a medicación solo para alcanzar una zona pequeña, aumentando el riesgo de efectos secundarios y cepas resistentes. En una lesión madura de acné, el biófilm espeso alrededor de C. acnes bloquea aún más la penetración. Incluso la terapia fototérmica —que usa partículas absorbentes de luz para generar calor que mata bacterias— encuentra limitaciones, porque las partículas no pueden moverse profundamente dentro del biófilm, y el entorno ácido y con poco oxígeno alrededor de la lesión alimenta la inflamación crónica en lugar de la curación.
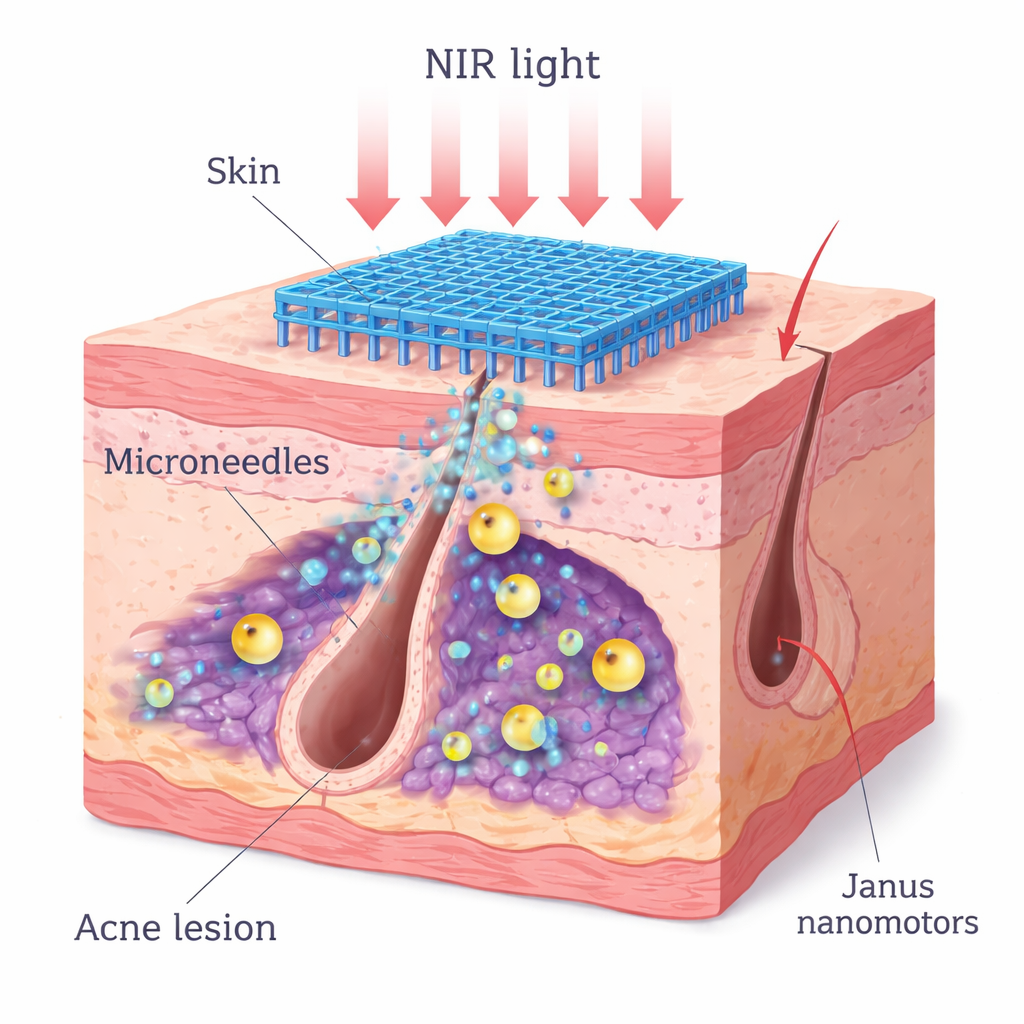
Un parche de microneedles activado por luz con pequeños motores
Los investigadores diseñaron un parche de microneedles disoluble que penetra sin dolor justo por debajo de la superficie de la piel y libera nanomotores diseñados. Cada nanomotor tiene un núcleo de peróxido de zinc que se descompone lentamente en condiciones ácidas, liberando peróxido de hidrógeno, que a su vez es convertido en oxígeno por una cubierta de dióxido de manganeso. Un lado de la partícula está recubierto con una capa absorbente de luz de polidopamina y dióxido de manganeso, creando una estructura tipo "Janus" (de dos caras). Cuando un láser de 808 nm en el infrarrojo cercano ilumina la piel, este recubrimiento asimétrico calienta un lado más que el otro, creando un gradiente de temperatura que impulsa la partícula hacia adelante. Esta autopropulsión ayuda a los nanomotores a difundirse a través de biófilms densos y espacios foliculares mientras simultáneamente entregan calor para debilitar las defensas bacterianas.
Del banco de laboratorio a la piel de ratón
En pruebas de laboratorio, los nanomotores se calentaron de manera eficiente bajo luz de infrarrojo cercano, se mantuvieron estables tras ciclos repetidos y liberaron más peróxido de hidrógeno y oxígeno en condiciones ácidas similares a las de un biófilm. Los parches de microneedles hechos de ácido hialurónico compatible con la piel fueron lo bastante resistentes para perforarla pero se disolvieron en aproximadamente media hora, liberando los nanomotores en la dermis. Bajo el haz de luz, las partículas mostraron un movimiento claramente aumentado y penetraron más profundamente tanto en biófilms artificiales como en piel de cerdo. En cultivos bacterianos de C. acnes y Staphylococcus aureus resistente a fármacos, la combinación de microneedles, nanomotores y cinco minutos de exposición al infrarrojo cercano redujo la masa del biófilm y la supervivencia bacteriana en más del 90 por ciento, y provocó daños visibles en las membranas y el ADN microbianos.
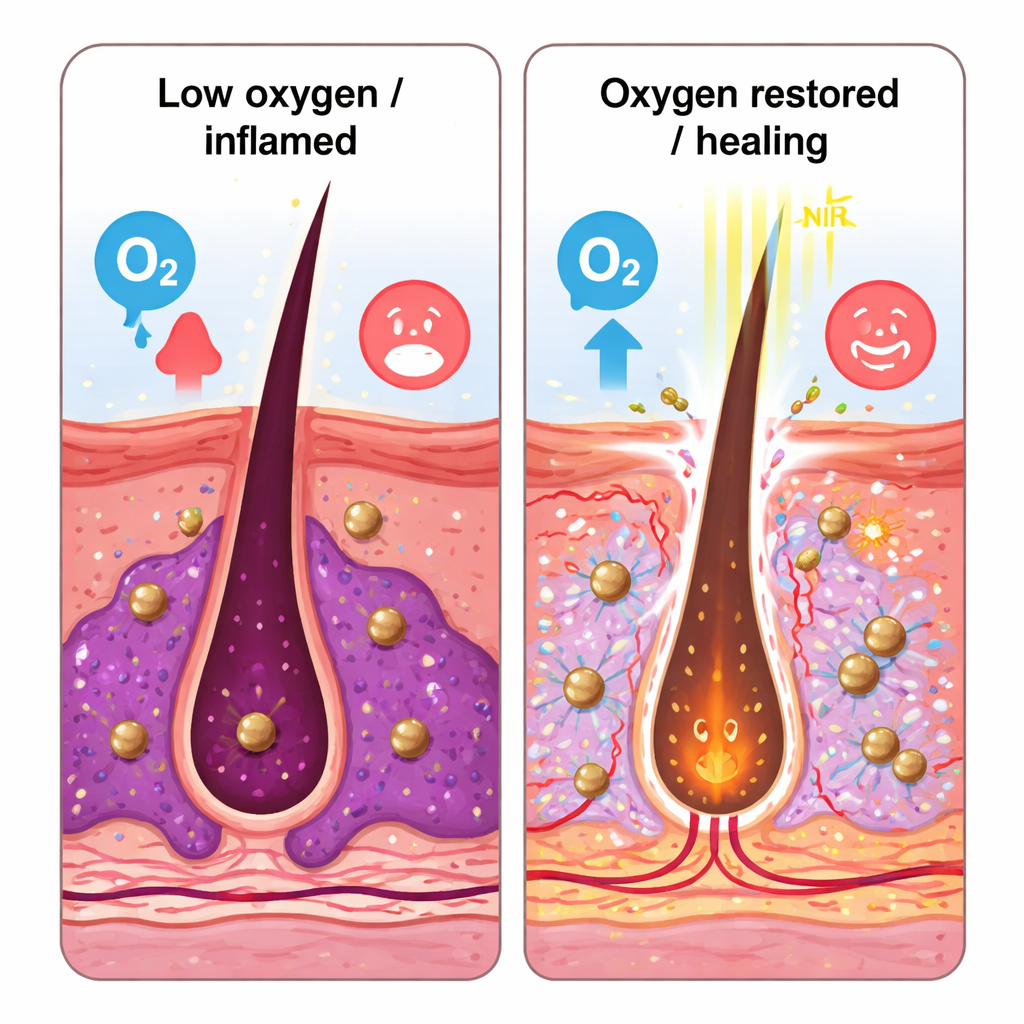
Calmar la inflamación y restaurar el equilibrio
En un modelo de ratón de acné, creado mediante la inyección de C. acnes en la piel, el parche activado por luz redujo el tamaño de las lesiones y el recuento bacteriano con la misma eficacia que el antibiótico eritromicina, pero sin daño tisular evidente. Las secciones de piel de los ratones tratados mostraron menos células inflamatorias, niveles más bajos de moléculas inflamatorias (IL‑6, TNF‑α) y menor actividad de HIF‑1α, un marcador de hipoxia. Al mismo tiempo, aumentaron marcadores de la formación de nuevos vasos sanguíneos y la reparación de heridas, y células inmunitarias clave llamadas ILC3, que habían sido suprimidas por la infección, se recuperaron y produjeron más del factor de reparación IL‑22. Los autores sugieren que, al suministrar oxígeno y descomponer físicamente los biófilms, los nanomotores ayudan a normalizar tanto el microbioma local como el entorno inmunológico de la piel.
Qué podría significar esto para el cuidado futuro del acné
Para el lector general, la conclusión es que este sistema de microneedles y nanomotores actúa como un tratamiento inteligente y localizado: abre suavemente un camino a través de la piel, dirige pequeños motores hacia el corazón de una lesión de acné y, con un breve pulso de luz invisible, entrega calor y oxígeno exactamente donde se necesitan. En ratones, este enfoque eliminó la infección, alivió la inflamación y favoreció la reparación tisular, igualando el rendimiento de los antibióticos sin exponer a todo el organismo a la medicación. Aunque aún hacen falta ensayos en humanos y estudios de seguridad a largo plazo, el trabajo apunta a una nueva clase de terapias contra el acné que combinan penetración mecánica, activación a demanda y generación propia de oxígeno para abordar las infecciones basadas en biófilms de manera más precisa y con menos efectos secundarios.
Cita: Hu, Z., Gan, Y., Song, Y. et al. Near-infrared light-driven nanomotors-based microneedles for the active therapy of bacterial infected acne. Nat Commun 17, 1675 (2026). https://doi.org/10.1038/s41467-026-68376-6
Palabras clave: tratamiento del acné, parche de microneedles, nanomotores, terapia por infrarrojo cercano, biófilms bacterianos