Clear Sky Science · es
Estructura por criomicroscopía electrónica del complejo humano ubiquitina ligasa COP1-DET1
Cómo las células deciden qué proteínas destruir
En el interior de cada célula, miles de proteínas deben construirse, remodelarse o destruirse constantemente en el momento adecuado. Este artículo analiza una de las máquinas clave de “control de calidad” de la célula, un triturador molecular que decide cuándo eliminar reguladores génicos potentes vinculados con el cáncer y el desarrollo. Al revelar su estructura tridimensional con detalle cercano al atómico, los autores muestran cómo esta máquina puede alternar entre un estado apilado e inactivo y una forma activa que procesa sustratos, un conocimiento que podría ayudar en el futuro a diseñar fármacos para activarla o inhibirla.
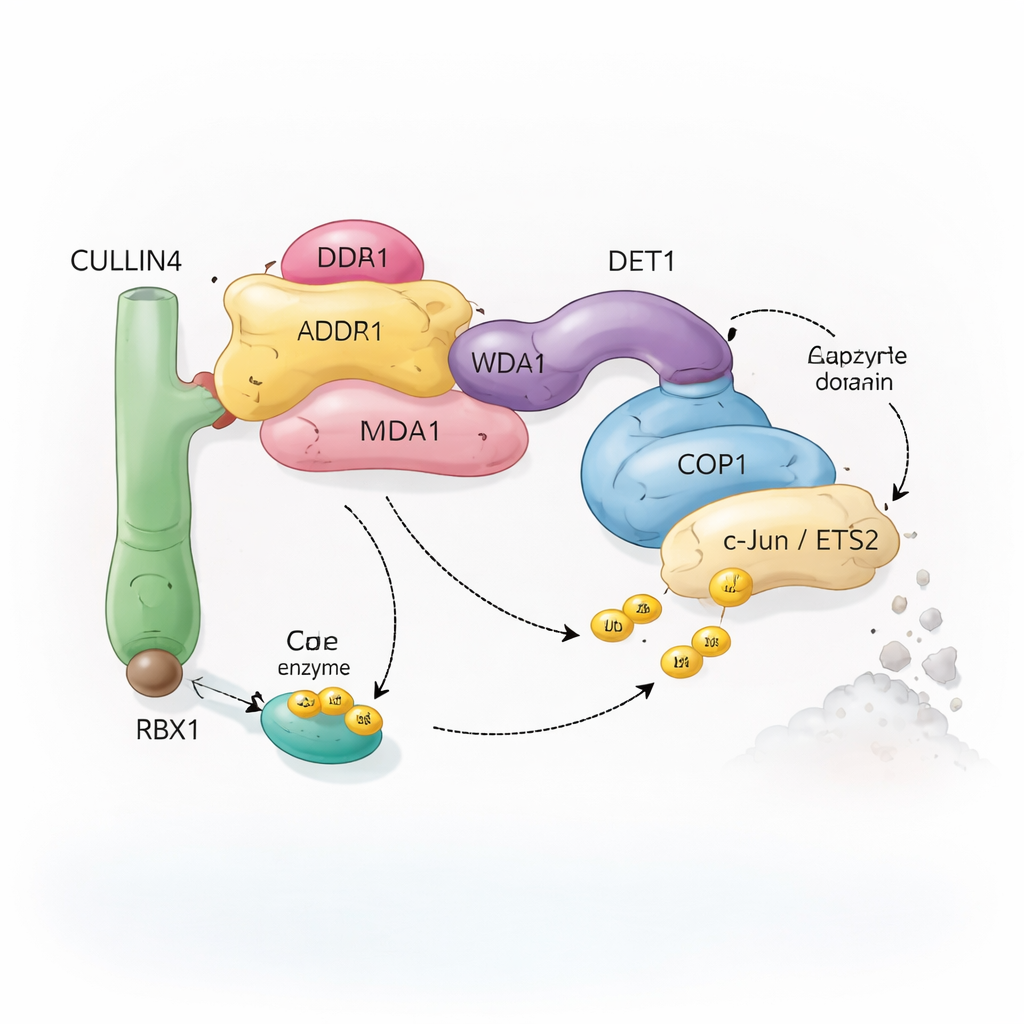
Un equipo molecular de reciclaje con muchas piezas
Las células dependen de un sistema llamado ubiquitinación para marcar proteínas destinadas al reciclaje. Pequeñas moléculas de ubiquitina actúan como banderas removibles que indican a la célula si una proteína debe modificarse, reubicarse o destruirse. Complejos enzimáticos especiales, conocidos como ligasas de ubiquitina, adjuntan estas banderas a dianas seleccionadas. El complejo estudiado aquí se centra en COP1, una proteína presente desde plantas hasta humanos, que ayuda a marcar factores de transcripción importantes—proteínas que controlan qué genes se activan o desactivan. COP1 no actúa solo: puede integrarse en un ensamblaje mayor construido alrededor de una proteína andamio llamada CULLIN4, además de varios adaptadores denominados DDB1, DDA1 y DET1. Juntos, estos componentes forman un “equipo de reciclaje” flexible que reconoce factores de transcripción específicos como c‑Jun y ETS2, muchos de los cuales están implicados en el crecimiento celular y el cáncer.
Capturando el complejo en 3D
Para entender cómo opera este equipo, los investigadores usaron criomicroscopía electrónica de partículas individuales, una técnica que imagina proteínas congeladas instantáneamente y reconstruye sus formas con alta resolución. Recrearon el sistema humano COP1–DET1 en células en cultivo, purificaron los complejos y visualizaron varios estados estructurales distintos. Primero resolvieron la estructura del módulo DDB1–DDA1–DET1, que actúa como un centro neurálgico. DET1 adopta una forma inusual y parcialmente flexible en lugar de un disco rígido, con una “garra” saliente que puede sujetar enzimas asociadas. Luego, al añadir COP1 y una clase de enzimas auxiliares conocidas como E2, capturaron ensamblajes mayores que muestran cómo encajan todas las piezas, revelando tanto pilas compactas como arreglos diméricos más abiertos (dos COP1).
Una pila inactiva y un dímero activo
Uno de los hallazgos más llamativos es una estructura apilada, filamentosa, formada por capas repetidas del complejo. En cada capa, ocho moléculas de COP1 se entrelazan a través de sus segmentos de hélice enrollada, formando un anillo con forma de diamante. Sus regiones de reconocimiento de sustratos, llamadas dominios WD40, apuntan en una sola dirección y quedan parcialmente protegidas por las capas vecinas. Este empaquetamiento estrecho probablemente representa un estado “apagado” en el que el acceso para las proteínas diana está limitado. En contraste, cuando el equipo examinó complejos coexpresados con sustratos de COP1 como c‑Jun o ETS2, vieron una forma diferente, dimérica: dos moléculas de COP1 dispuestas lado a lado, con sus dominios WD40 orientados hacia el exterior y disponibles para unirse a los cortos motivos “VP” presentes en muchos factores de transcripción. Pruebas bioquímicas confirmaron que solo este estado dimérico soporta de manera eficiente la construcción de largas cadenas de ubiquitina sobre c‑Jun.
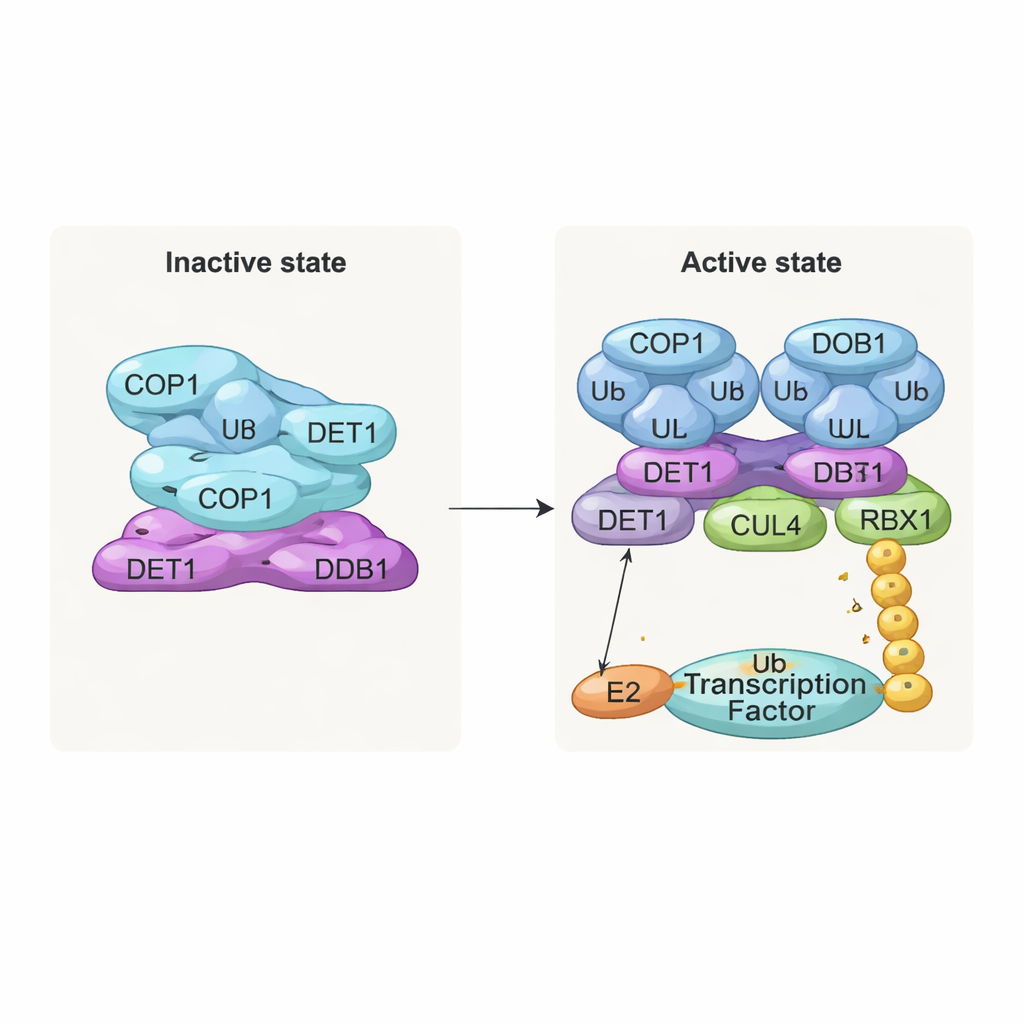
DET1 como puente flexible y director de tráfico
DET1 emerge como el organizador clave que enlaza todas las partes de la máquina. Su región N‑terminal se anida en DDB1, anclando el complejo al andamio CULLIN4, mientras que su región de garra se envuelve alrededor de una familia de enzimas E2 llamadas Ube2e. Experimentos detallados de mutagénesis muestran que DET1, y no COP1, es lo que sujeta directamente a estos E2, posicionándolos cerca de la región catalítica RING de COP1. En este arreglo, Ube2e parece ayudar a colocar las primeras marcas de ubiquitina sobre el sustrato. Una segunda enzima E2, Ube2d3, es entonces reclutada vía el brazo CULLIN4–RBX1 para extender estas marcas en cadenas más largas que señalan la degradación completa. En otras palabras, DET1 actúa como un puente flexible que presenta un E2 a COP1, mientras que el andamio mayor trae un segundo E2 para terminar el trabajo.
Por qué esto importa para la salud y la enfermedad
Al mapear estos estados estructurales y sus actividades, el estudio explica cómo el mismo conjunto de proteínas puede alternar entre una forma inactiva y apilada y un dímero activo que dirige factores de transcripción hacia la destrucción. Este interruptor es especialmente importante para factores como c‑Jun, que impulsan la división celular y están fuertemente vinculados al cáncer cuando se desregulan. Comprender cómo cooperan COP1 y DET1—cómo la garra de DET1 selecciona E2 específicos, cómo la superficie WD40 de COP1 reconoce sustratos que contienen VP y cómo se forma el dímero activo—proporciona un plano para trabajos futuros. A largo plazo, fármacos que estabilicen la pila inactiva o favorezcan el dímero activo podrían ofrecer a los investigadores nuevas formas de ajustar las vías de control génico en el cáncer y en otras enfermedades donde la degradación proteica falla.
Cita: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Palabras clave: ligasa de ubiquitina, COP1, degradación de proteínas, estructura por criomicroscopía electrónica, c-Jun