Clear Sky Science · es
INCENP y CDCA8 predicen la respuesta a quimioterapia neoadyuvante y los resultados en carcinoma escamoso de esófago
Por qué esta investigación importa para los pacientes con cáncer
Muchas personas con cánceres de esófago, mama o pulmón reciben quimioterapia intensiva antes de la cirugía para reducir sus tumores. Sin embargo, sólo alrededor de la mitad de estos pacientes se benefician realmente; para el resto, los fármacos provocan efectos secundarios sin frenar el cáncer. Este estudio plantea una pregunta simple pero crucial: ¿podemos predecir de antemano quién responderá a la quimioterapia, y podemos mejorar el tratamiento para quienes hoy no responden?
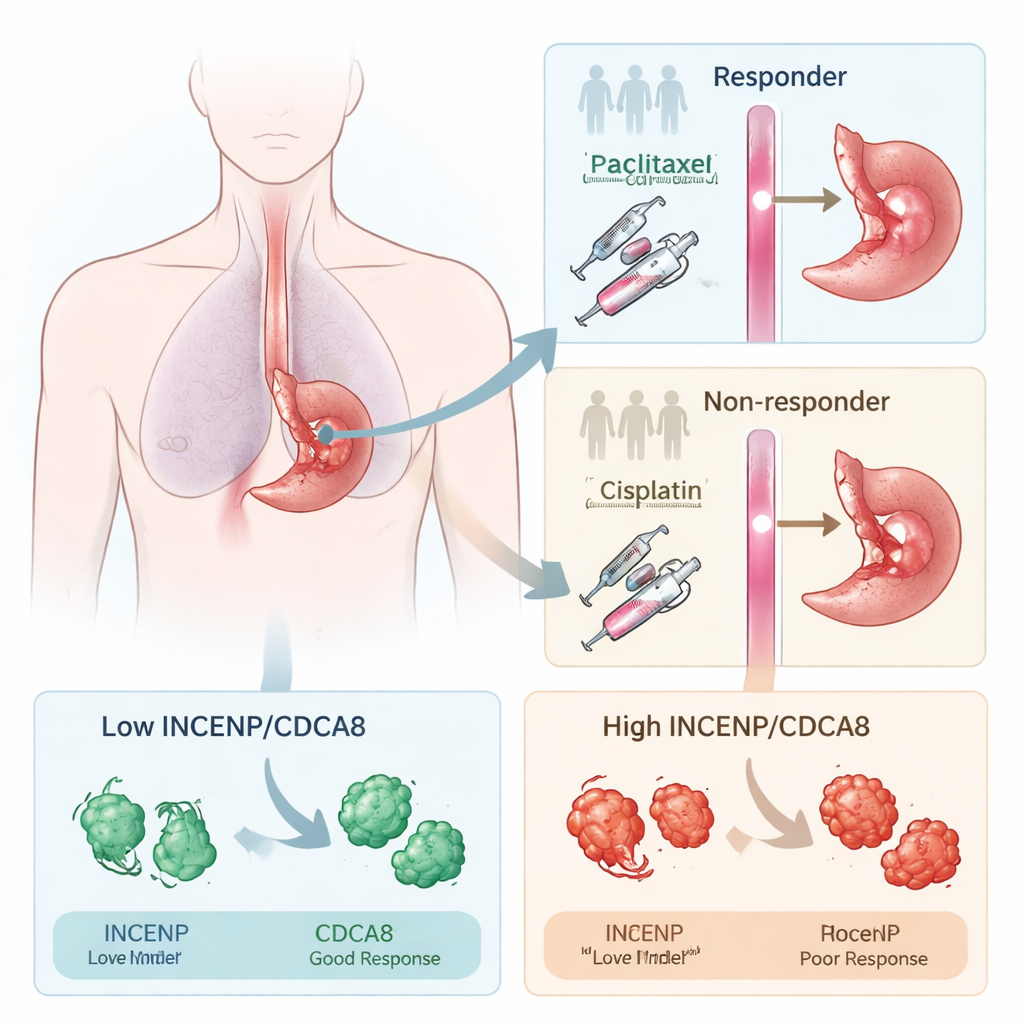
Detectar quién responde al tratamiento
Los investigadores se centraron en un régimen preoperatorio estándar que combina paclitaxel y cisplatino, usado ampliamente en varios cánceres. Trabajando primero con pacientes con carcinoma escamoso de esófago, compararon muestras tumorales de personas cuyos tumores se redujeron notablemente tras esta terapia (respondedores) con muestras de aquellos cuyos tumores apenas cambiaron (no respondedores). Al sondear qué genes estaban activados o reprimidos, hallaron que muchas diferencias involucraban cómo las células se dividen, un proceso que la quimioterapia pretende alterar. Dos proteínas que ayudan a controlar la separación de cromosomas durante la división celular, INCENP y CDCA8, se destacaron repetidamente por estar mucho más altas en tumores resistentes al tratamiento.
Dos proteínas que señalan probable resistencia
Para comprobar si INCENP y CDCA8 eran meros observadores o causantes activos de la resistencia, el equipo modificó sus niveles en células de cáncer de esófago cultivadas en el laboratorio. Cuando redujeron cualquiera de las dos proteínas, las células cancerosas se volvieron mucho más sensibles a paclitaxel y cisplatino, formaron menos colonias y mostraron dosis mucho menores necesarias para matarlas. Cuando forzaron a las células a producir más INCENP o CDCA8, sucedió lo contrario: los fármacos fueron menos eficaces. En ratones implantados con tumores esofágicos humanos, la reducción de estas proteínas hizo que la quimioterapia redujera los tumores con más intensidad. Los pacientes cuyos tumores contenían altos niveles de INCENP y CDCA8 antes del tratamiento también tendieron a tener progresión de la enfermedad y supervivencia más corta, lo que refuerza su valor como señales de alarma.
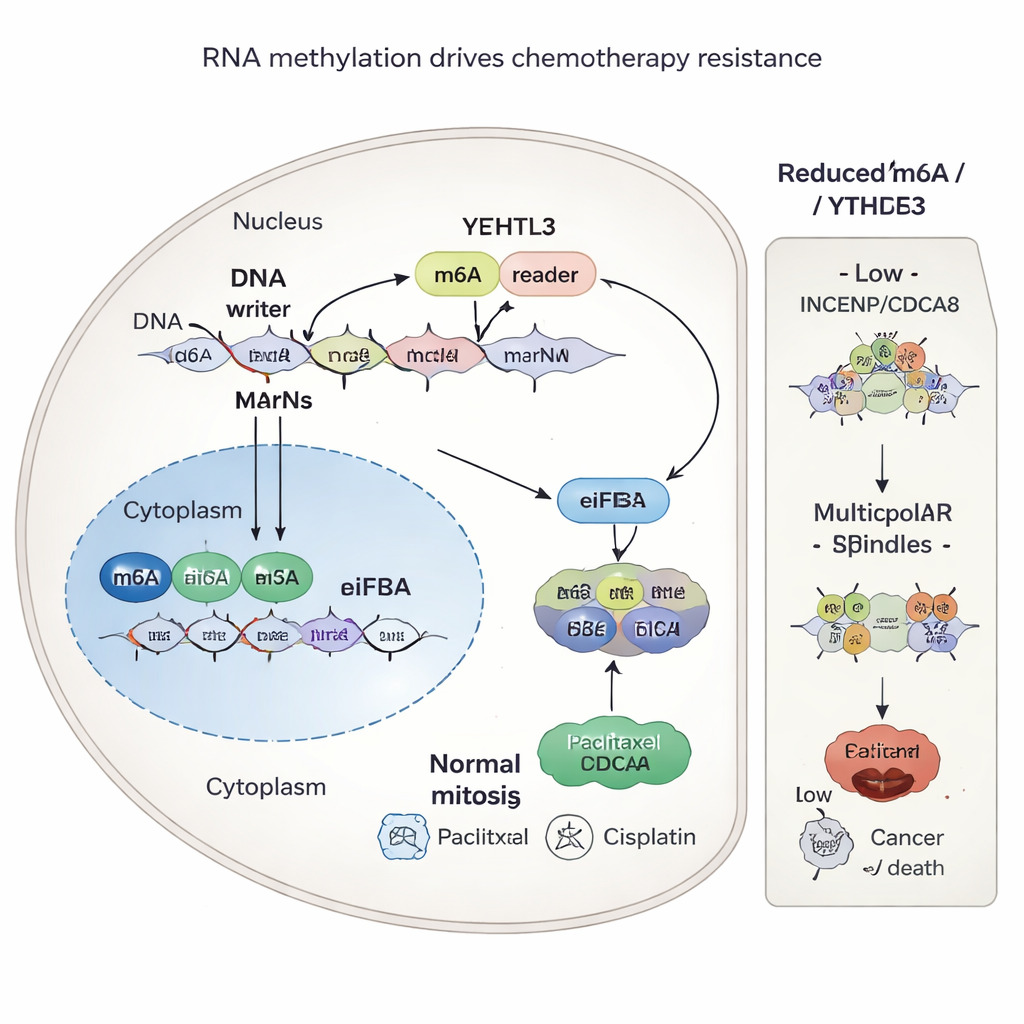
Una etiqueta química en el ARN que alimenta la resistencia
El estudio preguntó luego por qué INCENP y CDCA8 son tan abundantes en tumores resistentes. La respuesta se remontó a una sutil marca química en el ARN llamada m6A, que actúa como una perilla que regula la eficiencia con la que los mensajes genéticos se traducen en proteína. Una enzima llamada METTL3 añade estas marcas m6A en puntos específicos de los planos de ARN para INCENP y CDCA8. Otra proteína, YTHDF3, reconoce estas marcas y ayuda a reclutar la maquinaria de síntesis proteica de la célula, aumentando la producción de ambas proteínas. Cuando los científicos redujeron METTL3 o YTHDF3, o bloquearon YTHDF3 con una pequeña molécula llamada Ebselen, las marcas m6A se perdieron o fueron ignoradas, los niveles proteicos de INCENP y CDCA8 cayeron y las células cancerosas se volvieron más vulnerables a la quimioterapia.
Interrumpir la división celular para ayudar a la quimioterapia
INCENP y CDCA8 forman parte de una máquina mayor llamada complejo pasajero cromosómico que asegura que los cromosomas se repartan de forma pareja entre las células hijas. En células resistentes, los niveles altos de estas proteínas ayudan a mantener husos bipolares ordenados durante la división celular, lo que permite al cáncer sobrevivir al daño causado por paclitaxel y cisplatino. Cuando se suprimen INCENP y CDCA8, las células suelen formar husos defectuosos con múltiples polos. Este caos en la segregación cromosómica empuja a las células cancerosas hacia la muerte, amplificando el poder letal de la quimioterapia. Es crucial que la capacidad de INCENP y CDCA8 para proteger a las células dependía de esos sitios m6A específicos en su ARN; mutar esos sitios eliminó la resistencia.
Más allá de un tipo de cáncer
Dado que paclitaxel más cisplatino también se utilizan en cánceres de pulmón y mama, el equipo examinó biopsias de pacientes con esos tumores. En los tres tipos de cáncer, las personas cuyos tumores tenían bajos niveles de INCENP, CDCA8 y YTHDF3 antes de la terapia eran mucho más propensas a responder bien al tratamiento. Los análisis estadísticos mostraron que la combinación de estos tres marcadores ofrecía una potencia particularmente buena para distinguir probables respondedores de no respondedores, lo que sugiere un panel de prueba práctico que podría emplearse en varios cánceres.
Qué significa esto para pacientes y médicos
En términos sencillos, este trabajo identifica una “huella” molecular que ayuda a explicar por qué algunos tumores resisten a quimioterapias potentes. Altos niveles de INCENP y CDCA8, impulsados por un sistema de control basado en m6A que involucra METTL3 y YTHDF3, mantienen a las células cancerosas dividiéndose de forma ordenada incluso bajo el ataque de los fármacos. Medir estas proteínas en una biopsia podría ayudar a los médicos a predecir si paclitaxel más cisplatino probablemente beneficiará a un paciente, evitando que otros reciban un tratamiento ineficaz. Al mismo tiempo, fármacos que bloqueen esta vía podrían combinarse con la quimioterapia estándar para forzar a los tumores resistentes a cometer errores fatales en la división, mejorando potencialmente la supervivencia en pacientes con varios cánceres importantes.
Cita: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Palabras clave: quimioterapia neoadyuvante, carcinoma escamoso de esófago, resistencia a la quimioterapia, biomarcadores INCENP y CDCA8, metilación de ARN m6A