Clear Sky Science · es
Proteasas dependientes de ubiquitina K48 cortan proteínas post-RER
Cómo las células deciden qué proteínas destruir
Nuestras células eliminan continuamente proteínas desgastadas o dañadas, en particular las que están embebidas en membranas y actúan como puertas y sensores. Este artículo revela que las células emplean una pequeña etiqueta llamada ubiquitina no solo como una marca genérica de “basura”, sino como un código que indica exactamente cómo se degradarán las proteínas de membrana. Comprender este código ayuda a explicar cómo las células mantienen su salud y podría orientar terapias futuras que destruyan deliberadamente proteínas causantes de enfermedad.
Un código de barras celular para desechar proteínas
Las células decoran las proteínas no deseadas con cadenas de una pequeña proteína llamada ubiquitina. Estas cadenas pueden unirse de maneras distintas, algo así como cuentas ensartadas por agujeros diferentes, y cada patrón puede señalar un destino distinto. Los autores se centraron en proteínas de membrana que ya han salido del retículo endoplásmico (RER) y viajan por compartimentos como el aparato de Golgi y endosomas. Se preguntaron si dos tipos de cadenas comunes, llamadas ubiquitina unida por K48 y por K63, son realmente etiquetas intercambiables o si dirigen la carga hacia rutas diferentes de degradación.
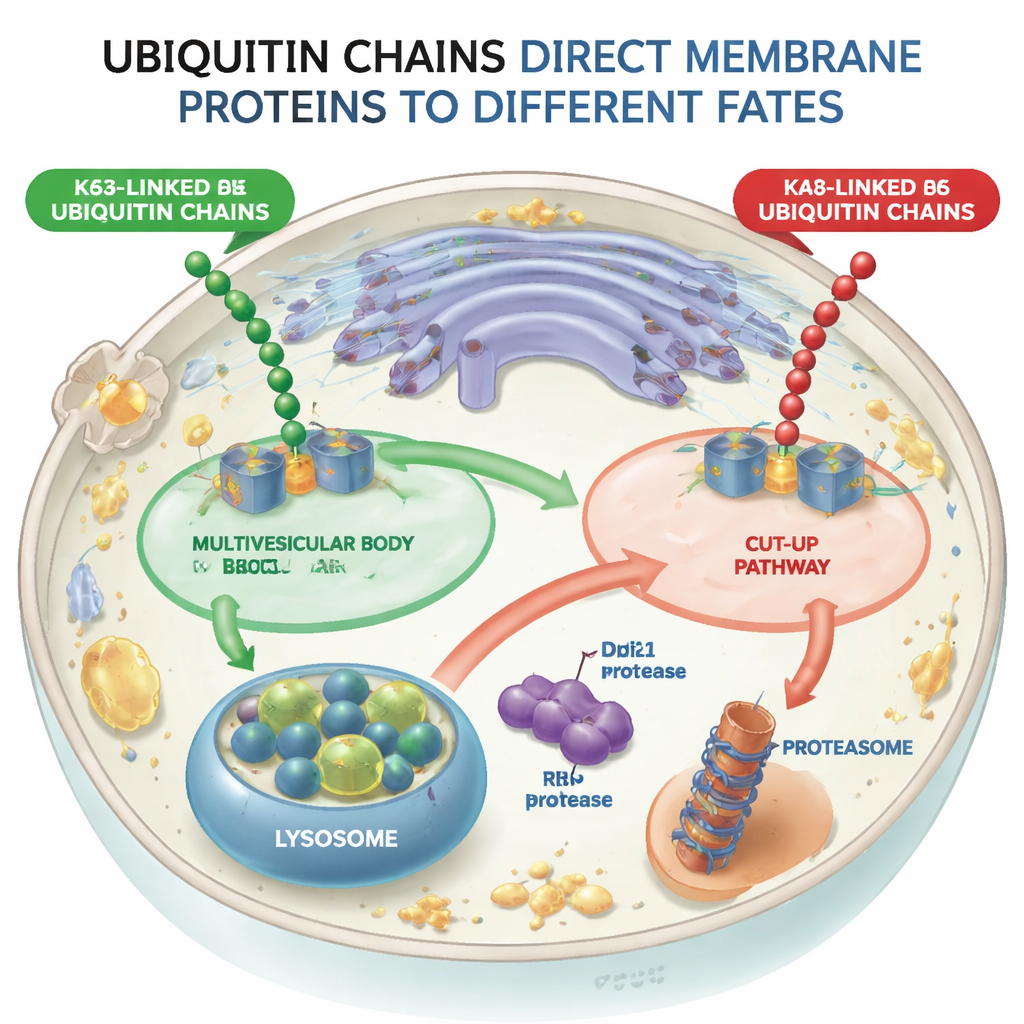
Dos vías divergentes para proteínas etiquetadas
Usando células de levadura como modelo, los investigadores diseñaron máquinas moleculares (ligasas de ubiquitina) que podían añadir cadenas unidas por K48 o por K63 a la misma proteína de membrana de prueba, un receptor de clasificación llamado Vps10. Cuando Vps10 recibió cadenas unidas por K63, fue enviado a vesículas internas dentro de los endosomas—estructuras conocidas como cuerpos multivesiculares—que finalmente se fusionan con los lisosomas, los compartimentos digestivos de la célula. En contraste, cuando Vps10 portaba cadenas unidas por K48, no siguió esta ruta multivesicular. En su lugar, fue desmembrado de una manera completamente diferente, lo que demuestra que la célula distingue entre estos dos tipos de cadena y que la vía multivesicular rechaza eficazmente la carga etiquetada con K48.
Una vía de “corte” que parte las proteínas en dos
El equipo descubrió que las cadenas unidas por K48 activan una vía de cizallamiento proteico que llamaron CUT-UP, abreviatura de Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. En lugar de extraer la proteína entera de la membrana de una vez, CUT-UP la trocea en fragmentos que luego son rematados por los sistemas de eliminación ya existentes en la célula. Una enzima clave, Ddi1, flota en el citosol y corta la porción de la proteína de membrana que mira al citoplasma. Ese fragmento es después digerido por el proteasoma, el principal triturador de proteínas de la célula. Al mismo tiempo, otra enzima, Rbd2, se sitúa dentro de la propia membrana y corta la parte de la proteína que mira al lumen del compartimento, liberándola en el espacio que acaba comunicándose con el lisosoma. Bloquear conjuntamente Ddi1, Rbd2, el proteasoma y las enzimas lisosomales fue necesario para proteger completamente a Vps10 etiquetado con K48 de la destrucción, lo que confirma que todos estos componentes cooperan en la vía CUT-UP.
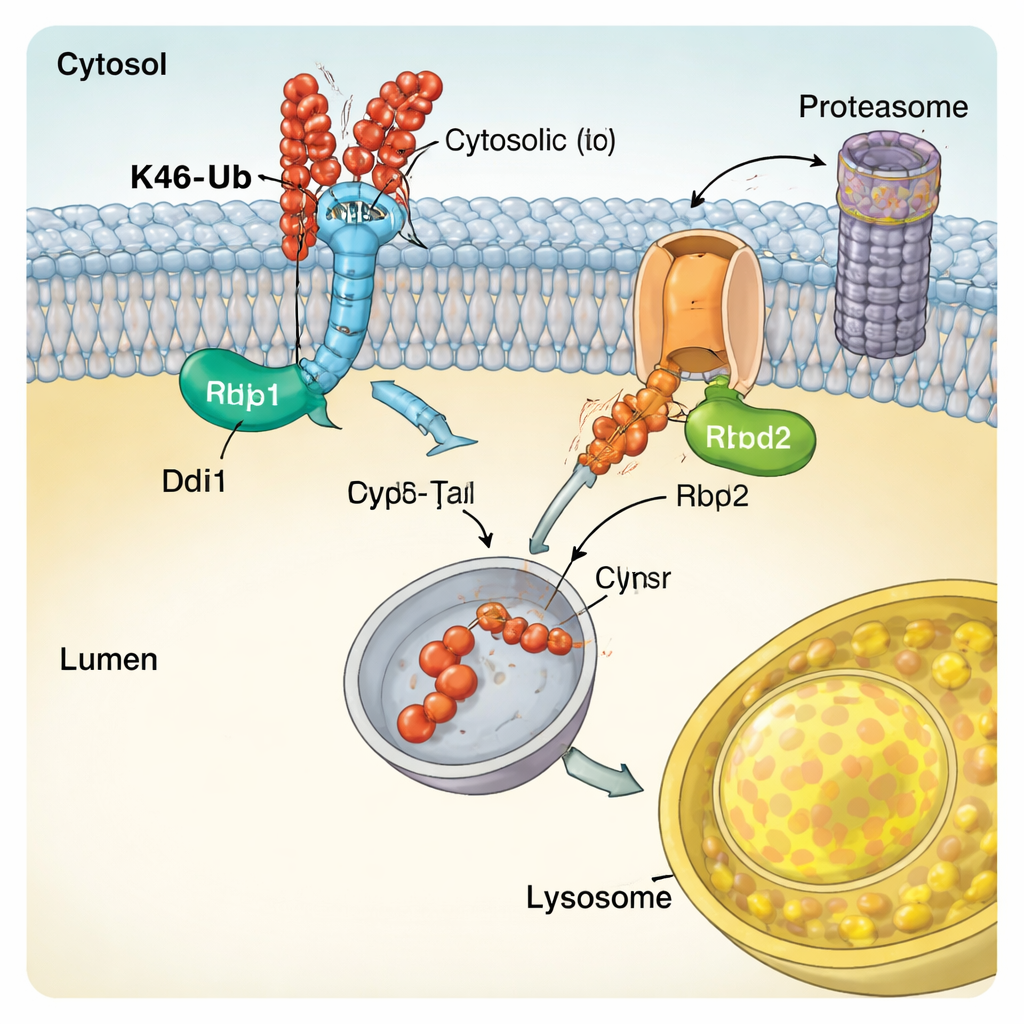
Enzimas especializadas que leen el código de ubiquitina
Para entender cómo CUT-UP reconoce sus objetivos, los autores examinaron las características moleculares de Ddi1. Demostraron que el núcleo catalítico central de Ddi1 no solo corta proteínas sino que también puede unirse directamente a la ubiquitina, y que su actividad se ajusta mediante regiones adicionales que se enganchan a las cadenas de ubiquitina. Ddi1 mostró una dependencia particular de las cadenas unidas por K48, coherente con su papel en CUT-UP. Rbd2, por otra parte, es una proteasa romboide que atraviesa la membrana. El estudio encontró que el sitio activo de Rbd2 es esencial para cortar las porciones de Vps10 que miran al lumen y que la enzima circula por varios compartimentos secretorios, lo que le permite actuar en múltiples localizaciones celulares. Existen enzimas similares en células humanas y se han implicado en condiciones que van desde la neurodegeneración hasta el cáncer, lo que sugiere que mecanismos similares a CUT-UP pueden ser de amplia importancia.
Por qué esto importa para la salud y la terapia
Al mostrar que distintos tipos de cadenas de ubiquitina envían a la misma proteína de membrana a destinos muy diferentes—ya sea la clasificación hacia cuerpos multivesiculares o el corte mediado por CUT-UP—este trabajo aporta evidencia sólida de que las células usan un auténtico “código de ubiquitina” para afinar la eliminación de proteínas. El descubrimiento de CUT-UP aclara cómo proteínas de membrana persistentes pueden ser desmontadas pieza a pieza e identifica a Ddi1 y Rbd2 como jugadores clave que leen y aplican este código. Para el público general, la conclusión es que las células no se limitan a marcar proteínas como basura; especifican cómo se sacará esa basura. A medida que los desarrolladores de fármacos diseñen herramientas que etiqueten proteínas dañinas con ubiquitina para eliminarlas, entender vías como CUT-UP será esencial para predecir qué fragmentos se producirán y cómo eso podría afectar el comportamiento celular.
Cita: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Palabras clave: código de ubiquitina, degradación de proteínas, proteínas de membrana, proteasoma, lisosoma