Clear Sky Science · es
Pérdida de la señalización por quorum Fsr favorece la formación de biopelículas y agrava el pronóstico en la endocarditis infecciosa por enterococos
Saboteadores silenciosos en las válvulas cardíacas
La endocarditis infecciosa es una infección potencialmente mortal de las válvulas del corazón y su incidencia está aumentando en todo el mundo. Este estudio se centra en un culpable principal, la bacteria intestinal Enterococcus faecalis, y plantea por qué algunas infecciones son especialmente difíciles de tratar. Al desvelar cómo estas bacterias se comunican entre sí y construyen biopelículas protectoras sobre las válvulas cardíacas, los investigadores muestran por qué determinadas cepas provocan una enfermedad más grave y resisten a los antibióticos, y por qué un sistema de comunicación bacteriana llamado Fsr resulta, sorprendentemente, ser un freno más que un acelerador del daño.
Cómo las bacterias levantan fortalezas en el corazón
Las válvulas cardíacas normalmente soportan algunos de los flujos sanguíneos más rápidos del cuerpo, pero si la superficie valvular se daña, las plaquetas y las proteínas de la coagulación pueden formar un pequeño coágulo o vegetación. Este coágulo se convierte en una plataforma de aterrizaje para bacterias en el torrente sanguíneo. Una vez adheridas, las bacterias se multiplican y se entrelazan en una biopelícula: una comunidad viscosa y estructurada que las protege de las células inmunitarias y de los fármacos. El equipo utilizó dispositivos microfluídicos para imitar el flujo sanguíneo en el laboratorio y un modelo en ratas para recrear la endocarditis en animales vivos, lo que les permitió observar cómo E. faecalis se adapta a medida que la infección progresa desde unas pocas células dispersas hasta biopelículas gruesas y maduras. 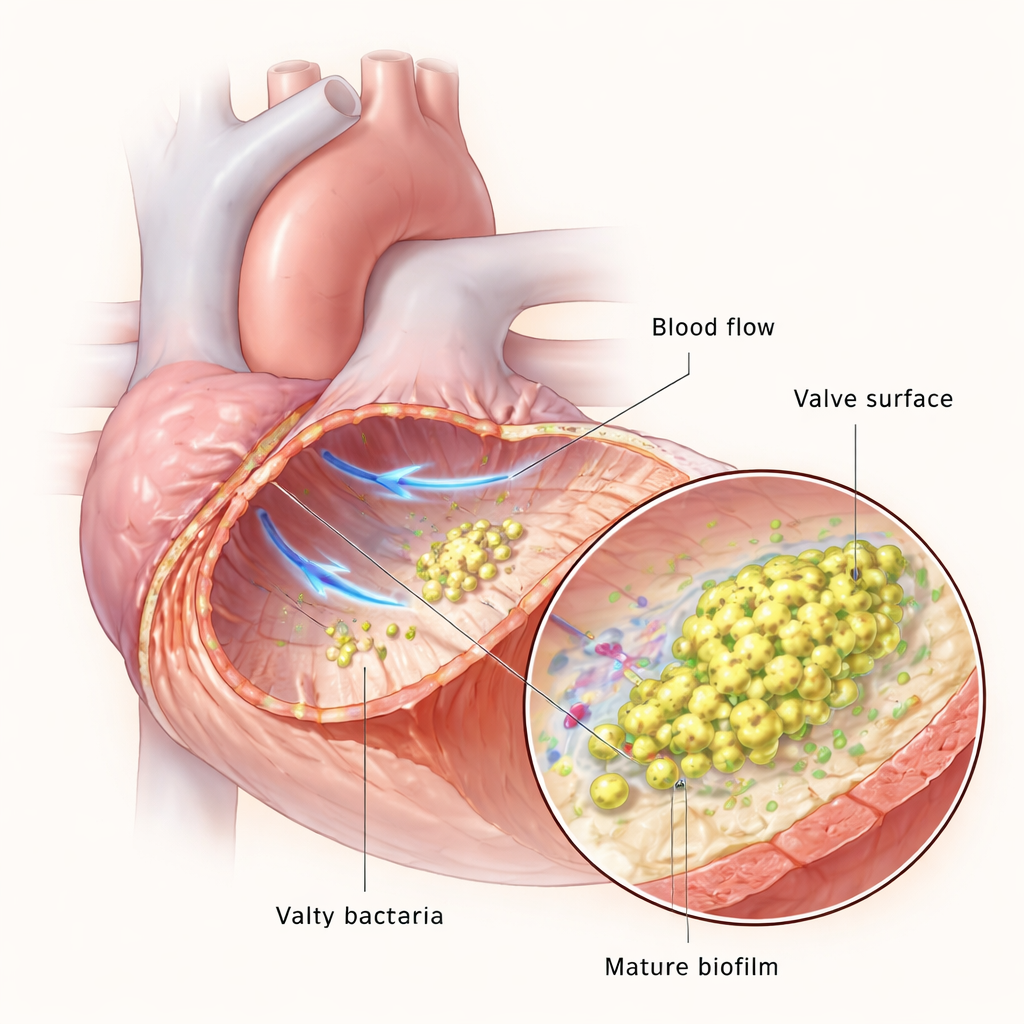
Cuando el flujo sanguíneo rápido apaga la “charla” bacteriana
Las bacterias a menudo coordinan su comportamiento mediante el quorum sensing, un sistema químico de “votación” que enciende o apaga genes cuando hay suficientes células presentes. Fsr es el sistema de quorum sensing que utiliza E. faecalis. Sorprendentemente, los investigadores observaron que el flujo fuerte y en movimiento realmente arrastra las moléculas señalizadoras necesarias para activar Fsr. En las fases tempranas de la infección, cuando las bacterias están ancladas en la superficie expuesta de la vegetación y sienten la fuerza del flujo sanguíneo, Fsr permanece en gran medida silencioso. Solo más tarde, cuando las microcolonias crecen y quedan sepultadas más profundamente dentro de la vegetación—protegidas del flujo—Fsr se activa. Esto significa que, en el corazón real, el quorum sensing no depende solo del número de bacterias, sino también de su posición dentro de la estructura tridimensional.
Apagar Fsr permite que las biopelículas se descontrolen
Para probar qué hace realmente Fsr en la infección, el equipo comparó bacterias normales con mutantes que carecían de todo el sistema Fsr. Al principio, ambas versiones colonizaban las válvulas por igual. Pero al cabo de tres días, los animales infectados con cepas deficientes en Fsr presentaban vegetaciones más grandes y muchas más bacterias compactadas en ellas. Las imágenes detalladas mostraron que sus biopelículas cubrían más la superficie del coágulo y sus microcolonias eran mayores. La pérdida de Fsr también silenciaba dos enzimas secretadas clave, GelE y SprE, que normalmente ayudan a dar forma a la biopelícula y pueden limitar el crecimiento excesivo. Los animales infectados con mutantes que carecían solo de estas enzimas también desarrollaron biopelículas más voluminosas, aunque no tan extremas como en las cepas nulas para Fsr, lo que sugiere que hay otros factores controlados por Fsr implicados. 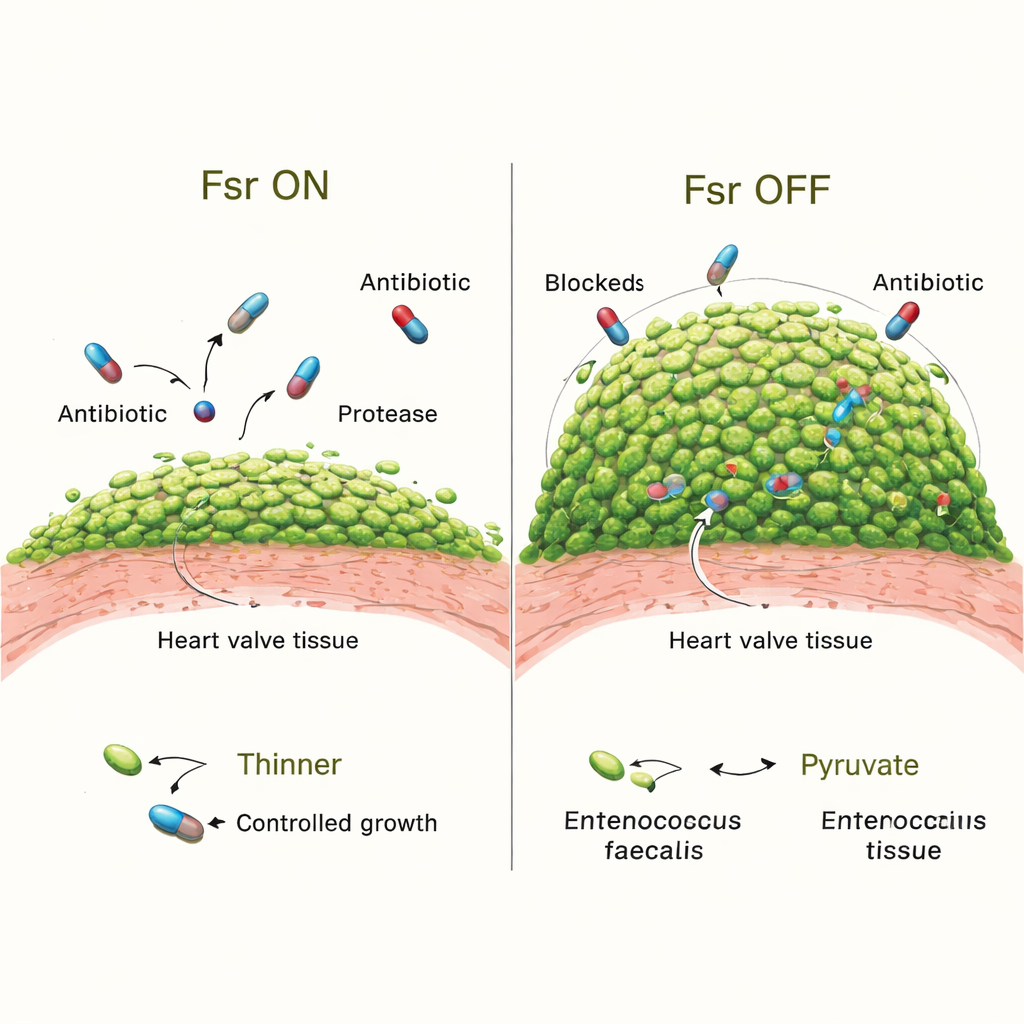
Reconfiguración metabólica y mayor resistencia frente a antibióticos
El perfil de expresión génica de las bacterias dentro de las válvulas infectadas reveló que Fsr hace más que controlar unas pocas enzimas. Sin Fsr, cientos de genes cambiaron su actividad, en especial los implicados en la captación de azúcares y la producción de energía. Un par de genes, lrgA y lrgB, destacó: estaban fuertemente activados en bacterias deficientes en Fsr y ayudaban a las células a explotar mejor el piruvato, una pequeña molécula energética presente en la sangre. Cuando los investigadores eliminaron lrgAB junto con Fsr, el crecimiento excesivo de la biopelícula desapareció, apuntando a un papel clave de esta vía metabólica en impulsar la infección desmesurada. Cabe destacar que las biopelículas deficientes en Fsr también resultaron más difíciles de tratar. En ratas tratadas con el antibiótico gentamicina, las infecciones con bacterias normales se redujeron y los recuentos de plaquetas—un marcador de gravedad—mejoraron. En contraste, las infecciones deficientes en Fsr respondieron muy poco, aunque las bacterias no mostraron mayor resistencia a los fármacos en las pruebas de laboratorio estándar.
Un matiz específico de humanos en la inflamación
El estudio también descubrió una posible vía por la que estas bacterias pueden agravar la inflamación en personas. La enzima GelE puede cortar el precursor humano de la señal inmune IL-1β en una forma activa que desencadena respuestas inflamatorias. De forma intrigante, GelE cortó la IL-1β de rata de manera diferente, degradándola en lugar de activarla, y el corte preciso necesario para la “activación” faltaba en las proteínas de rata y ratón. Este efecto específico de especie sugiere que en humanos GelE podría contribuir a concentrar la inflamación en el borde de la biopelícula, empeorando el daño tisular durante la endocarditis.
Del laboratorio a la clínica: por qué la pérdida de Fsr importa para los pacientes
Para comprobar si estos hallazgos experimentales tenían repercusión en la vida real, los investigadores analizaron aislamientos de E. faecalis de 81 pacientes con endocarditis infecciosa en Suiza y Estados Unidos. Casi la mitad de las cepas carecían de forma natural del sistema Fsr. Los pacientes infectados con estas cepas Fsr-negativas tuvieron bacteriemias de mayor duración—más días con bacterias detectables en sangre—y tenían más probabilidades de entrar en una categoría de alta gravedad que incluía cuidados intensivos, estancias hospitalarias prolongadas, procedimientos cardíacos mayores o muerte. Otros genes de virulencia no pudieron explicar este patrón, apuntando directamente a la pérdida de Fsr como un marcador clave de enfermedad más agresiva.
Por qué esto importa para tratamientos futuros
En conjunto, estos hallazgos desmienten la idea simplista de que bloquear la comunicación bacteriana siempre debilita las infecciones. En la endocarditis por E. faecalis, el sistema Fsr en realidad frena la expansión de la biopelícula y hace que las bacterias sean más vulnerables a los antibióticos. Cuando Fsr falta, las bacterias forman biopelículas más densas, aprovechan mejor los nutrientes de la sangre y contribuyen a infecciones persistentes y difíciles de erradicar. Para los pacientes, esto significa que las cepas sin Fsr pueden predecir enfermedades más difíciles de tratar, y que las terapias que cierran a ciegas el quorum sensing podrían resultar contraproducentes en este contexto. En su lugar, dirigir con cuidado vías metabólicas como el uso del piruvato, o monitorizar el estado de Fsr y GelE como marcadores pronósticos, puede ofrecer formas mejores de manejar estas peligrosas infecciones cardíacas.
Cita: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Palabras clave: endocarditis infecciosa, biopelículas bacterianas, quorum sensing, Enterococcus faecalis, tolerancia a antibióticos