Clear Sky Science · es
saRNA con VPg diseñado logra una codificación cap-independiente, baja inmunogenicidad y precisa de proteínas terapéuticas in vivo
Reescribiendo las reglas para los fármacos de ARN
Las vacunas basadas en ARN mensajero (ARNm) ayudaron a cambiar el rumbo frente a la COVID-19, pero usar moléculas similares para reemplazar o suplementar proteínas faltantes en enfermedades crónicas es mucho más difícil. El organismo tiende a destruir rápidamente el ARN extraño y a montar respuestas inmunitarias fuertes, y muchos diseños existentes de ARN autoamplificante cometen errores al copiarse. Este estudio describe un nuevo tipo de ARN autoamplificante —construido a partir de partes del norovirus humano— que ha sido diseñado para ser duradero, menos inflamatorio y extraordinariamente preciso, abriendo la puerta a medicinas de ARN más precisas y duraderas.
Un ARN auto-replicante más inteligente
Los fármacos convencionales de ARNm llevan una sola “receta” para una proteína y son leídos una vez por la célula antes de degradarse. El ARN autoamplificante (saRNA) incluye maquinaria viral adicional que permite que el ARN se copie dentro de las células, aumentando mucho la producción a partir de una dosis pequeña. Los sistemas de saRNA mejor estudiados proceden de alfavirus, pero son voluminosos, activan fuertes defensas antivirales y copian sus secuencias con una precisión relativamente baja. Los autores, en cambio, recurrieron al norovirus humano, una causa común de gastroenteritis. Aislaron una sección compacta del material genético del norovirus y la reconstruyeron como portadora de genes terapéuticos. En su núcleo está VPg, una pequeña proteína viral que se une químicamente al extremo delantero del ARN. VPg sustituye a la estructura de “cap” habitual en los ARNm humanos y permite que el ARN sea traducido por un conjunto distinto de factores celulares que son menos sensibles a ciertas señales de estrés. 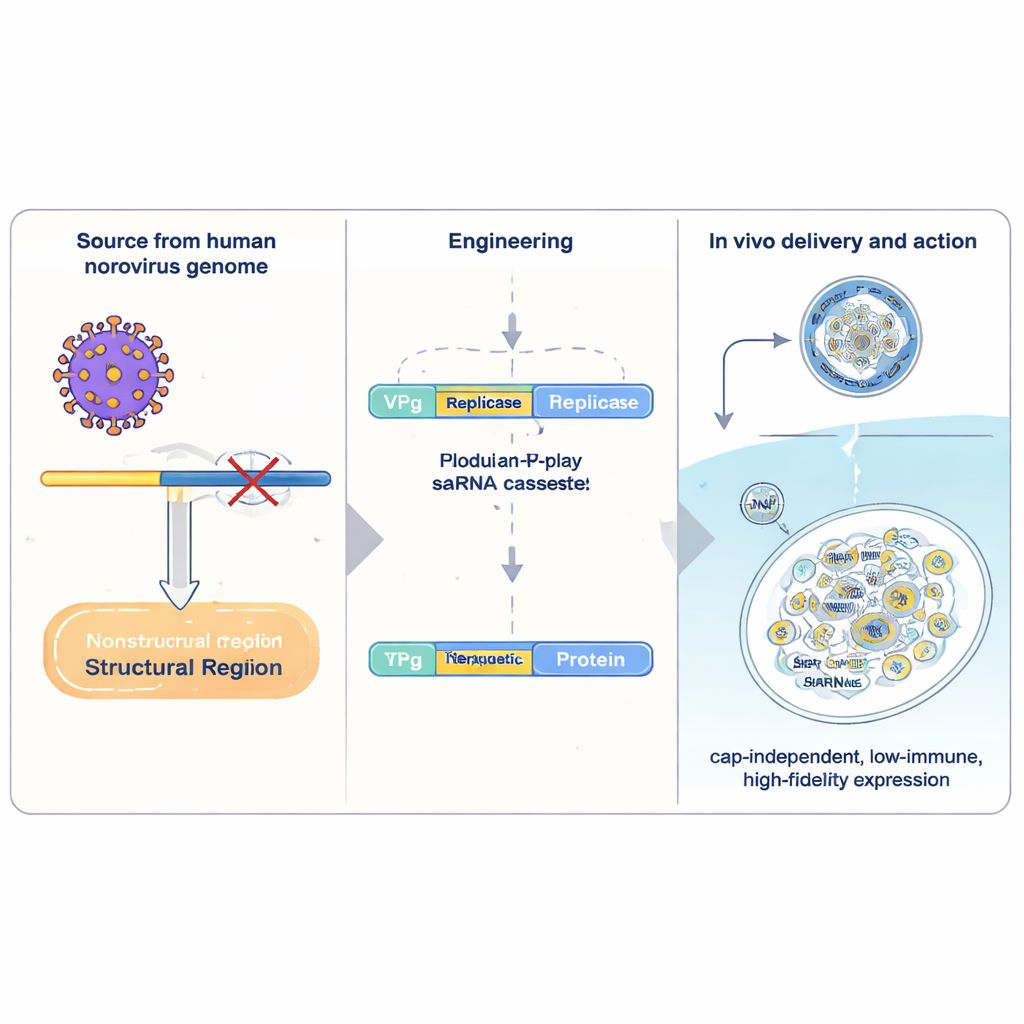
Alta precisión sin provocar la inmunidad
Para las terapias proteicas, la precisión importa: incluso pequeños errores de copia pueden alterar el comportamiento de un fármaco o generar subproductos tóxicos. El equipo mostró que cuando VPg del norovirus se une a la enzima copiadora de ARN del virus (una polimerasa), ralentiza la incorporación de bloques incorrectos, reduciendo drásticamente la tasa de errores. Identificaron aminoácidos específicos en VPg que contactan una región de control clave de la polimerasa y demostraron que perturbar esta interfaz empeora la fidelidad de copia. Al mismo tiempo, los diseños clásicos de saRNA generan grandes cantidades de ARN de doble cadena, una alarma molecular que activa defensas antivirales y detiene la producción proteica. Al rediseñar la polimerasa para favorecer una forma inicial ligada a VPg y al reorganizar el genoma para que solo la hebra terapéutica se produzca eficientemente, los autores redujeron en gran medida la formación de ARN de doble cadena. Además ajustaron una región cola del ARN para que VPg se acople en el sitio correcto, evitando fragmentos cortos e imprevistos que podrían traducirse en péptidos indeseados.
Funciona donde el ARNm estándar falla
El nuevo saRNA basado en VPg se probó en entornos patológicos exigentes donde el ARNm enmascarado estándar tiene dificultades. En la caquexia asociada al cáncer —un síndrome de desgaste en el que se pierden músculo y grasa— factores clave de traducción que reconocen el cap estándar se apagan, haciendo ineficaces los ARNm dependientes de cap. Dado que VPg utiliza un punto de entrada alternativo en la maquinaria de traducción celular, siguió impulsando la producción de la hormona ghrelina, reguladora del apetito y el metabolismo, en un modelo murino de cáncer de páncreas. Inyecciones mensuales de baja dosis ayudaron a preservar músculo y grasa, mejoraron la ingesta de alimentos y el metabolismo, y prolongaron modestamente la supervivencia, sin toxicidad evidente ni signos de activación inmune crónica.
Ataque oncológico preciso y menor autoinmunidad
Para comprobar si la alta fidelidad de copia realmente importa, los investigadores cargaron el vector VPg con un constructo oncolítico complejo, GSDMDENG, diseñado para perforar las mitocondrias de las células tumorales y estimular respuestas inmunitarias específicas contra el tumor. Cuando el mismo constructo se colocó en un saRNA convencional de alfavirus, se acumularon mutaciones tras rondas repetidas de copia y se debilitaron sus funciones selectivas de matar células cancerosas y de activar la inmunidad. En contraste, el sistema VPg preservó la secuencia prevista, produjo una fuerte destrucción de células tumorales y desencadenó respuestas de linfocitos T duraderas que frenaron o evitaron el cáncer de páncreas en modelos murinos. Finalmente, aplicaron el saRNA VPg a otro desafío: la enfermedad crónica injerto contra huésped, donde las células inmunitarias atacan los pulmones tras un trasplante de médula ósea. Un saRNA VPg que codificaba proteína C activada redujo la formación de anticuerpos nocivos, previno la fibrosis pulmonar y mejoró la respiración en ratones, mientras que un constructo comparable basado en alfavirus provocó una mayor inmunidad innata y empeoró los resultados.
Por qué esto importa para los futuros fármacos de ARN
En conjunto, el trabajo describe una plataforma de ARN compacta y “plug-and-play” que combina tres rasgos deseables: se copia con alta fidelidad, está diseñada para minimizar las alarmas inmunitarias y sortea algunos de los cuellos de botella que restringen la traducción del ARNm estándar. Dado que el gen terapéutico se intercambia simplemente en un armazón fijo basado en norovirus, pueden probarse muchas proteínas diferentes —desde hormonas a reguladores de la coagulación o agentes oncolíticos— sobre el mismo chasis. Aunque queda mucho por hacer antes de su uso en humanos, este enfoque de saRNA con VPg sugiere un camino hacia fármacos de ARN que actúen más como infusiones proteicas estables: baja dosis, mayor duración y diseñados para operar incluso en tejidos enfermos donde los mensajes de ARNm ordinarios no pueden leerse con fiabilidad. 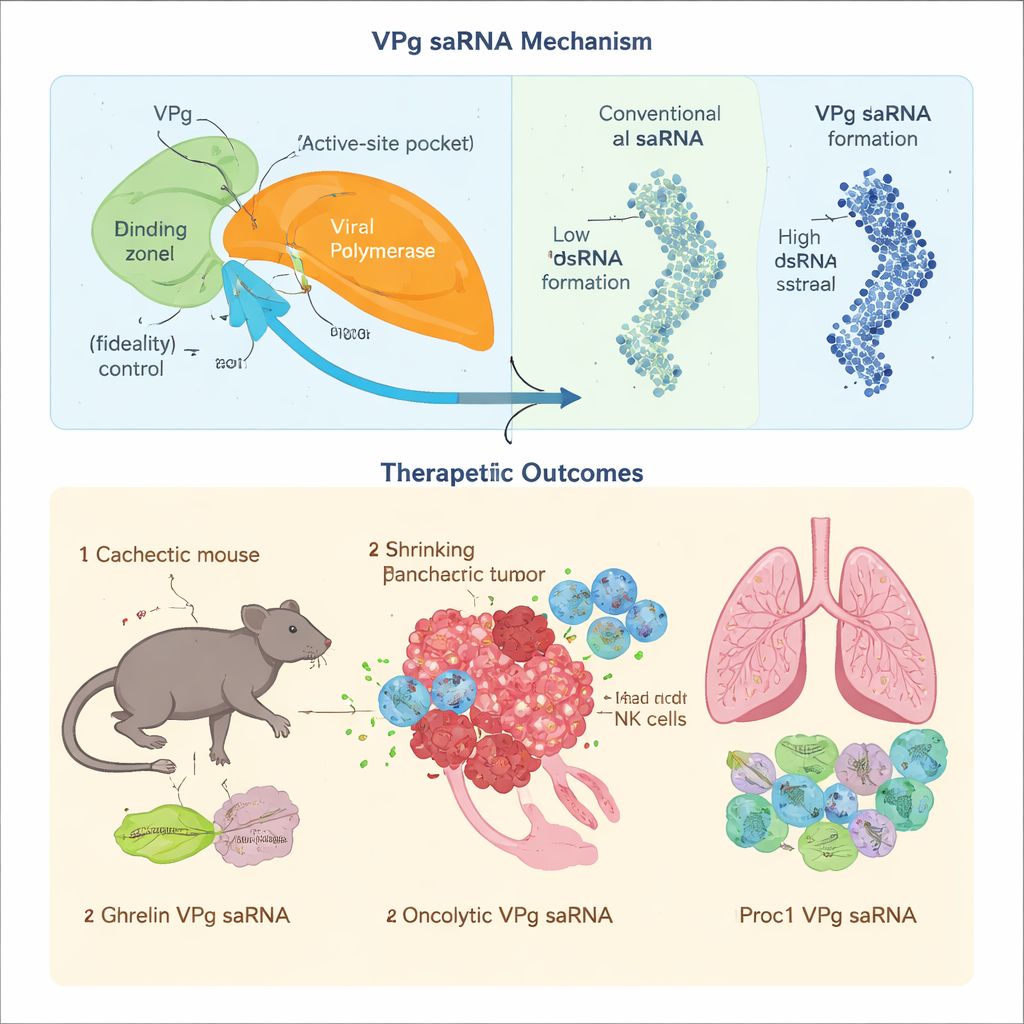
Cita: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Palabras clave: ARN autoamplificante, terapéuticas de ARNm, VPg de norovirus, caquexia asociada al cáncer, enfermedad injerto contra huésped