Clear Sky Science · es
El papel de las repeticiones de baja complejidad en las interacciones ARN–ARN y un marco de aprendizaje profundo para la predicción de dímeros
Secuencias de ARN pegajosas que moldean el comportamiento celular
Dentro de cada célula, las moléculas de ARN se encuentran constantemente entre sí, formando asociaciones fugaces que ayudan a controlar qué genes se activan, cómo se producen las proteínas y cómo se desarrollan las células. Este estudio revela que muchos de estos encuentros ARN–ARN no son aleatorios: están guiados por secuencias cortas, simples y altamente repetitivas que actúan como Velcro molecular. Los investigadores también desarrollan una herramienta de inteligencia artificial capaz de detectar dónde es probable que se formen esos pares de ARN, abriendo nuevas vías para explorar cómo funcionan las células en la salud y la enfermedad.
Repeticiones simples con efectos potentes
El ARN suele describirse como un mensajero que lleva información genética del ADN a las proteínas, pero también funciona como andamiaje, regulador y guía. Gran parte de esta actividad depende de que dos hebras de ARN se unan entre sí. Al combinar datos de varios estudios experimentales extensos en células humanas y de ratón, los autores muestran que las regiones de ARN que participan en dicho apareamiento están fuertemente enriquecidas en lo que denominan repeticiones de baja complejidad. Se trata de tramos formados por motivos cortos —como series de bases G y C— repetidos una y otra vez. En lugar de ser “basura” genómica, estos fragmentos repetitivos resultan ser sitios de acoplamiento preferentes donde un ARN puede adherirse a muchos otros, formando centros de interacción densos a lo largo del transcriptoma. 
Hubs de ARN para el desarrollo y la regulación
Cuando el equipo examinó qué genes contienen estos sitios de contacto ricos en repeticiones, surgió un patrón llamativo: muchos de ellos codifican proteínas que controlan el desarrollo y la identidad celular, como factores de transcripción. Incluso en líneas celulares cancerígenas que no están en proceso activo de diferenciación, los ARNs vinculados a programas de desarrollo participaron de manera destacada en contactos basados en repeticiones. Los autores también analizaron concretamente ciertos ARN largos no codificantes (lncRNAs), que no codifican proteínas pero a menudo las regulan. Por ejemplo, los blancos del lncRNA TINCR y de otro lncRNA importante para la formación de motoneuronas, Lhx1os, mostraron un exceso de repeticiones complementarias. En estos casos, las repeticiones simples en el lncRNA se emparejan con repeticiones complementarias en sus ARNs asociados, permitiendo emparejamientos estables que pueden ayudar a ajustar los niveles o la traducción de genes clave del desarrollo.
Dónde se involucran proteínas y enzimas de edición
Estos contactos impulsados por repeticiones rara vez actúan solos. Los autores superpusieron mapas de unión de proteínas sobre sus datos de interacción y encontraron que muchos sitios de contacto portadores de repeticiones también son reconocidos por proteínas que se unen al ARN implicadas en el control de la traducción, la degradación del ARN y la formación de gránulos citoplasmáticos como los cuerpos P y los gránulos de estrés. Una proteína en particular, STAU1, que puede desencadenar la destrucción de sus ARNs diana, se une con frecuencia a dímeros formados mediante repeticiones de baja complejidad. La reducción de STAU1 condujo a niveles más altos de los ARNs implicados en estos dímeros, especialmente los que contienen repeticiones, lo que sugiere que el apareamiento mediado por repeticiones puede marcar transcritos para su degradación controlada. Las mismas regiones ricas en repeticiones también atraen enzimas de edición del ARN como ADAR1, que modifican químicamente bases específicas dentro de ARN de doble cadena, lo que insinúa que las repeticiones de baja complejidad ayudan a posicionar sitios de edición que afinan el comportamiento del ARN.
Enseñando a una red neuronal a leer contactos de ARN
Los programas informáticos estándar intentan predecir la unión ARN–ARN principalmente en función de la estabilidad termodinámica—cuánta energía se necesitaría para formar o romper un dímero. Aunque útiles, estos modelos a menudo no detectan interacciones reales observadas en células, especialmente entre ARNs largos. Para ir más allá de las reglas energéticas simples, los autores entrenaron un modelo de aprendizaje profundo llamado RIME que usa incrustaciones al estilo de modelos de lenguaje: representaciones numéricas de secuencias de ARN que codifican patrones aprendidos a partir de enormes colecciones de datos de ácidos nucleicos. A RIME se le muestran pares de segmentos de ARN y aprende a clasificar si interactúan, usando muchos apareamientos reales obtenidos por experimentos de entrecruzamiento basados en psoraleno como ejemplos positivos y pares no interaccionantes cuidadosamente construidos como negativos. 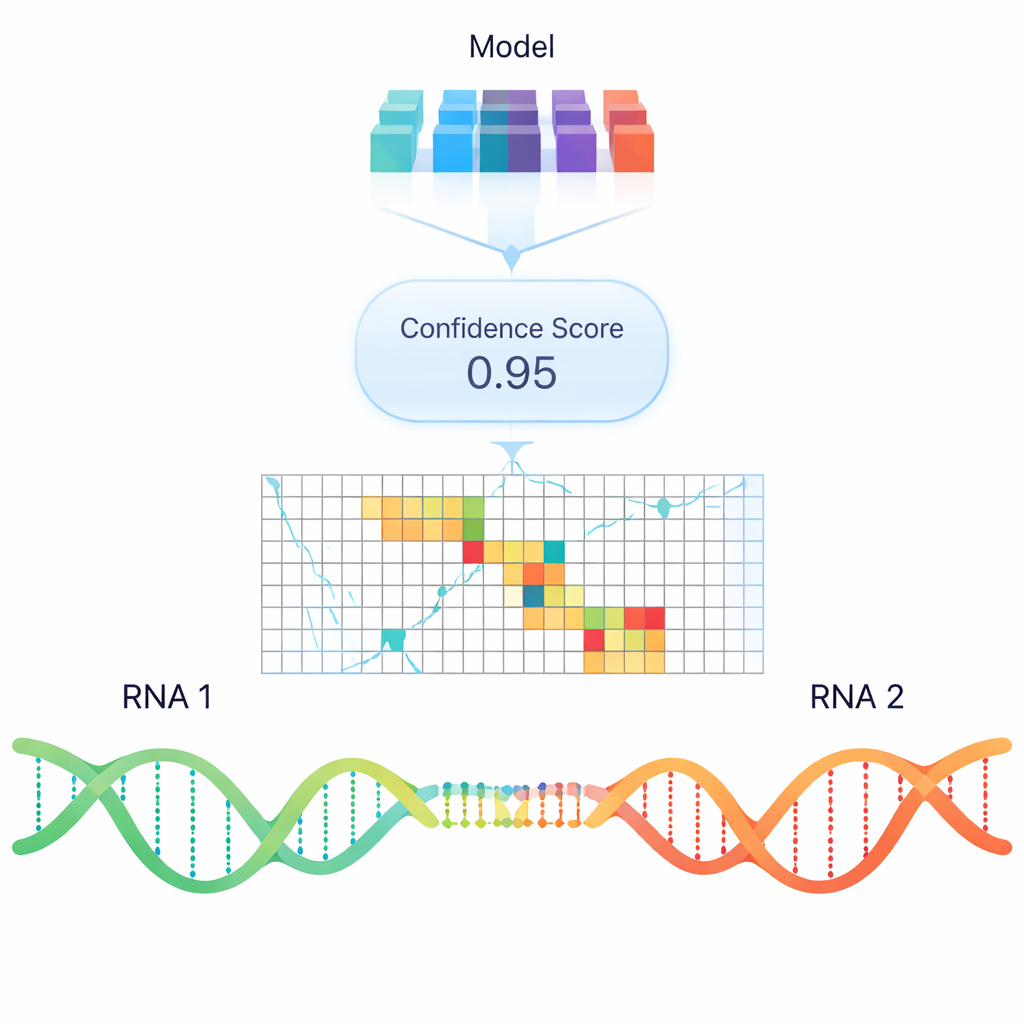
Predicciones más inteligentes y nuevas pistas biológicas
Al compararlo con herramientas líderes basadas en termodinámica y con otro método de red neuronal, RIME rinde consistentemente mejor al distinguir contactos ARN–ARN verdaderos de señuelos, especialmente para interacciones experimentales de alta confianza. No solo predice si dos ARNs se emparejarán, sino que además suele señalar las regiones exactas implicadas, y aprende de forma natural que las repeticiones de baja complejidad son predictores fuertes de contacto. De forma notable, el mismo modelo, entrenado únicamente en interacciones entre ARNs distintos, también funciona bien para predecir el apareamiento interno dentro de una sola molécula de ARN, alineándose tanto con experimentos estructurales como con algoritmos clásicos de plegamiento. Para reguladores no codificantes como TINCR, NORAD y SMaRT, RIME redescubre con éxito sitios funcionales conocidos y sugiere regiones candidatas adicionales.
Por qué importa esto
Para un lector general, el mensaje clave es que tramos cortos y repetitivos del ARN —antes fáciles de descartar como ruido sin valor— actúan como puntos centrales de conexión en el diagrama de cableado del ARN celular. Ayudan a reunir ARNs, atraen proteínas reguladoras y enzimas de edición, y se emplean de forma intensiva en vías que controlan cómo se desarrollan las células y responden al estrés. El nuevo modelo RIME ofrece a los investigadores una herramienta potente para explorar genomas en busca de estas asociaciones ARN–ARN, incluidas aquellas que pueden fallar en enfermedades neurológicas y otras condicionadas por expansiones de repeticiones. En esencia, este trabajo muestra que entender —y predecir— cómo se adhieren juntas las repeticiones simples de ARN puede revelar capas ocultas de regulación génica.
Cita: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Palabras clave: Interacciones ARN–ARN, repeticiones de baja complejidad, ARN largo no codificante, aprendizaje profundo, regulación génica