Clear Sky Science · es
Depleción guiada por firmas transcriptómicas de células alveolares epiteliales intermedias mejora la fibrosis pulmonar en ratones
Por qué importan los pulmones con cicatrices
La fibrosis pulmonar es una enfermedad pulmonar grave en la que los delicados sacos de aire se transforman progresivamente en tejido cicatricial rígido, haciendo que cada respiración sea un esfuerzo. Los médicos saben que este tejido cicatricial comienza cuando los procesos normales de reparación se desvían, pero no estaba claro qué células específicas son las culpables ni cómo eliminarlas sin dañar el tejido pulmonar sano. Este estudio explora una nueva forma de “leer” los mensajes moleculares dentro de las células pulmonares, usar esa información para identificar células transicionales perjudiciales y eliminarlas selectivamente para reducir la cicatrización en ratones.
Células atrapadas en el acto de una reparación defectuosa
Tras una lesión pulmonar, células especiales productoras de surfactante llamadas células tipo II normalmente se multiplican y luego maduran en delgadas células tipo I que recubren los sacos de aire y permiten que el oxígeno pase a la sangre. En la fibrosis, muchas de estas células quedan atascadas en un estado intermedio o transicional en lugar de completar ese recorrido. Estudios previos de secuenciación de ARN unicelular habían hallado estas células intermedias en ratones y humanos, pero no quedaba claro si eran meros observadores o impulsores clave de la enfermedad. Los autores se centraron en un tipo transicional de ratón llamado intermedios de diferenciación alveolar Krt8+ y en sus homólogos humanos conocidos como células basaloides aberrantes, que aparecen en gran número en pulmones cicatrizados.
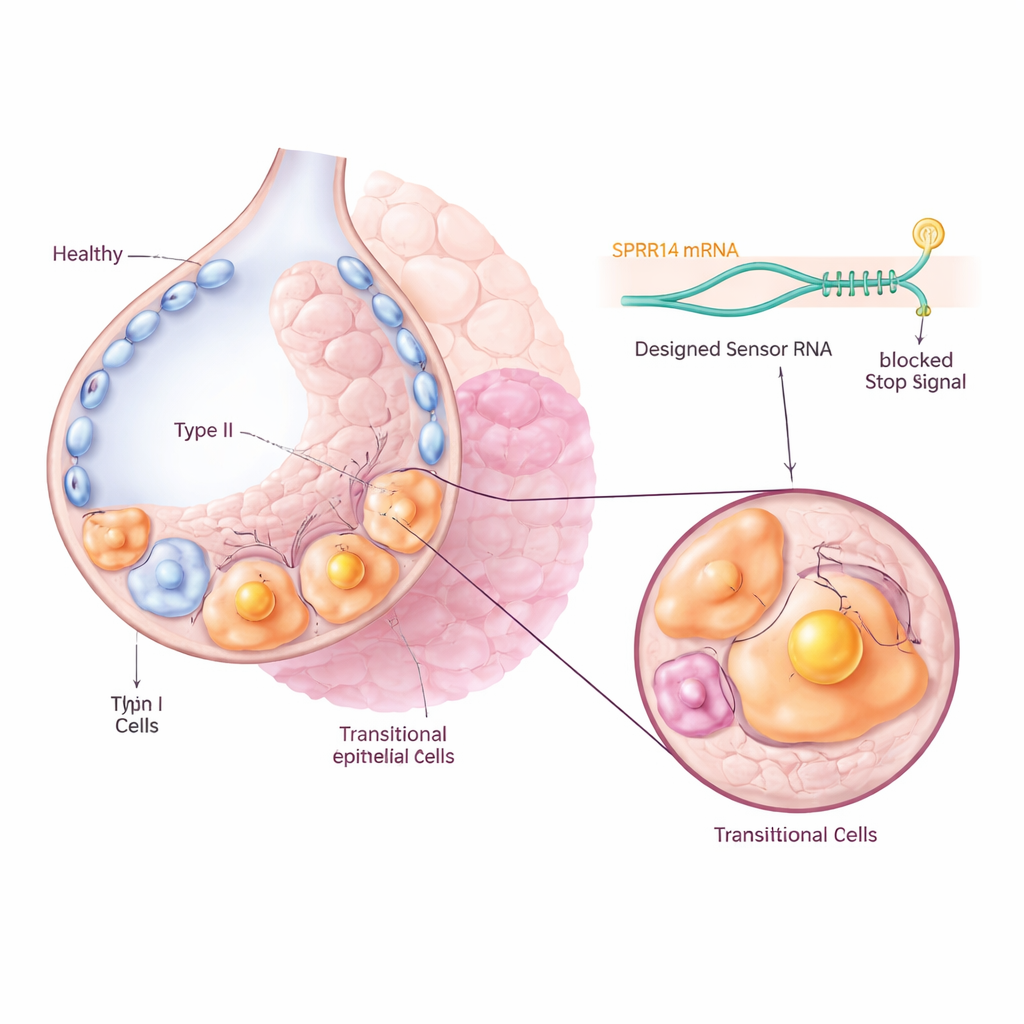
Encontrar una etiqueta molecular única
Para dirigirse a estas células problemáticas sin afectar a sus vecinas sanas, el equipo primero buscó en grandes conjuntos de datos de expresión génica un marcador que estuviera activado de forma intensa y específica en la población transicional. Identificaron una molécula llamada SPRR1A como una “etiqueta” destacada: estaba muy enriquecida en las células intermedias Krt8+ en pulmones fibróticos de ratón, y en las células basaloides aberrantes KRT5-/KRT17+ de pacientes con fibrosis pulmonar idiopática, pero ausente en gran medida en las células pulmonares normales. La microscopía de tejido pulmonar tanto de ratón como humano confirmó que SPRR1A aparecía principalmente en regiones lesionadas y remodeladas y no en los sacos aéreos sanos, lo que sugiere que podría servir como un identificador preciso de las células culpables.
Programar células con un sensor de ARN
Los investigadores utilizaron entonces una tecnología desarrollada recientemente llamada CellREADR, que actúa como un sensor molecular interno. Diseñaron secuencias de ARN cortas que pueden aparearse con el ARN SPRR1A dentro de una célula. Cuando el sensor detecta SPRR1A, desencadena la producción de una proteína “efectora” adjunta, como una etiqueta fluorescente o un receptor que hace a la célula sensible a un fármaco. En ratones, se emplearon virus para entregar estos constructos sensor–efector a las células pulmonares. Solo las células que producían activamente SPRR1A encendieron la señal fluorescente, lo que permitió al equipo rastrear y aislar las células transicionales directamente de pulmones fibróticos. La secuenciación unicelular mostró que las células marcadas coincidían estrechamente con la firma génica transicional conocida, confirmando que el sensor de ARN estaba localizando con precisión la población prevista.
Apagar los intermediarios perjudiciales
A continuación, el efector se cambió de una proteína fluorescente inocua al receptor de la toxina diftérica, de modo que las células positivas para SPRR1A pudieran ser eliminadas selectivamente administrando toxina diftérica. Al sincronizar el tratamiento con la abundancia máxima de células transicionales tras una lesión pulmonar química, los autores lograron eliminar aproximadamente un tercio de esta población. Esta depleción dirigida condujo a una reducción notable de la cicatrización pulmonar: hubo menor acumulación de colágeno, niveles más bajos de proteínas fibróticas y estructuras de los sacos aéreos con aspecto más normal. Análisis detallados mostraron que la mayoría de las células positivas para SPRR1A presentaban signos de un estado de estrés similar al envejecimiento, con un pequeño subconjunto capaz de alta proliferación, lo que sugiere que estos intermediarios tanto fallan en reparar correctamente el tejido como contribuyen a sostener el proceso fibrótico.
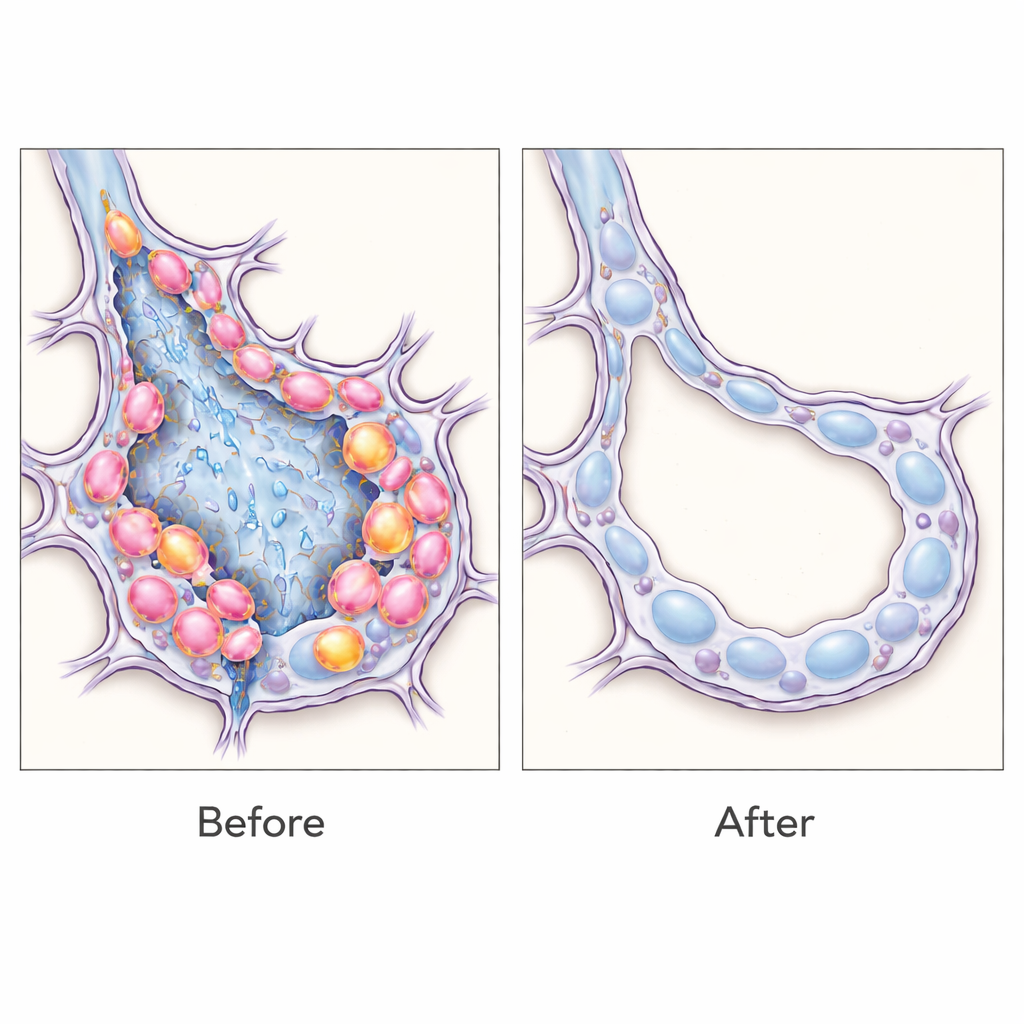
Qué implica esto para tratamientos futuros
Estos hallazgos sostienen que las células epiteliales transicionales no son solo marcadores sino impulsores activos de la fibrosis pulmonar, y que su eliminación selectiva puede inclinar la balanza hacia una arquitectura pulmonar más saludable en ratones. De forma más amplia, el trabajo demuestra una estrategia flexible: al “leer” firmas de ARN específicas de células, los investigadores pueden etiquetar, estudiar e incluso eliminar poblaciones celulares definidas de manera muy concreta en tejido vivo sin crear líneas animales personalizadas cada vez. Si bien queda mucho por hacer antes de que estas herramientas de detección de ARN puedan adaptarse con seguridad a humanos, este enfoque abre un camino hacia terapias de precisión que apunten a los tipos celulares exactos que descarrilan la reparación en la cicatrización pulmonar crónica y, potencialmente, en otras enfermedades fibróticas.
Cita: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Palabras clave: fibrosis pulmonar, células epiteliales alveolares, secuenciación de ARN unicelular, tecnología de detección de ARN, senescencia celular