Clear Sky Science · es
Atlas de núcleos individuales de la amígdala central revela dinámicas de cromatina y transcripción génica en el trastorno por consumo de alcohol
Por qué esta investigación importa en la vida cotidiana
El trastorno por consumo de alcohol (TCA) afecta a millones de personas y a sus familias, pero seguimos sabiendo sorprendentemente poco sobre lo que el consumo excesivo a largo plazo hace al cerebro humano a nivel de células individuales. Este estudio se centra en una región pequeña pero crítica —la amígdala central, un núcleo para el miedo, el estrés y la motivación— para cartografiar cómo el alcohol remodela las células cerebrales y sus sistemas de control genético. Al combinar la vanguardia de la secuenciación “de una sola célula” con estudios genéticos sobre el riesgo de adicción, los autores empiezan a explicar por qué algunas personas son más vulnerables al TCA y cómo el alcohol deja cicatrices moleculares duraderas en el cerebro.
Observando de cerca un diminuto centro cerebral
La amígdala central es una estación de salida clave en la red emocional y del estrés del cerebro y se vincula fuertemente con el alivio de la ansiedad, el deseo y el consumo compulsivo de alcohol. En este trabajo, los investigadores analizaron unos 175.000 núcleos celulares individuales obtenidos postmortem de la amígdala central de 50 personas —22 con historial de trastorno por consumo de alcohol y 28 sin TCA. Usando una tecnología que lee tanto la actividad génica (ARN) como la accesibilidad de la cromatina (qué tan “abierta” o “cerrada” está la ADN) en la misma célula, construyeron un atlas detallado de todos los principales tipos celulares de esta región, incluyendo varios tipos de neuronas y células de soporte como astrocitos y microglía. Encontraron que las neuronas inhibidoras —que atenúan o esculpen la actividad cerebral— son especialmente abundantes en la amígdala central y parecen particularmente afectadas en personas con TCA. 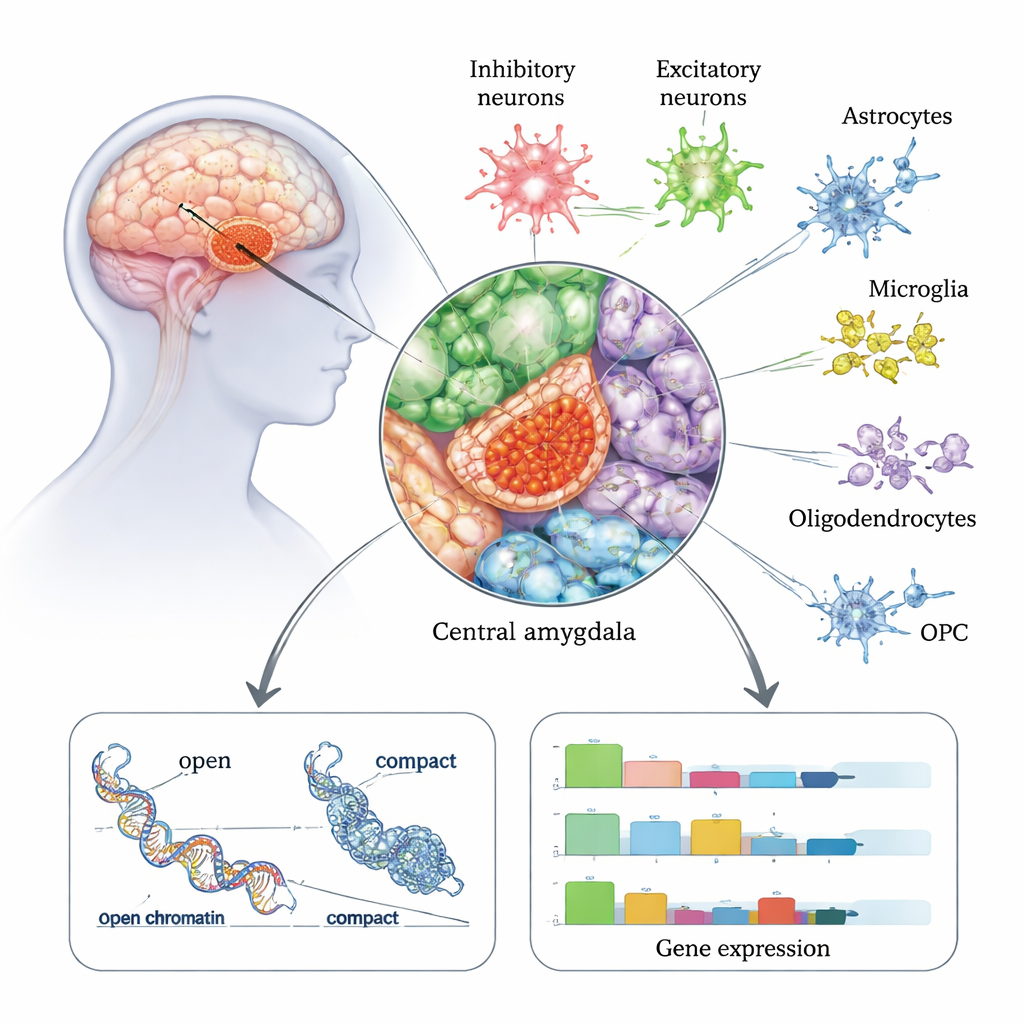
¿Qué células y genes cambian en el trastorno por consumo de alcohol?
El equipo comparó sistemáticamente la actividad génica en personas con y sin TCA, tipo celular por tipo celular. Descubrieron más de 1.800 genes cuya actividad se alteró en poblaciones celulares específicas, con los mayores cambios en neuronas inhibidoras, seguidas por neuronas excitadoras y astrocitos. Un subtipo de neurona inhibidora marcado por el péptido proencefalina (PENK) mostró cambios especialmente intensos. Muchos de los genes afectados participan en la comunicación entre células cerebrales, especialmente en el equilibrio entre la señal excitadora glutamato y la señal inhibidora GABA. Por ejemplo, el gen GABRA2, que contribuye a formar un tipo importante de receptor GABA, estaba aumentado en ciertas neuronas inhibidoras, mientras que GRM8, un receptor de glutamato, y NCAM1, una molécula de adhesión celular importante para las sinapsis, cambiaron en direcciones opuestas según los subtipos neuronales. Estos patrones sugieren que el ajuste fino de la excitación y la inhibición en la amígdala central está perturbado en el TCA.
Los interruptores de control del cerebro: cromatina y elementos reguladores
Los genes no actúan solos; están controlados por tramos de ADN que funcionan como interruptores y reguladores de intensidad. Al examinar la cromatina —la forma en que se empaqueta el ADN—, los investigadores identificaron más de medio millón de elementos reguladores candidatos y los vincularon a genes cercanos de manera específica por tipo celular. Casi la mitad de estos elementos eran únicos de un solo tipo celular, lo que subraya cuán especializados son los distintos tipos de células cerebrales. Muchos de los elementos reguladores que cambiaron en el TCA estaban conectados a genes implicados en el manejo del calcio y la señalización del glutamato, como CALN1, un gen ligado a la unión del calcio y altamente activo en neuronas. En las neuronas inhibidoras, CALN1 mostró tanto un aumento de expresión como densos cúmulos de bucles regulatorios, lo que implica que la exposición al alcohol remodela la arquitectura local del ADN que controla este gen. 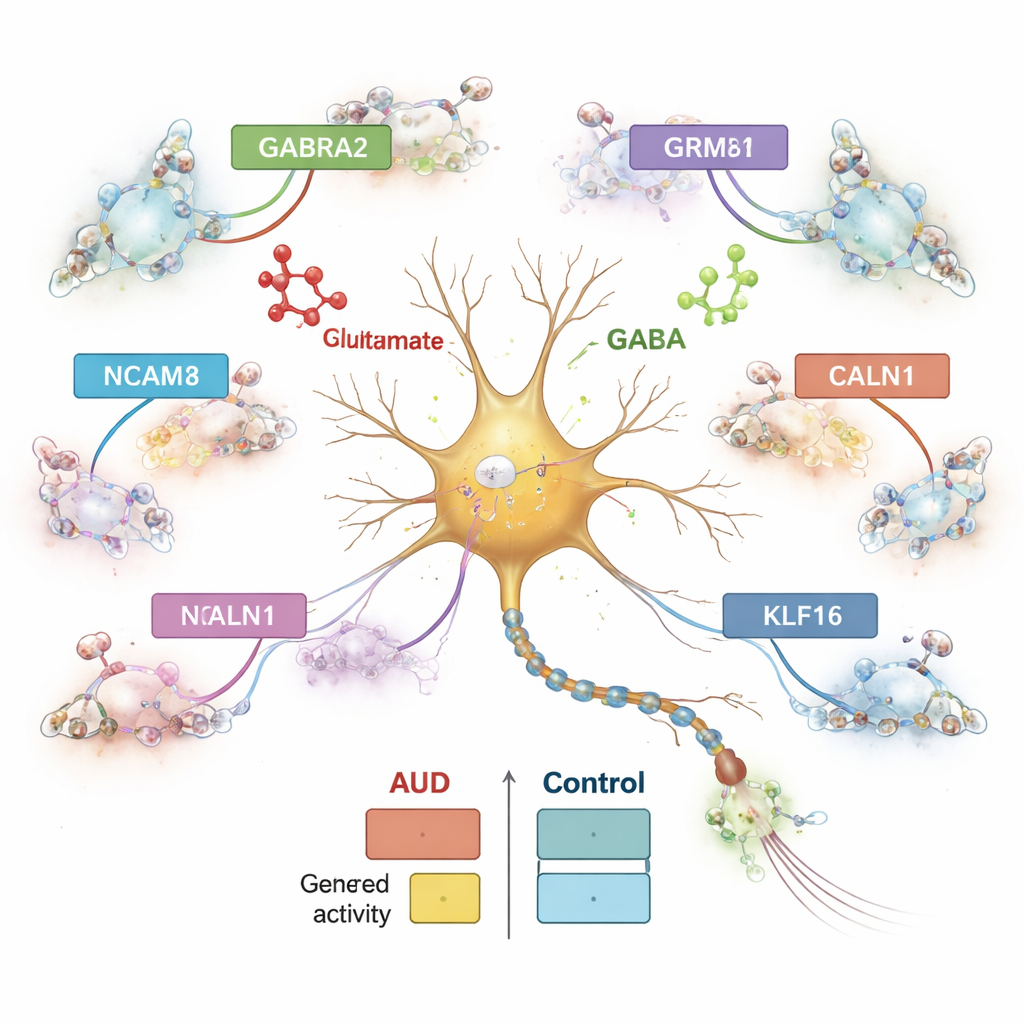
De los genes de riesgo a los cambios reales en el cerebro
Los estudios genéticos han identificado muchas variantes de ADN que aumentan el riesgo de desarrollar problemas con el alcohol, pero dónde y cómo actúan en el cerebro no estaba claro. Al superponer sus mapas de una sola célula con grandes estudios de asociación del genoma completo sobre consumo problemático de alcohol, los autores hallaron que los genes de riesgo están desproporcionadamente activos y desregulados en neuronas de la amígdala central, especialmente en las inhibidoras. Identificaron más de 200 variantes de riesgo probablemente causales ubicadas dentro de elementos reguladores que están accesibles en tipos celulares específicos. Algunas cayeron dentro o cerca de genes ya vinculados a la adicción, como CACNA1C y DRD2, que ayudan a controlar la excitabilidad neuronal y la señalización de dopamina. Otras, incluidas SEMA6D y NF1, surgieron como nuevas candidatas. El equipo también identificó una familia de factores de transcripción llamados factores tipo Kruppel (notablemente KLF16) que parecen coordinar cambios generalizados en genes relacionados con el calcio y el glutamato, y confirmaron partes de esta red reguladora en un modelo murino de exposición aguda al alcohol.
Qué significa esto para entender y tratar el TCA
En términos sencillos, este estudio muestra que el trastorno por consumo de alcohol no es solo un problema cerebral difuso, sino una alteración altamente organizada concentrada en tipos celulares y vías moleculares particulares dentro de un centro emocional crítico. Las neuronas inhibidoras de la amígdala central, junto con astrocitos y otras células de soporte, muestran cambios coordinados en la actividad génica y en los interruptores de ADN que controlan esos genes —especialmente en sistemas que gestionan las señales de glutamato, GABA y calcio. Al conectar estos cambios celulares con variantes de riesgo genético, el trabajo ofrece una hoja de ruta que vincula la vulnerabilidad heredada con eventos moleculares concretos en el cerebro. Con el tiempo, mapas celulares tan específicos podrían guiar el desarrollo de tratamientos más precisos que restauren el equilibrio entre excitación e inhibición, en lugar de actuar de forma general sobre todo el cerebro.
Cita: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Palabras clave: trastorno por consumo de alcohol, amígdala central, genómica de una sola célula, neuronas inhibidoras, regulación génica