Clear Sky Science · es
De la formación del complejo TDP-43/ARN a la agregación de TDP-43 relacionada con la enfermedad mediante un enfoque estructural y celular
Por qué importa esta proteína cerebral
Las enfermedades neurodegenerativas como la esclerosis lateral amiotrófica (ELA) y la demencia frontotemporal suelen presentar acumulaciones de proteínas mal plegadas dentro de las células nerviosas. Uno de los culpables más comunes es una proteína llamada TDP-43, que normalmente ayuda a procesar el ARN —la copia operativa de nuestros genes—. Este estudio plantea una pregunta crucial: ¿qué hace TDP-43 en células sanas y qué falla para convertir a este útil ayudante del ARN en una proteína que forma agregados tóxicos?
Cómo funciona TDP-43 en las células nerviosas sanas
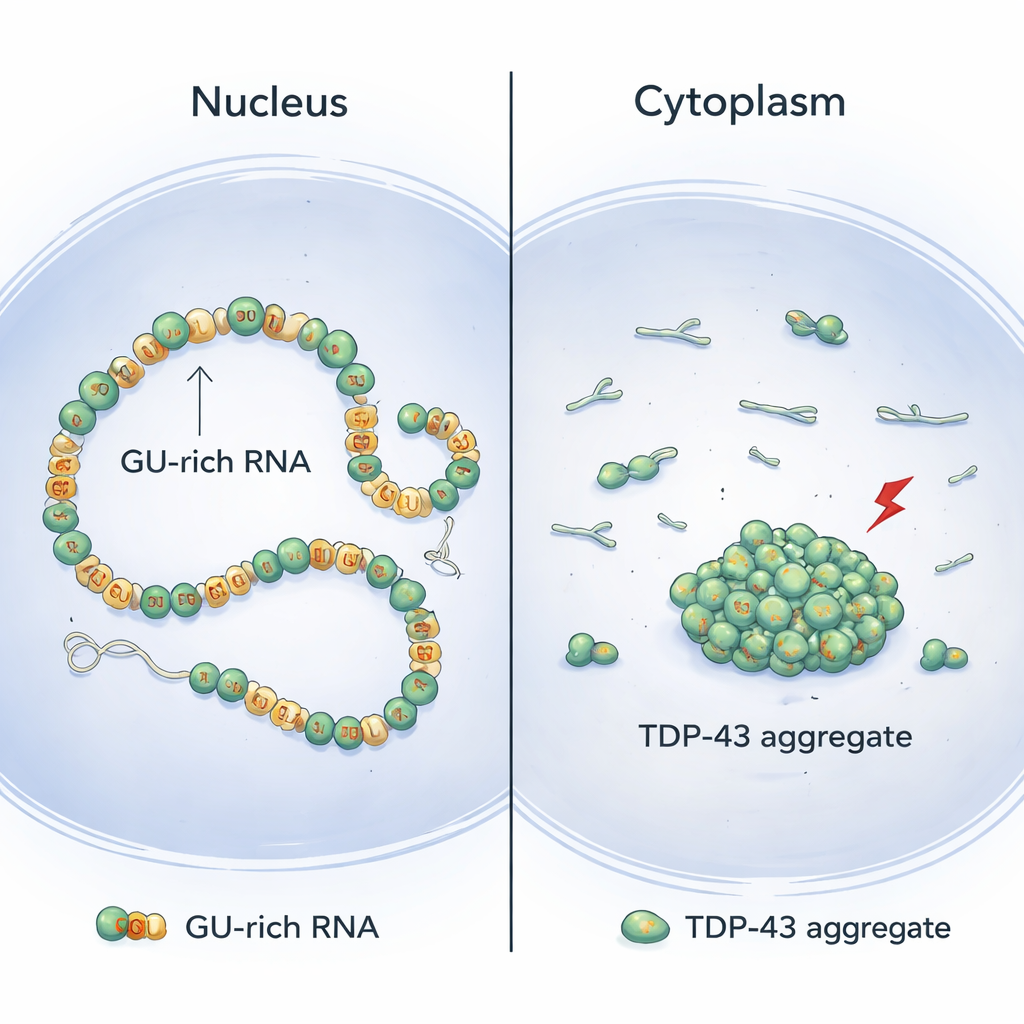
TDP-43 suele localizarse en el núcleo celular, donde se une a tramos largos de ARN ricos en repeticiones de los nucleótidos “GU”. Mediante una combinación de biología estructural y experimentos celulares, los autores muestran que las moléculas de TDP-43 se alinean de forma cooperativa a lo largo de estas regiones ricas en GU, formando cadenas continuas y homogéneas sobre el ARN. Dispuestas así, el extremo anterior de la proteína —su dominio N-terminal— permanece físicamente separado entre moléculas vecinas. Como resultado, esos segmentos N-terminales quedan disponibles para conectar secciones distantes ricas en GU del mismo ARN, provocando bucles y compactación suave de intrones largos (los tramos no codificantes dentro de los genes) sin formar agregados.
Una lucha interna integrada dentro de la proteína
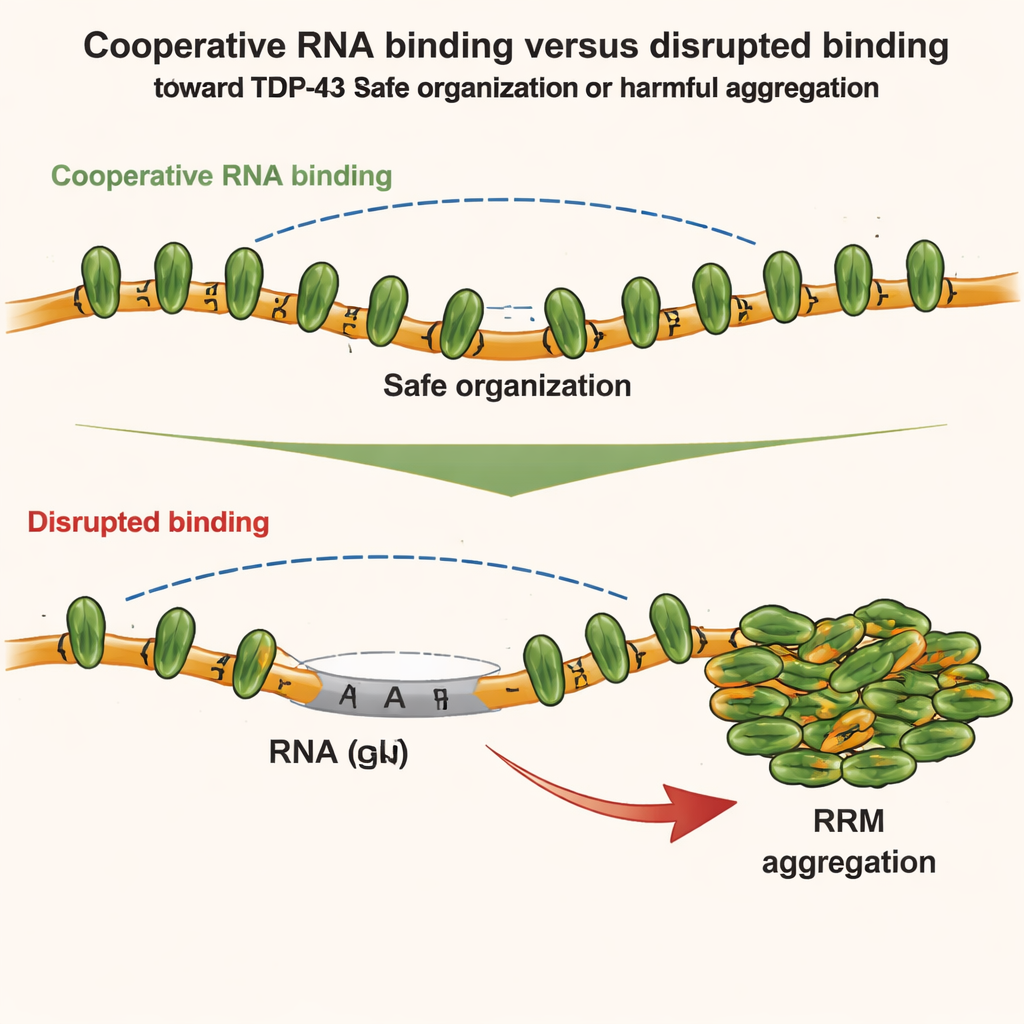
El equipo investigó luego cómo distintas partes de TDP-43 compiten o cooperan entre sí. Se centraron en dos regiones: el dominio N-terminal, que puede pegarse a otros dominios N-terminales, y los módulos centrales de unión al ARN, que promueven la unión cooperativa a ARN rico en GU. Usando técnicas sensibles como espectroscopía de RMN, calorimetría y dispersión de rayos X a ángulo pequeño, hallaron que cuando TDP-43 se une cooperativamente al ARN, la geometría de la cadena en realidad debilita los contactos directos N-terminal–N-terminal entre moléculas adyacentes. En otras palabras, la unión cooperativa fuerte al ARN mantiene bajo control las interacciones N-terminales locales. Pero cuando esa cooperatividad se rompe —por ejemplo, al insertar tramos que no son GU en el ARN o al mutar TDP-43—, las regiones N-terminales de proteínas vecinas se acercan y pueden unirse entre sí.
De la compactación útil al apelmazamiento dañino
Estas ideas estructurales se probaron en células vivas. Los autores emplearon sistemas celulares diseñados para seguir cómo distintos mutantes de TDP-43 se mezclan o se separan dentro de compartimentos artificiales ricos en ARN. Encontraron que tanto la unión cooperativa al ARN como las interacciones N-terminales contribuyen a organizar a TDP-43 en ensamblajes de orden superior, pero de formas diferentes. La unión cooperativa organiza las proteínas a lo largo del ARN rico en GU, mientras que los contactos N-terminales enlazan conjuntos distantes. Sin embargo, bajo estrés oxidativo leve la situación cambia. Un agente químico estresante (arseniato) provoca modificaciones químicas específicas —acetilación— en los motivos centrales de unión al ARN, haciéndolos proclives a adherirse. Si la unión cooperativa al ARN está intacta, TDP-43 permanece mayormente soluble. Si la cooperatividad se debilita, los enlaces N-terminales entre moléculas vecinas actúan como un andamiaje que aproxima los núcleos acetilados, favoreciendo la agregación irreversible.
Por qué TDP-43 se apelmaza más en el citoplasma
El modelo que surge de este trabajo ayuda a explicar por qué los agregados de TDP-43 se encuentran con frecuencia en el citoplasma de neuronas enfermas en lugar de en el núcleo. En el núcleo son comunes los intrones largos con muchas repeticiones GU, lo que favorece una unión continua y cooperativa que mantiene bajas las interacciones N-terminales riesgosas entre vecinos y permite en su lugar un bucleado seguro a larga distancia. En el citoplasma, en cambio, los ARN maduros tienen muchas menos regiones ricas en GU. Esto hace que la unión de TDP-43 sea más parcheada y menos cooperativa, aumentando las posibilidades de que los dominios N-terminales vecinos interactúen y preparen el terreno para la agregación cuando se producen cambios químicos inducidos por el estrés. Apoyando esta visión, la provisión artificial de intrones extra ricos en GU en el núcleo redujo la agregación de TDP-43 bajo estrés.
Qué significa esto para futuras terapias
En pocas palabras, el estudio presenta a TDP-43 como una proteína en equilibrio entre la organización útil del ARN y el apelmazamiento dañino, siendo la unión cooperativa a ARN rico en GU un mecanismo de seguridad. Cuando esa red de seguridad falla —por secuencias de ARN alteradas, mutaciones de la proteína o estrés celular—, los mismos dominios que normalmente compactan tramos largos de ARN pueden impulsar la formación de agregados tóxicos. Para el público general, la conclusión clave es que mantener el tipo correcto de interacciones entre TDP-43 y el ARN podría ser una estrategia prometedora para prevenir o ralentizar la agregación proteica observada en la ELA y en enfermedades cerebrales relacionadas.
Cita: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Palabras clave: Agregación de TDP-43, Proteínas de unión a ARN, ELA, interacciones proteína–ARN, neurodegeneración