Clear Sky Science · es
Ingeniería de ligandos con precisión atómica en nanopartículas de oro mediante transferencia de masa entre fases
Por qué las partículas diminutas de oro importan para la salud
La imagen médica depende cada vez más de nanopartículas: partículas diminutas miles de veces más pequeñas que un cabello humano, que permiten iluminar órganos y tumores en lo profundo del cuerpo. Este estudio muestra cómo los científicos pueden afinar ahora el recubrimiento exterior de partículas de oro ultrasmall casi átomo por átomo, de modo que el mismo núcleo luminoso pueda dirigirse hacia distintos órganos, en particular desplazándose del hígado y el bazo hacia los riñones. Ese control podría ayudar a diseñar agentes de imagen y transportadores de fármacos más seguros que vayan exactamente donde los médicos los necesitan y salgan del cuerpo de forma más limpia.
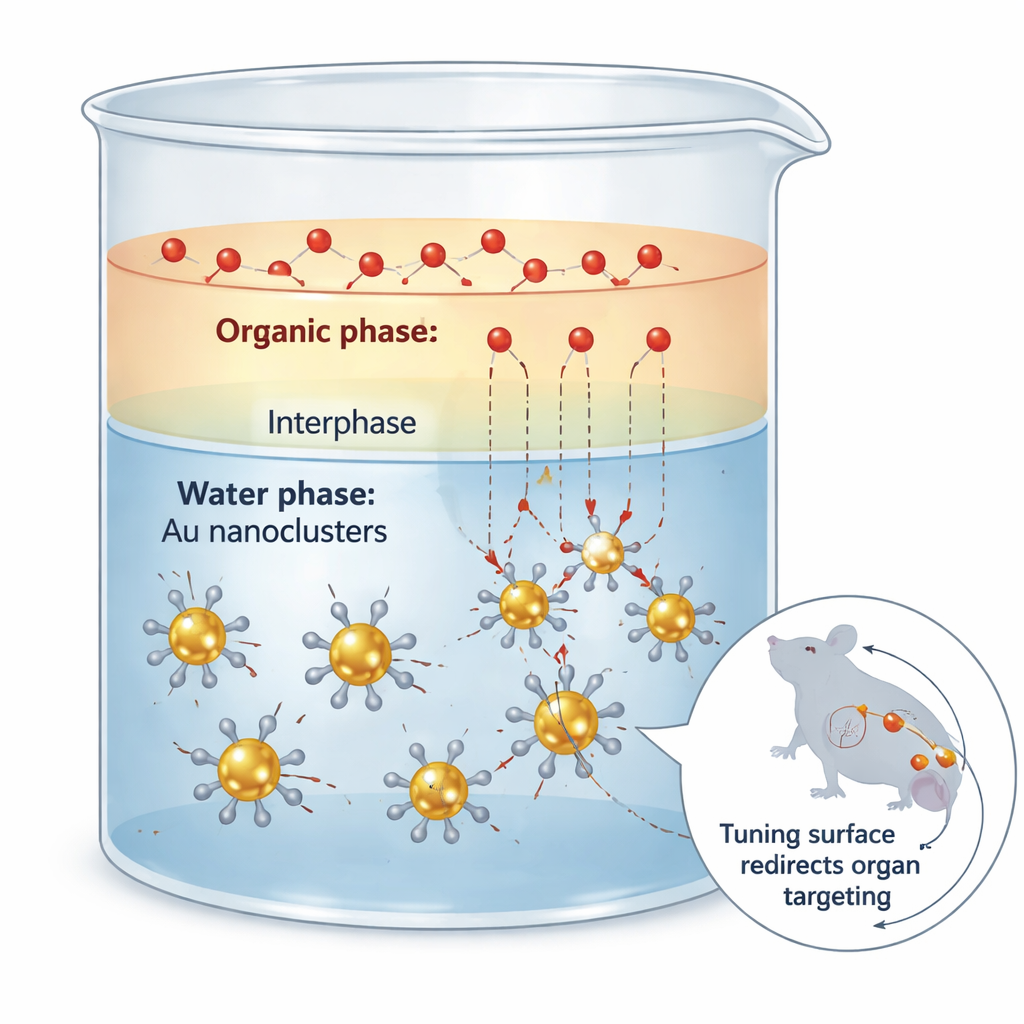
El reto de vestir a los diminutos cúmulos de oro
Los nanocúmulos de oro son partículas de oro ultrasmall que se comportan más como moléculas grandes que como granos metálicos. Pueden emitir luz en la ventana del infrarrojo cercano II, que penetra profundamente en el tejido y proporciona imágenes nítidas con bajo fondo. Sin embargo, casi todo acerca de cómo se comportan estos cúmulos en el cuerpo—dónde viajan, cuánto tiempo circulan y cómo se eliminan—depende no del oro en sí, sino de los ligandos orgánicos, o moléculas de “capa”, adheridos a su superficie. Las maneras tradicionales de cambiar esta capa suelen funcionar como una cirugía burda: la reacción va demasiado rápido, el recubrimiento queda desigual y el núcleo de oro puede ser parcialmente corroído, arruinando tanto la estructura como las propiedades ópticas.
Frenando el tráfico entre dos líquidos
Los investigadores abordaron este problema explotando una idea física sencilla: la resistencia al transporte de masa en la frontera entre dos líquidos que no se mezclan completamente. Colocaron los cúmulos de oro en agua y los ligandos entrantes a base de azufre en un disolvente orgánico como el acetato de etilo. En la delgada región donde los dos líquidos se mezclan parcialmente, los ligandos difunden lentamente hacia los cúmulos y se intercambian con la capa original. Mediciones cinéticas cuidadosas mostraron que el indeseado “etching” (corrosión) del núcleo de oro es extremadamente sensible a la concentración de ligando, mientras que el intercambio deseado lo es mucho menos. Al usar el sistema bifásico para mantener niveles bajos pero continuamente repuestos de ligando libre, el equipo suprimió la corrosión aproximadamente sesenta veces mientras preservaba la mayor parte de la tasa útil de intercambio.
Construyendo un kit molecular preciso
Con este método asistido por la interfase, los autores pudieron reemplazar ligandos superficiales en un cúmulo modelo de oro, Au25, de manera altamente controlada. Partieron de cúmulos protegidos por un ligando ácido sulfónico con carga negativa y lo intercambiaron por una variedad de nuevos tioles que llevaban ácidos carboxílicos, aminas, grupos hidroxilo, nitro y anillos aromáticos hidrofóbicos. La espectrometría de masas reveló mezclas limpias y bien definidas, como cúmulos Au25 que portaban números específicos de cada tipo de ligando, en lugar de distribuciones amplias y desordenadas. El método también funcionó para otros tamaños de cúmulos y familias de ligandos, lo que sugiere que es una estrategia general para diseñar nanocúmulos de oro robustos y a medida para distintas aplicaciones.
Guiando nanopartículas del hígado a los riñones
La prueba más llamativa de esta precisión provino de experimentos de imagen in vivo en ratones. Al introducir gradualmente un ligando con carga positiva, p-aminotiofenol, en una capa que de otro modo era negativa, el equipo creó una serie de cúmulos cuya carga superficial global pasó de fuertemente negativa a casi zwitteriónica (grupos positivos y negativos equilibrados). Todas las versiones emitían luz de forma similar en pruebas de laboratorio, pero su biodistribución en ratones difería de forma drástica. Los cúmulos puramente negativos se acumulaban principalmente en el hígado y el bazo. A medida que se añadieron más ligandos positivos, se observó menos señal en estos órganos y más en los riñones y la vejiga, lo que indica una mayor eliminación renal. Cuando se usó un ligando neutro con grupo hidroxilo en lugar de la amina, este desplazamiento no ocurrió, subrayando el papel especial de las cargas positivas en redirigir las partículas.
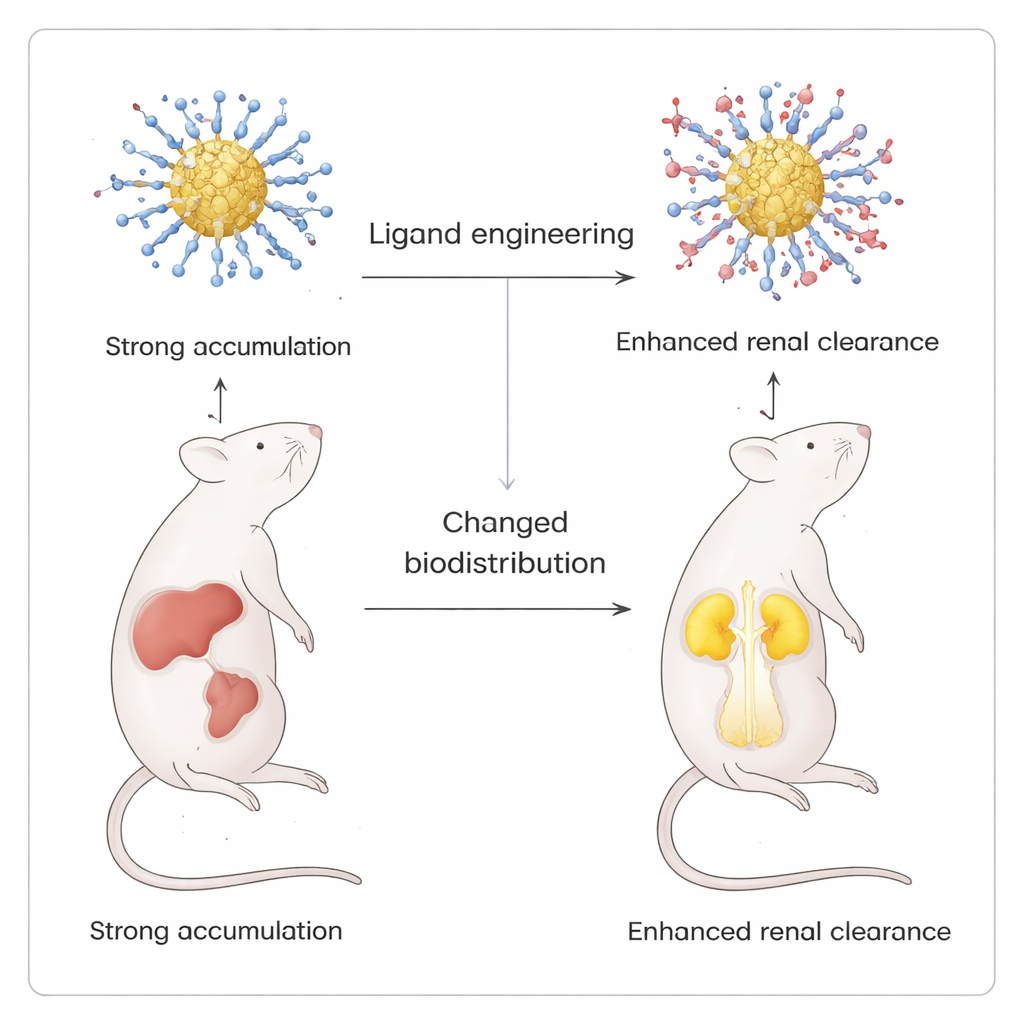
Qué significa esto para las medicinas del futuro
Para el público general, la conclusión clave es que los científicos han encontrado una manera de “vestir” nanocúmulos de oro luminosos con recubrimientos moleculares que pueden ajustarse casi una molécula a la vez, sin dañar la partícula subyacente. Mediante un montaje suave de dos líquidos, pueden controlar tanto la química como el destino final de estas partículas dentro del cuerpo. Este nivel de control hace posible diseñar agentes de imagen y potenciales transportadores de fármacos que iluminan órganos específicos y luego se eliminan por los riñones en lugar de permanecer en el hígado y el bazo, allanando el camino hacia una nanomedicina más segura y predecible.
Cita: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Palabras clave: nanocúmulos de oro, ingeniería de ligandos, bioimagen, nanomedicina, biodistribución