Clear Sky Science · es
La actividad de DOT1L limita la velocidad de elongación de la transcripción y favorece las pausas de la ARN polimerasa II para facilitar la mutagénesis por AID
Cómo nuestras células inmunitarias afinan ediciones de ADN arriesgadas
Nuestro sistema inmunitario crea anticuerpos potentes mutando deliberadamente su propio ADN, una estrategia arriesgada que a veces puede impulsar el cáncer. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿qué controla dónde y con qué eficiencia ocurren estas mutaciones intencionadas? La respuesta se centra en una proteína llamada DOT1L, que ajusta la velocidad de lectura de los genes en las células B y, al hacerlo, ayuda a dirigir la maquinaria de mutación hacia los puntos adecuados.
Activar la mutación para afinar los anticuerpos
Cuando las células B se enfrentan a una infección, mejoran sus anticuerpos de dos maneras. Introducen pequeños cambios en la región que se une al antígeno para mejorar la afinidad y sustituyen la cola del anticuerpo para modificar la respuesta inmune. Ambas mejoras comienzan con una enzima llamada AID, que corta y altera el ADN en genes que se están leyendo activamente. Aunque AID es crucial para una buena inmunidad, también puede afectar a otros genes, creando roturas peligrosas que promueven cánceres sanguíneos. Trabajos previos mostraron que AID prefiere genes muy leídos y regulados por potentes interruptores de ADN llamados superpotenciadores, pero eso no explicaba completamente por qué solo un subconjunto selecto de genes es realmente vulnerable.
Un marcador de cromatina que señala genes sensibles a AID
Los autores se centraron en proteínas que se sitúan cerca de AID en el núcleo. Usando una técnica de etiquetado por proximidad en células humanas, encontraron que AID se agrupa cerca de DOT1L, una enzima que marca un sitio específico en las histonas alrededor de las cuales se enrolla el ADN. Esta marca, un etiquetado químico en la histona H3 en la posición K79, es común en genes activos. En células B de ratón, los genes que AID muta con frecuencia —incluidos los genes de anticuerpos y los objetivos accidentales relacionados con el cáncer— presentan niveles particularmente altos de estas marcas realizadas por DOT1L. Cuando los investigadores desactivaron DOT1L en líneas celulares B o bloquearon su actividad con un fármaco, el «cambio de clase» de anticuerpos disminuyó, al igual que las roturas de ADN inducidas por AID y las fusiones propensas al cáncer entre genes de anticuerpos y el gen de crecimiento cMyc. Es importante que la función catalítica de DOT1L, no solo su presencia, fuera necesaria: versiones mutantes incapaces de colocar la marca en histonas no pudieron restaurar el cambio de clase normal.
Ralentizar al lector génico para dar tiempo a AID
A primera vista, esto resulta desconcertante porque DOT1L se asocia con genes activos, sin embargo su eliminación no apagó simplemente los genes. Usando un método que captura el ARN recién sintetizado, el equipo descubrió que las células B carentes de DOT1L en realidad producían más transcritos nacientes a lo largo de muchos genes marcados por DOT1L, aunque había algo menos de la enzima principal de lectura génica, la ARN polimerasa II, asentada en esos genes. Al combinar esta lectura de ARN naciente con mapas de ocupación de la polimerasa, infirieron que, en condiciones normales, las marcas de histona de DOT1L actúan como suaves resaltos de velocidad. Frenan la polimerasa a medida que avanza por el gen y extienden pausas breves cerca del inicio y dentro del cuerpo de los genes marcados por DOT1L. Sin DOT1L, la polimerasa avanza más rápido y las pausas son más cortas. Dado que AID necesita ventanas breves en las que el ADN queda expuesto y la polimerasa se demora, esta aceleración reduce paradójicamente la capacidad de AID para engancharse y hacer su trabajo, incluso cuando la transcripción global aumenta.
Desacoplar la actividad génica del riesgo de mutación
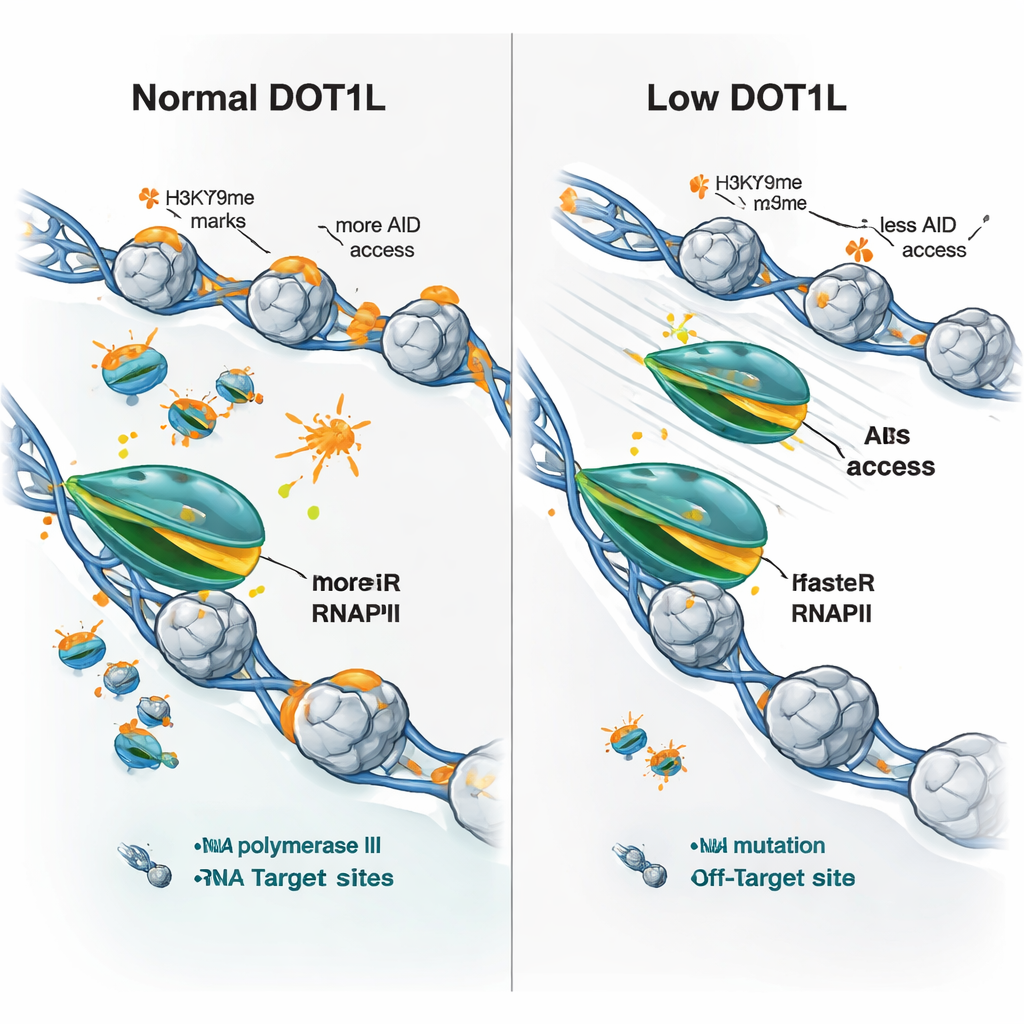
Los investigadores preguntaron entonces si estos cambios de velocidad podían explicar el patrón mixto de expresión génica observado al perder DOT1L: algunos genes suben, otros bajan. Encontraron que prácticamente todos los genes marcados por DOT1L compartían una característica en las células knockout: una elongación más rápida por parte de la ARN polimerasa II. Pero el resultado dependía del estado inicial. Los genes lentos y débilmente expresados tendían a producir más ARN cuando la polimerasa aceleraba, mientras que genes largos y ya muy activos a veces producían menos, probablemente porque un paso demasiado rápido altera el procesamiento o la finalización eficiente. Crucialmente, tanto en los genes de anticuerpos como en los clásicos objetivos accidentales de AID, la pérdida de DOT1L condujo a un movimiento más rápido de la polimerasa, menos evidencias de «atascos» de la polimerasa y una ocupación de AID significativamente reducida, incluso cuando los propios genes no se veían disminuidos.
Por qué esto importa para la inmunidad y el cáncer
En conjunto, el trabajo dibuja a DOT1L como un sutil controlador del tráfico para la maquinaria que lee los genes en las células B. Al instalar marcas de histona específicas, DOT1L ralentiza ligeramente la ARN polimerasa II y prolonga sus pausas, creando un entorno transcripcional donde AID puede involucrarse productivamente con los genes de anticuerpos —y, desafortunadamente, con un conjunto limitado de otros genes vulnerables— para introducir mutaciones. Cuando DOT1L falta o se inhibe, la polimerasa atraviesa más rápido, dejando a AID con menos oportunidades para actuar, lo que atenúa la diversificación de anticuerpos y, al mismo tiempo, reduce el riesgo de ciertos reordenamientos dañinos. Esta visión mecanicista explica por qué la pérdida de DOT1L puede tanto aumentar como disminuir la expresión génica, y vincula el control fino de la velocidad de transcripción directamente con los lugares donde nuestro sistema inmunitario se atreve a reescribir su propio ADN.
Cita: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Palabras clave: diversificación de anticuerpos, enzima AID, DOT1L, transcripción génica, células B