Clear Sky Science · es
Base molecular del antagonismo del receptor humano de vasopresina arginina 1A en forma dimérica
Por qué importa un receptor cerebral hormonal
Las hormonas como la vasopresina y la oxitocina son más conocidas por regular el equilibrio de agua, la tensión arterial, el parto y el vínculo social. Sin embargo, el funcionamiento de sus receptores a nivel atómico ha permanecido en gran parte oculto. Este artículo revela estructuras 3D detalladas de un receptor clave, el receptor humano de vasopresina V1a, que está vinculado al comportamiento social, al estrés y a varios trastornos cerebrales. Comprender su forma y cómo los fármacos lo bloquean podría ayudar a los científicos a diseñar tratamientos mejores para afecciones como el autismo, el trastorno de estrés postraumático y la enfermedad de Huntington.
Un receptor gemelo que modela señales en corazón, riñón y cerebro
El receptor V1a se encuentra en la superficie de muchas células del cuerpo, especialmente en los vasos sanguíneos, los riñones y ciertas regiones del cerebro. Cuando la hormona vasopresina se une a él, el receptor activa vías de señalización internas que controlan la presión arterial, el equilibrio de líquidos y los circuitos cerebrales relacionados con la interacción social, la emoción y el estrés. Estudios genéticos y clínicos han relacionado una señalización anómala de V1a con el trastorno del espectro autista, el TEPT y la enfermedad de Huntington, lo que lo convierte en un objetivo farmacológico atractivo. Varios fármacos bloqueadores de V1a (antagonistas) ya se usan o están en ensayos clínicos, pero hasta ahora nadie había visto el receptor humano V1a con alta resolución, lo que dejaba preguntas fundamentales sobre cómo se ensambla y cómo exactamente estos fármacos lo inactivan. 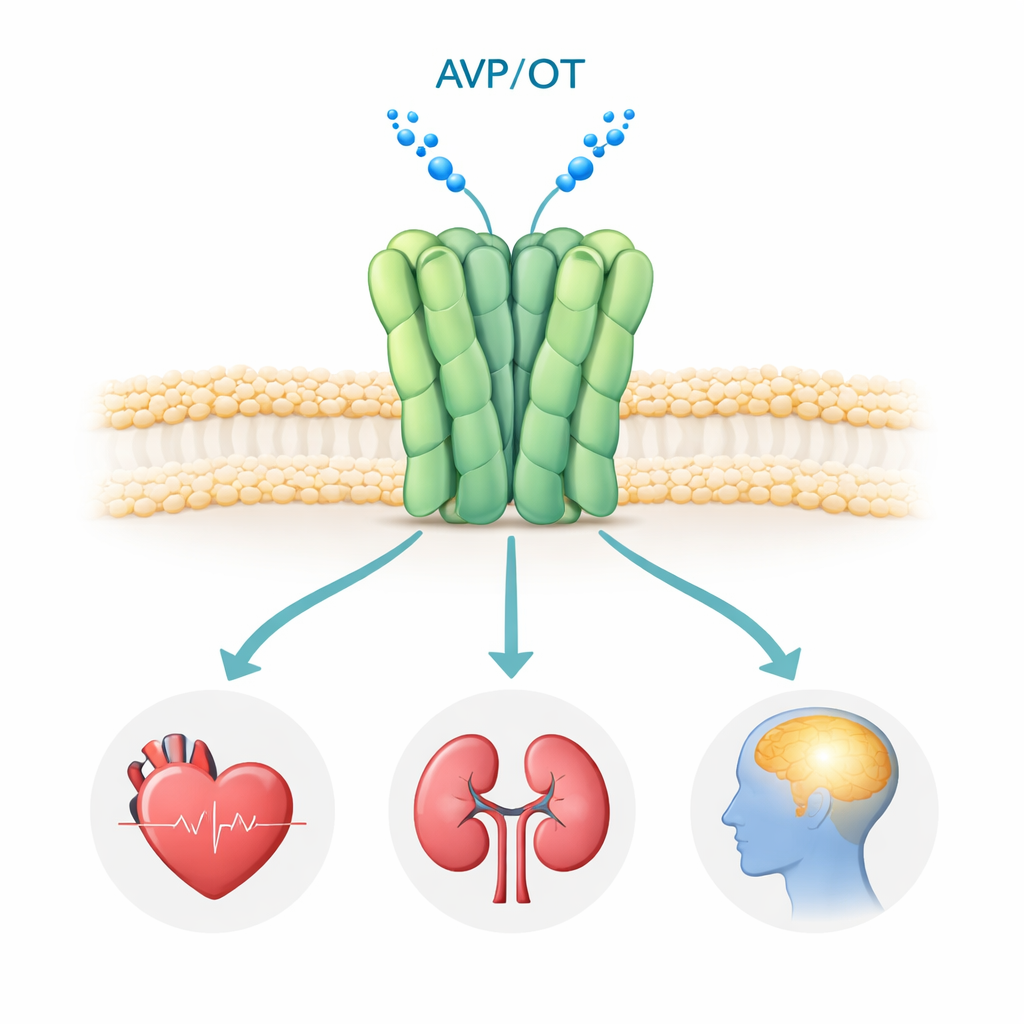
Capturar la estructura del receptor en varios estados unidos a fármacos
Los investigadores utilizaron crio–microscopía electrónica (cryo-EM), una técnica que congela rápidamente las proteínas y las imagen con un haz de electrones, para visualizar el receptor humano V1a. Para estabilizar la proteína, diseñaron una forma ligeramente modificada que aún se une bien a los fármacos y la emparejaron con un fragmento de anticuerpo pequeño (un nanocuerpo) para facilitar la imagen. Resol vieron estructuras del receptor solo y unido a tres antagonistas de interés médico: atosibán (un péptido usado para prevenir el parto prematuro) y dos pequeñas moléculas capaces de penetrar el cerebro, balovaptán y SRX246, probadas en personas con autismo o enfermedad de Huntington. Todas las estructuras alcanzaron resolución cercana a la atómica, revelando las posiciones de las siete hélices transmembrana del receptor, los bucles flexibles y los fármacos unidos.
Un receptor que prefiere actuar por parejas
A diferencia de receptores relacionados que se habían visto solo como unidades singulares, V1a apareció como un par —un dímero— en las cuatro estructuras de cryo-EM. Los dos receptores yacen lado a lado en la membrana, estableciendo contactos estrechos principalmente a través de una de sus hélices, ayudados por interacciones tanto polares como hidrofóbicas. Para comprobar si este emparejamiento también ocurre en células vivas, el equipo fusionó V1a con una proteína fluorescente brillante y utilizó un método de fotoblanqueo a nivel de molécula única: si un punto en la superficie celular contenía dos copias del receptor, su luz desaparecería en dos pasos. Aproximadamente tres cuartas partes de los puntos observados se blanquearon en exactamente dos pasos, respaldando con fuerza la idea de que V1a forma dimers de forma natural en la superficie celular. Cuando los científicos mutaron residuos clave de contacto para perturbar la interfaz, el receptor cambió hacia unidades singulares y se volvió menos sensible a la hormona y al fármaco, lo que implica que el dímero no es solo una decoración estructural sino funcionalmente importante. 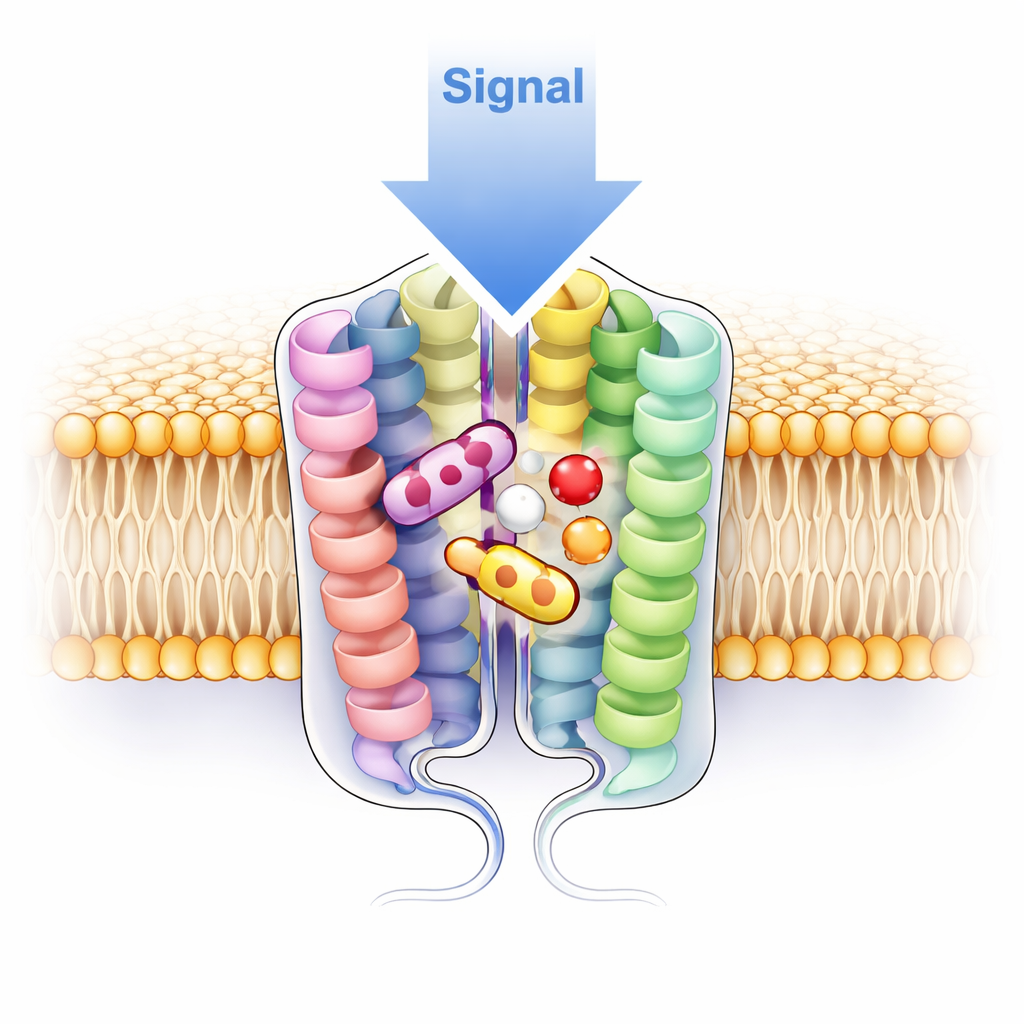
Una compuerta flexible en la entrada de la hormona
El equipo descubrió una región inesperada que actúa como “compuerta”, llamada bucle extracelular 2 (ECL2), que se sitúa en la parte superior del bolsillo de unión a la hormona. En el estado libre de fármaco (apo), este bucle yace extendido sobre el bolsillo como una tapa y no forma el enlace disulfuro habitual (un enlace azufre–azufre) que se observa en muchos receptores relacionados. En su lugar, partes del bucle se pliegan dentro del bolsillo y se mantienen en su lugar por una red de interacciones con las hélices circundantes, cubriendo parcialmente la cavidad de unión amplia y pegajosa. Cuando cualquiera de los tres antagonistas se une, ECL2 se eleva y se aleja, forma el puente disulfuro clásico y crea una cavidad ancha llena de solvente que ocupan los fármacos. Este movimiento dramático sugiere que V1a puede usar ECL2 como una barrera dinámica para limitar la activación accidental por moléculas errantes, y que los fármacos podrían diseñarse tanto para atrapar el bucle en su “estado basal” plano como para aprovechar su conformación elevada y abierta.
Cómo tres fármacos silencian el mismo receptor de maneras diferentes
El atosibán, que imita estrechamente a la hormona natural oxitocina, se extiende desde la parte superior del bolsillo hasta su base, anclándose mediante una combinación de enlaces de hidrógeno y contactos hidrofóbicos. Al cambiar unas pocas posiciones clave en comparación con la oxitocina, no logra desencadenar la cadena de desplazamientos internos normalmente requeridos para la activación del receptor: residuos cruciales que actúan como “microswitches” y que se mueven durante la señalización permanecen bloqueados en sus posiciones inactivas, la cavidad interna que acepta la proteína G nunca se abre y se altera un sitio de unión al magnesio importante para la activación. En contraste, balovaptán y SRX246 son moléculas compactas no peptídicas que se introducen profundamente en el bolsillo pero usan estrategias distintas. Balovaptán depende de un núcleo rígido e hidrofóbico que se empaqueta firmemente en una hendidura profunda, más una cola polar flexible que alcanza la entrada del bolsillo. SRX246 utiliza una arquitectura modular, similar a fragmentos, anclada por un núcleo β-lactámico, con diferentes “zonas” que taponan subpocketes y se extienden hacia los bucles extracelulares. En ambos casos, los fármacos estabilizan una conformación inactiva incompatible con la unión de la proteína G. Diferencias sutiles en la forma y química del bolsillo —especialmente en dos posiciones de las hélices 5 y 7— ayudan a explicar por qué balovaptán y SRX246 prefieren V1a frente a receptores estrechamente relacionados.
Implicaciones para futuras terapias
Al proporcionar instantáneas de alta resolución de V1a como dímero, revelar una conformación de bucle “plana” previamente no vista en el estado libre de fármaco y detallar cómo tres antagonistas muy distintos apagan el receptor, este trabajo ofrece a los diseñadores de fármacos un mapa estructural preciso para dirigirse a V1a. Sugiere maneras de diseñar medicinas de próxima generación que exploten características específicas del dímero o bloqueen el receptor en un estado basal especialmente inactivo, con el objetivo final de tratar trastornos cerebrales y relacionados con el estrés de forma más específica y con menos efectos secundarios.
Cita: Zhong, P., Chu, B., Yu, Z. et al. Molecular basis of antagonism of the dimeric human arginine vasopressin receptor 1A. Nat Commun 17, 1622 (2026). https://doi.org/10.1038/s41467-026-68331-5
Palabras clave: receptor de vasopresina V1a, receptor acoplado a proteína G, Dimerización del receptor, estructura por cryo-EM, diseño de fármacos neuropsiquiátricos