Clear Sky Science · es
Glicerol 3‑fosfato aciltransferasa agrava la toxicidad inducida por α‑sinucleína al aumentar la peroxidación lipídica
Por qué importan las grasas en el cerebro para el Parkinson
La enfermedad de Parkinson suele describirse como un problema con una proteína llamada alfa‑sinucleína que se agrupa y daña las células cerebrales que controlan el movimiento. Este estudio muestra que las grasas del cerebro —especialmente la forma en que se sintetizan y se dañan— juegan un papel sorprendentemente potente en cuán tóxica resulta la alfa‑sinucleína. Al descubrir una enzima productora de lípidos que empeora la lesión neuronal, el trabajo apunta a una vía nueva y susceptible de intervención farmacológica que podría complementar los esfuerzos existentes para abordar el Parkinson en su origen.
Una proteína que se comporta mal en el Parkinson
Las personas con Parkinson pierden gradualmente las neuronas productoras de dopamina en una región profunda del cerebro que coordina el movimiento. Dentro de estas células moribundas, los científicos suelen encontrar depósitos densos llamados cuerpos de Lewy, repletos de la proteína alfa‑sinucleína. En familias raras, mutaciones o copias adicionales del gen de la alfa‑sinucleína causan directamente el Parkinson, pero las variantes genéticas comunes en ese gen sólo aumentan modestamente el riesgo. Esto sugiere que otros genes y vías modifican cuán dañina se vuelve la alfa‑sinucleína. Cada vez hay más evidencias que señalan a los lípidos —grasas y moléculas similares a grasas que forman las membranas celulares y los depósitos energéticos— como socios clave tanto en la agregación de la alfa‑sinucleína como en la muerte neuronal.
Encuentro de una enzima lipídica poderosa en modelos de mosca de la fruta
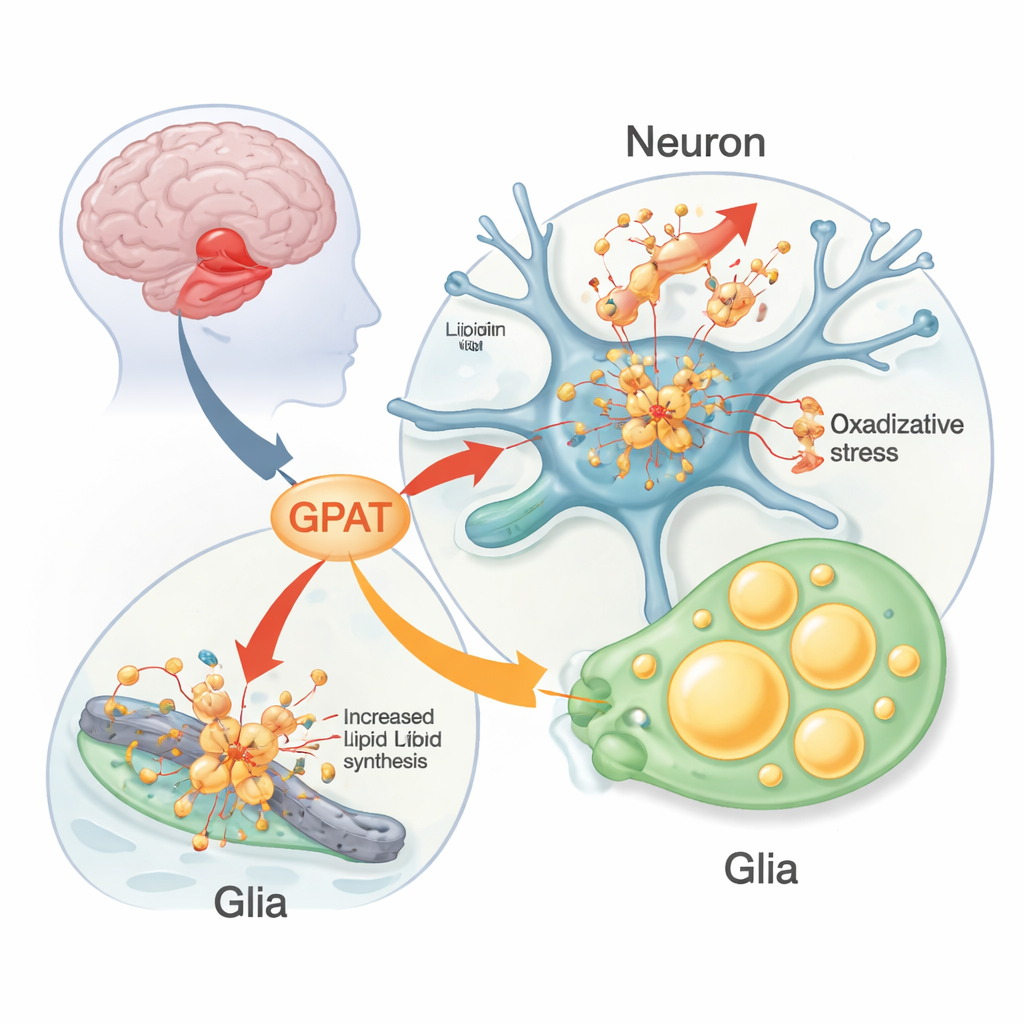
Los investigadores usaron moscas de la fruta modificadas para producir alfa‑sinucleína humana en su sistema nervioso como un banco de pruebas vivo. Estas moscas desarrollan problemas similares al Parkinson: pérdida de neuronas productoras de dopamina, dificultad para trepar y ritmos de actividad diaria alterados. El equipo modificó sistemáticamente versiones de mosca de genes de riesgo humanos para ver cuáles cambiaban el impacto de la alfa‑sinucleína. Uno destacó: un gen llamado mino, que codifica una forma mitocondrial de la enzima glicerol 3‑fosfato aciltransferasa (GPAT). GPAT se ubica en el punto de entrada de la síntesis de fosfolípidos y triglicéridos —los lípidos que forman membranas y gotas de grasa. Cuando el equipo redujo la actividad de mino en neuronas, las moscas con alfa‑sinucleína conservaron más de sus neuronas dopaminérgicas y se movieron mejor durante más tiempo; aumentar la expresión de mino provocó el efecto contrario y dañino.
Grasas dañadas, mitocondrias estresadas y gotas lipídicas en glía
Al profundizar, los científicos encontraron que GPAT influía en la cantidad de daño oxidativo acumulado en los lípidos cerebrales. En moscas con alfa‑sinucleína mantenidas a mayor temperatura (lo que agrava los rasgos de la enfermedad), la peroxidación lipídica —el “oxido” químico de las grasas— aumentó en las membranas cerebrales. Reducir mino recortó este daño, mientras que sobreexpresarlo lo incrementó; sin alfa‑sinucleína, cambiar mino tuvo poco efecto. Los marcadores de muerte celular en la región visual del cerebro reflejaron este patrón. El equipo también observó una acumulación llamativa de gotas lipídicas —pequeñas esferas de almacenamiento de grasa— no en las propias neuronas sino en las células gliales vecinas. Estas gotas se expandieron con la edad en las moscas con alfa‑sinucleína y fueron moduladas por enzimas que sintetizan o degradan triglicéridos, subrayando una asociación metabólica activa entre neuronas y glía bajo estrés.
Reconfiguración metabólica y agregación de alfa‑sinucleína
Las mediciones de metabolitos en cerebros de mosca revelaron que la expresión de alfa‑sinucleína se vinculaba a un cuello de botella en el ciclo productor de energía de la célula: el citrato y el isocitrato, dos intermedios del ciclo de los ácidos tricarboxílicos (TCA), se acumularon de forma pronunciada, mientras que los pasos posteriores cambiaron de forma más modesta. Los niveles de lactato también aumentaron, coherente con una glucólisis intensificada. Al mismo tiempo, el perfil detallado de lípidos mostró cambios en el equilibrio de fosfolípidos de membrana y en la composición de sus ácidos grasos, favoreciendo especies más propensas al daño oxidativo. Cuando el equipo redujo varias enzimas GPAT —mino en mitocondrias y enzimas relacionadas en el retículo endoplasmático— la alfa‑sinucleína todavía se acumuló, pero su tendencia a formar oligómeros de mayor orden (paquetes multiproteicos) disminuyó, y las mitocondrias mostraron menos signos de estrés por oxígeno reactivo y de “envejecimiento”.
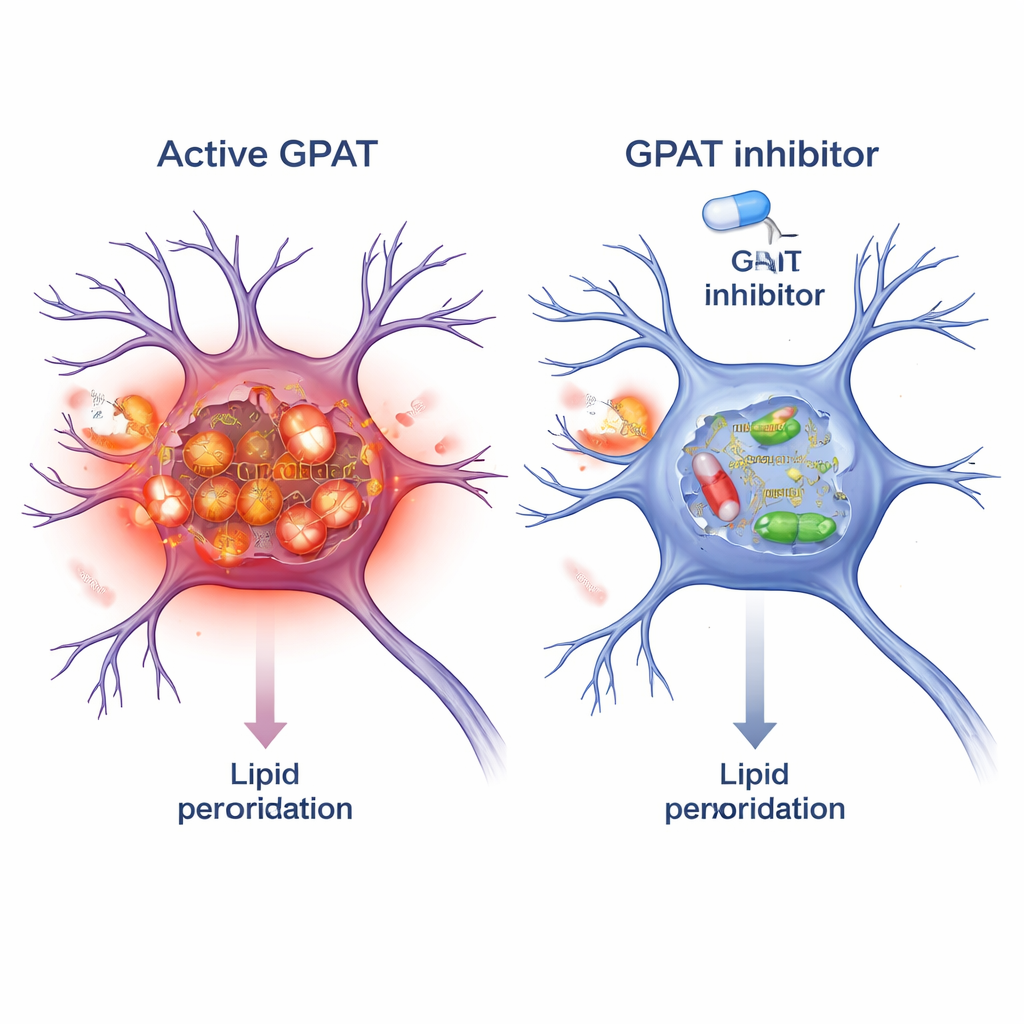
Bloquear GPAT como estrategia protectora
Puesto que GPAT es una enzima, puede ser objetivo de fármacos de pequeña molécula. Los investigadores probaron FSG67, un inhibidor de GPAT existente desarrollado originalmente para la obesidad y la diabetes. En las moscas con alfa‑sinucleína, añadir FSG67 a la comida reprodujo los beneficios del silenciamiento genético de GPAT: mejor movimiento, mayor supervivencia de las neuronas dopaminérgicas, menos oligómeros dañinos de alfa‑sinucleína y menor estrés oxidativo mitocondrial. Para comprobar si este concepto se trasladaba a mamíferos, trataron neuronas cerebrales de ratón en cultivo con fibrillas preformadas de alfa‑sinucleína, que inducen agregados tóxicos. El tratamiento conjunto con FSG67 redujo la acumulación de alfa‑sinucleína fosforilada y disminuyó múltiples marcadores independientes de peroxidación lipídica dentro de estas neuronas.
Qué significa esto para las personas con Parkinson
En términos sencillos, este trabajo muestra que la forma en que el cerebro maneja las grasas puede aumentar o disminuir la toxicidad de la alfa‑sinucleína. Cuando GPAT está altamente activa, se incorporan a las membranas y a las gotas de almacenamiento lípidos más vulnerables, lo que los hace más fáciles de oxidar; este entorno de lípidos dañados parece favorecer formas nocivas de alfa‑sinucleína y tensionar las mitocondrias, las centrales energéticas de la célula. Reducir la actividad de GPAT —ya sea genéticamente o con un fármaco— desplaza el equilibrio hacia menos “oxidación” lipídica, menos ensamblajes proteicos tóxicos y neuronas más sanas. Aunque estos hallazgos son preliminares y proceden de moscas y de células de ratón en cultivo, ponen de relieve el metabolismo de los lípidos, y GPAT en particular, como un ángulo prometedor para terapias del Parkinson que podrían complementar las estrategias que apuntan directamente a la alfa‑sinucleína.
Cita: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Palabras clave: Enfermedad de Parkinson, alfa‑sinucleína, peroxidación lipídica, inhibidor de GPAT, neurodegeneración