Clear Sky Science · es
Estructura del complejo SHOC2-KRAS-PP1C revela determinantes específicos de isoformas RAS e ideas sobre cómo dirigir el ensamblaje del complejo con inhibidores de RAS
Cómo deciden las células cuándo crecer
Nuestras células dependen de un sistema de cableado interno para decidir cuándo crecer, dividirse o permanecer inactivas. En el centro de este sistema están las proteínas RAS, diminutos interruptores moleculares que con frecuencia fallan en el cáncer. Este estudio examina en profundidad cómo un grupo particular de proteínas —SHOC2, RAS y PP1C— se unen para activar un interruptor clave de crecimiento, y cómo los fármacos modernos contra el cáncer podrían ajustarse para bloquear ese proceso de forma más eficaz y evitar que los tumores eludan el tratamiento.
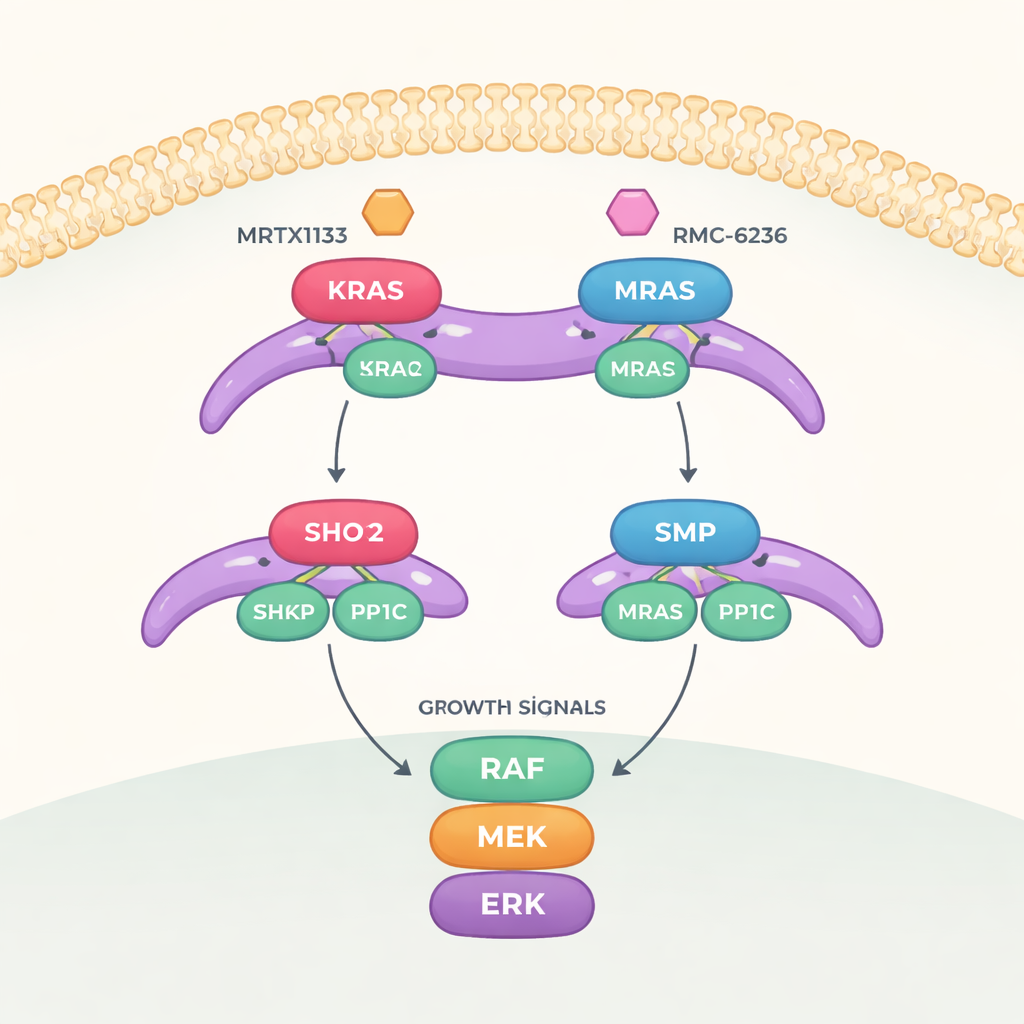
Un interruptor de crecimiento con tres partes críticas
El trabajo se centra en una ruta de señalización llamada vía MAPK, que transmite mensajes de crecimiento desde la superficie celular hasta el núcleo. Para activar por completo esta vía, otra proteína llamada RAF debe cambiar de un estado “apagado” a uno “encendido”. Ese cambio está controlado por un complejo de tres partes formado por SHOC2 (un andamio que mantiene unidas las piezas), PP1C (una enzima que elimina una etiqueta de fosfato) y una proteína RAS activa. Cuando se ensamblan, este trío elimina una marca de fosfato específica de RAF, liberándola para activar la cascada de crecimiento aguas abajo.
Por qué un socio de menor afinidad sigue siendo importante en el cáncer
Existen varios tipos de proteínas RAS. MRAS forma un complejo muy estable con SHOC2 y PP1C, mientras que los conductores de cáncer más conocidos KRAS, HRAS y NRAS forman versiones más débiles del mismo complejo. Sorprendentemente, las células cancerosas impulsadas por KRAS, HRAS o NRAS mutantes muestran una fuerte dependencia de SHOC2, aun cuando sus complejos son menos estables. Grandes conjuntos de datos de cribado genético muestran que muchos tumores con ciertas mutaciones en RAS —especialmente las que afectan posiciones clave como Q61 y G13— son muy sensibles a la pérdida de SHOC2, lo que significa que este ensamblaje es esencial para su supervivencia.
Revelando la forma del complejo con KRAS
Hasta ahora, los científicos solo habían observado una estructura de alta resolución del complejo basado en MRAS, que es de alta afinidad. La versión más débil con KRAS se desarmaba con facilidad y era difícil de capturar. En este estudio, los autores emplearon mutaciones vinculadas a enfermedad que fortalecen sutilmente los contactos entre los componentes para estabilizar el complejo SHOC2–KRAS–PP1C el tiempo suficiente como para obtener imágenes por criomicroscopía electrónica. Hallaron que la arquitectura general coincide estrechamente con la del complejo MRAS, pero KRAS carece de varias pequeñas características estructurales que MRAS usa para agarrar con mayor firmeza a SHOC2 y PP1C. Como resultado, el ensamblaje con KRAS oculta menos área de contacto y forma menos enlaces, lo que explica por qué es intrínsecamente menos estable, aunque sigue siendo muy importante en tumores donde KRAS está sobreactivado.
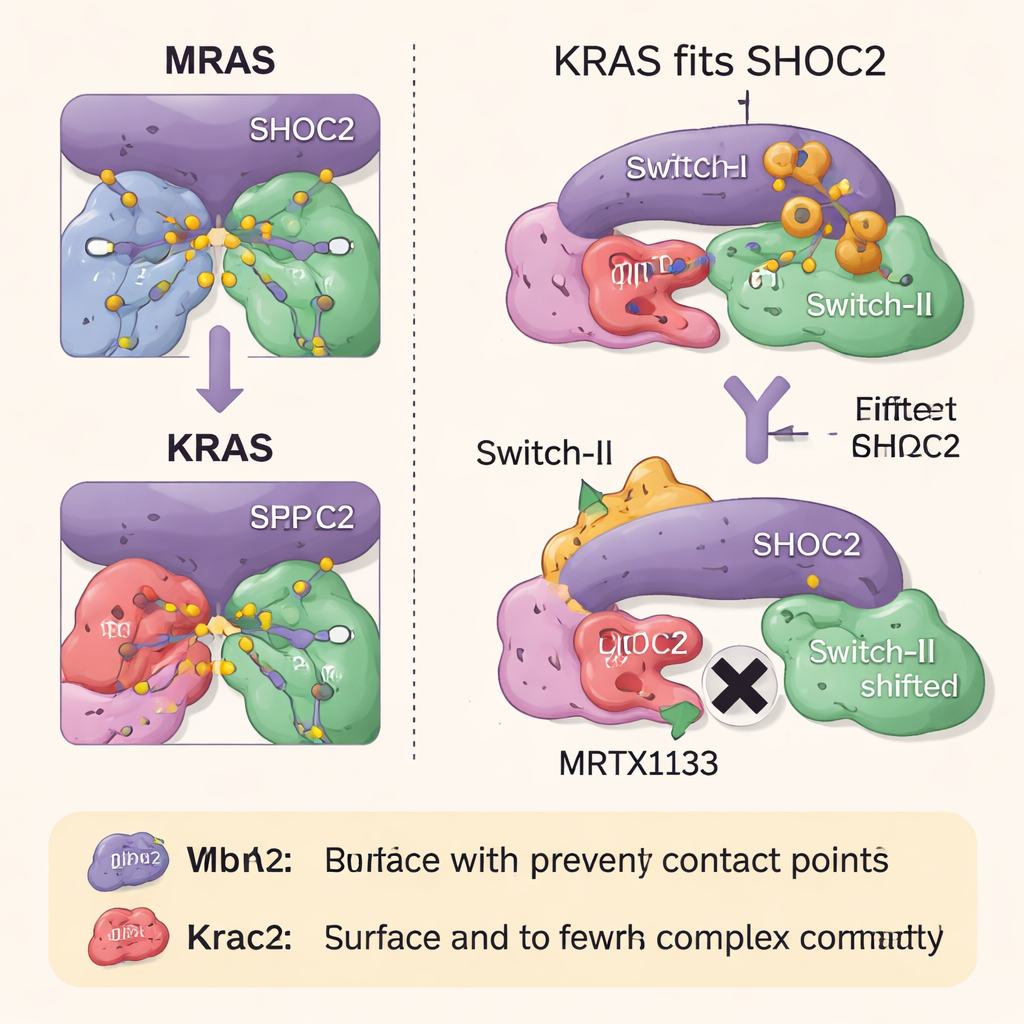
Cómo los fármacos contra RAS bloquean el ensamblaje del complejo
El equipo exploró cómo dos clases de fármacos dirigidos a RAS afectan a este complejo de tres partes. MRTX1133, diseñado para unirse a una cavidad cerca de una región flexible de KRAS conocida como Switch-II, bloquea esa región en una conformación que choca con la superficie de SHOC2. Esto impide con fuerza la formación de nuevos complejos SHOC2–KRAS–PP1C, aunque es menos eficaz para deshacer los complejos ya existentes. Un segundo fármaco, RMC-6236, actúa junto con una proteína auxiliar (ciclofilina A) y también bloquea las mismas superficies de KRAS necesarias para la unión a SHOC2. Sin embargo, ninguno de los dos fármacos se une de forma natural a MRAS, por lo que el complejo de alta afinidad con MRAS permanece intacto y puede ayudar a reactivar la vía de crecimiento cuando KRAS está inhibido.
Hacia un doble objetivo para prevenir la resistencia
Para probar si es posible un doble objetivo, los investigadores diseñaron una variante de MRAS cuya cavidad Switch-II fue modificada para que MRTX1133 pudiera unirse. Este mutante seguía formando un complejo fuerte con SHOC2 y PP1C, pero el fármaco pasó a bloquear su ensamblaje y redujo su capacidad para activar RAF en ensayos de tubo de ensayo. Junto con datos sobre compuestos que se unen a SHOC2, estos resultados muestran que es realista diseñar fármacos que apaguen tanto los complejos basados en KRAS como en MRAS. Para el público general, el mensaje clave es que las células cancerosas usan múltiples interruptores estrechamente relacionados para mantener el flujo de señales de crecimiento, especialmente cuando uno de los interruptores está inhibido por un fármaco. Al comprender las formas y los contactos precisos dentro de estos ensamblajes proteicos, los investigadores pueden ahora planificar terapias que ataquen ambas rutas de respaldo a la vez, dificultando que los cánceres impulsados por RAS se adapten y desarrollen resistencia al tratamiento.
Cita: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Palabras clave: Señalización RAS, Inhibidores de KRAS, Vía MAPK, Complejos proteicos, Resistencia a fármacos