Clear Sky Science · es
Control de pH reversible mediado por lípidos de conexina-46/50 mediante crio‑EM
Por qué importan para la salud y la enfermedad estos minúsculos canales celulares
Cada segundo, nuestras células intercambian señales eléctricas y pequeñas moléculas a través de túneles microscópicos llamados uniones gap. Estos canales ayudan a que el corazón lata al unísono, que el cerebro elimine subproductos tóxicos y que el cristalino del ojo permanezca transparente. Cuando las condiciones dentro de las células se vuelven ácidas, como ocurre durante un ictus, un infarto o la formación de cataratas, muchos de estos canales se cierran; sin embargo, cómo detectan y responden a la acidez ha sido durante mucho tiempo un misterio. Este estudio utiliza microscopía crioelectrónica de alta resolución para revelar, casi átomo a átomo, cómo canales específicos del cristalino ocular se cierran en respuesta al ácido y cómo este proceso puede revertirse por completo.
Túneles celulares que mantienen los tejidos sincronizados
Las uniones gap están formadas por proteínas llamadas conexinas, que se ensamblan en canales en forma de anillo que atraviesan las membranas de dos células vecinas. Este trabajo se centra en un par de conexinas estrechamente relacionadas, conexina‑46 y conexina‑50, que forman canales en el cristalino del ojo. Estos canales permiten que iones y pequeñas moléculas fluyan directamente entre células, ayudando a mantener la claridad del cristalino y la salud del tejido. Sin embargo, cuando las células están estresadas, esos mismos canales pueden convertirse en vías para señales dañinas. Para proteger los tejidos, las uniones gap se cierran cuando el interior celular se vuelve más ácido. Entender el mecanismo a escala fina de este “cierre por pH” es importante para descifrar cómo los tejidos sobreviven al estrés y por qué ciertas mutaciones conducen a enfermedades como las cataratas.
Ver el movimiento de los canales con crio‑EM
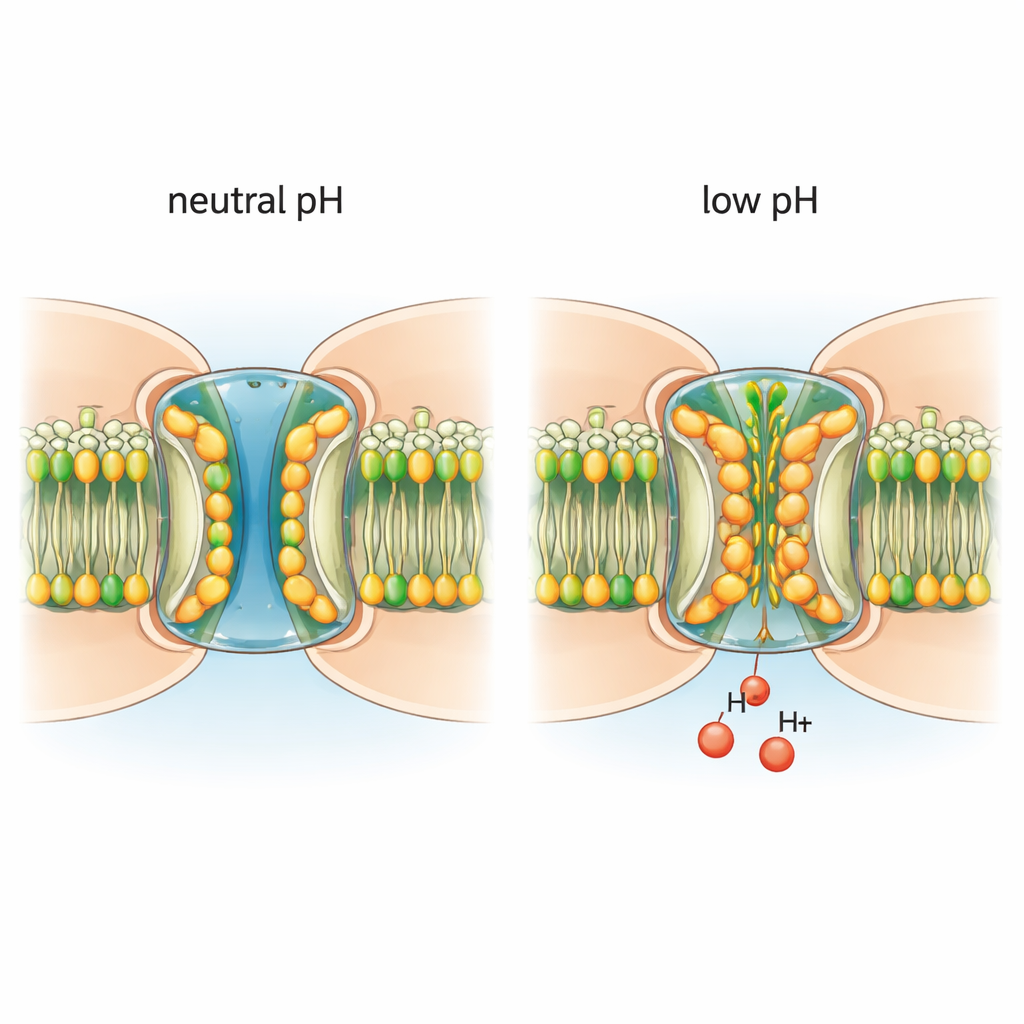
Los investigadores purificaron canales nativos de conexina‑46/50 de cristalinos de oveja envejecidos y los incorporaron en una membrana modelo. Usando microscopía crioelectrónica, tomaron imágenes de los canales a resolución casi atómica en condiciones neutras, que favorecen un poro abierto, y en condiciones ligeramente ácidas, que desencadenan el cierre. A pH neutro, los canales adoptan en su mayoría un estado abierto estable, con un túnel central lo suficientemente amplio para iones y pequeñas moléculas y con un segmento flexible, el dominio N‑terminal, que recubre la entrada del poro. En estas condiciones el poro está limpio: no hay moléculas extra que obstaculicen el paso y los lípidos de la membrana circundante permanecen ordenados en capas regulares.
El ácido atrae lípidos hacia el poro
Cuando el entorno se hizo ligeramente ácido, la arquitectura del canal cambió de forma llamativa. Moléculas lipídicas de la membrana circundante fueron atraídas hacia el poro, deslizándose entre y por debajo de los segmentos N‑terminales. Estos lípidos invasores forman una “junta” hidrofóbica de dos capas que empuja los dominios N‑terminales hacia el interior, estrechando el canal y contribuyendo a bloquear el paso. Lípidos adicionales se intercalan entre subunidades proteicas vecinas en sus interfaces, aparentemente sirviendo como vías de entrada desde la membrana hacia el poro. De forma importante, cuando los canales se colocaron en un entorno detergente que carece de una membrana lipídica verdadera, el pH bajo ya no inducía estos cambios estructurales. Esto demuestra que los lípidos reales no son meros espectadores: son socios necesarios en el proceso de regulación por pH.
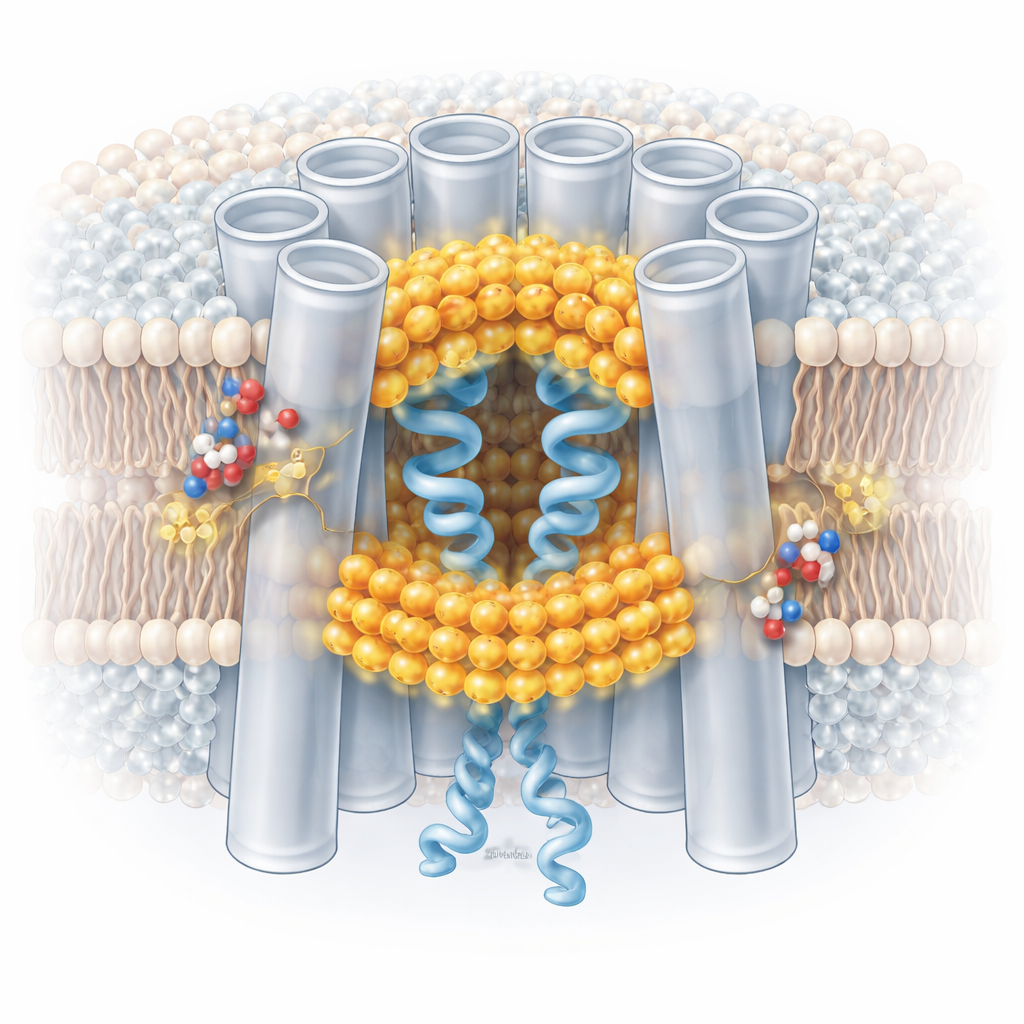
Un interruptor de seguridad reversible y finamente afinado
Al seguir millones de partículas individuales de canal, los autores encontraron que el pH bajo no simplemente cambia los canales de totalmente abiertos a totalmente cerrados. En su lugar, desplaza la población hacia una mezcla de estados: algunas subunidades dentro de un canal muestran conformaciones bloqueadas y estabilizadas por lípidos, mientras que otras permanecen más abiertas. El comportamiento de cierre es en gran medida no cooperativo: cada bloque estructural del canal puede responder de forma algo independiente. Las condiciones ácidas favorecen estas conformaciones bloqueadas, pero cuando el pH vuelve a neutral, los lípidos del poro regresan a la membrana y los canales revierten al estado abierto. Aminoácidos conservados llamados histidinas, que adquieren carga positiva a pH bajo, parecen ayudar a reclutar y estabilizar los lípidos interfaciales que inician este proceso, ofreciendo un sensor molecular de pH plausible.
Implicaciones para las cataratas y la protección tisular
Estos resultados respaldan un modelo en el que los lípidos actúan como tapones móviles que controlan de forma reversible el flujo a través de las uniones gap en respuesta a la acidez. En el cristalino del ojo, un mecanismo así puede ayudar a aislar células dañadas y evitar que señales tóxicas se propaguen, aunque un cierre crónico o mal regulado también podría contribuir a la formación de cataratas relacionadas con la edad. Dado que se han observado intrusiones lipídicas similares en familias de canales relacionadas, el trabajo sugiere un principio más general: bajo estrés, las propias membranas celulares pueden suministrar componentes dinámicos que ayudan a activar o desactivar canales vitales, ofreciendo nuevas ideas para fármacos que estabilicen ya sea el estado abierto o el cerrado en enfermedad.
Cita: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Palabras clave: uniones gap, conexina 46/50, regulación por pH, catarata, crio‑EM