Clear Sky Science · es
Transcriptómica unicelular dinámica revela la formación de redes neuronales guiada por lsamp en machos de S. japonicum que impulsa la reproducción femenina
Por qué importa la vida amorosa de un parásito
La esquistosomiasis es una enfermedad parasitaria que enferma a más de 250 millones de personas, sobre todo en regiones pobres con acceso médico limitado. La enfermedad no la causan las mordeduras o toxinas de los gusanos, sino la enorme cantidad de huevos que depositan las hembras dentro del cuerpo. Sorprendentemente, las hembras solo pueden madurar y empezar a poner huevos tras emparejarse con un macho. Este estudio plantea una pregunta simple pero crucial: ¿qué hace exactamente el macho para activar la fertilidad de la hembra, y podría desactivarse ese interruptor para detener la enfermedad?
Mapear un mundo oculto célula a célula
Para responder, los investigadores construyeron un detallado “atlas celular” del trematodo sanguíneo Schistosoma japonicum durante la ventana clave en que machos y hembras se emparejan y alcanzan la madurez sexual. Usando secuenciación de ARN unicelular, una técnica que lee qué genes están activos en células individuales, analizaron más de 100.000 células de gusanos recolectados en cuatro puntos temporales tras la infección en ratones. Identificaron 76 tipos celulares distintos, incluidos muchos tipos de neuronas, células madre y células reproductoras. Esto les permitió seguir cómo poblaciones celulares concretas se expanden, se contraen o cambian de identidad a medida que los gusanos crecen y comienzan a reproducirse.
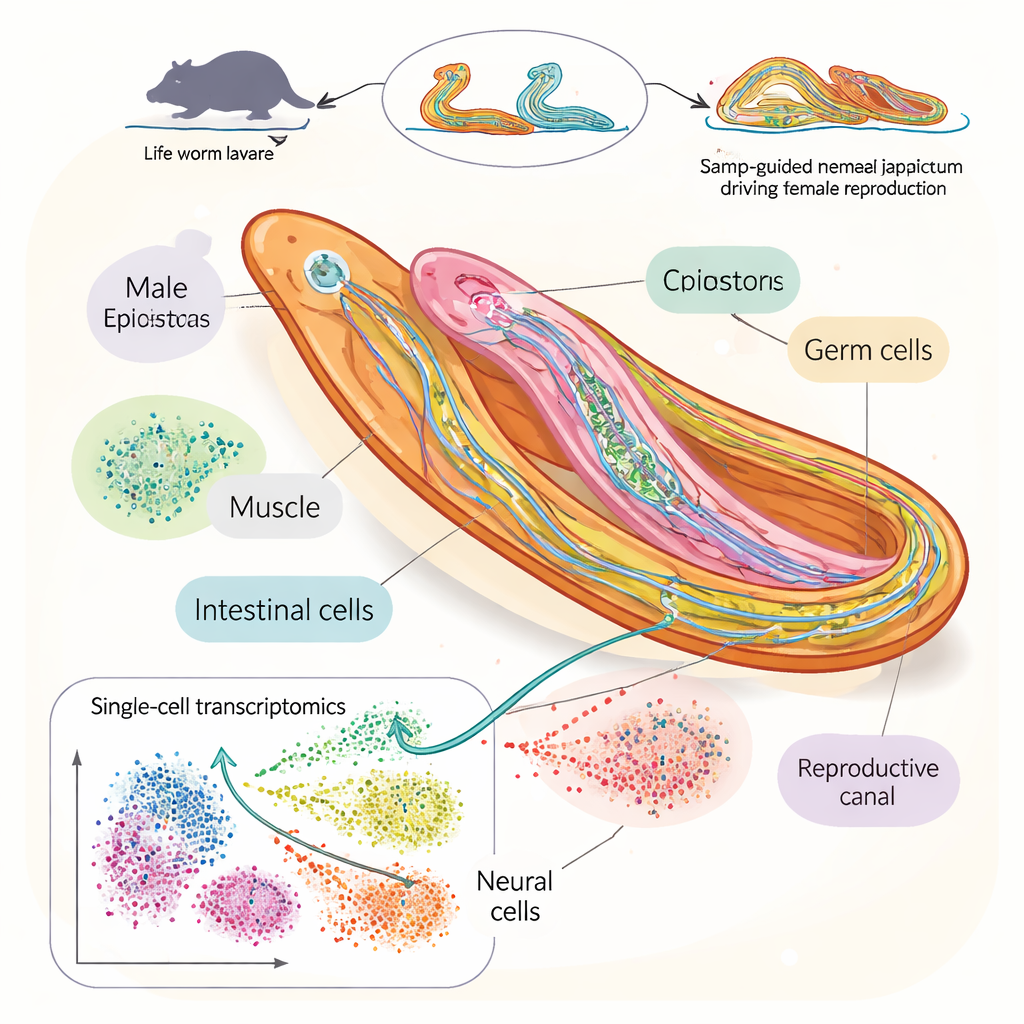
Siguiendo el aumento de huevos y espermatozoides
Al centrarse en células de testículos, ovarios y tejidos relacionados, el equipo reconstruyó el desarrollo escalonado de espermatozoides y óvulos. Mostraron cómo las células madre germinales dan lugar a células espermáticas y ovocíticas en estadios tardíos mediante programas de actividad génica distintos en machos y hembras. En las hembras, los genes que apoyan el crecimiento de los huevos enfatizan la producción y el empaquetado de proteínas, mientras que en los machos se orientan más a estructuras como los cilios y los microtúbulos que ayudan al movimiento de los espermatozoides. El estudio también trazó cómo se desarrolla el masivo órgano de soporte de los huevos en las hembras, la vitelaria, pasando por estadios intermedios, y identificó nuevos marcadores genéticos que revelan el grado de madurez de cada tejido reproductivo.
Un circuito nervioso exclusivo de machos en un canal de agarre
Uno de los descubrimientos más llamativos provino del sistema nervioso. Lejos de ser una colección dispersa de neuronas, el atlas reveló cinco linajes neuronales claros, incluidos varios que diferían entre machos y hembras. Tres tipos neuronales—denominados N2.2, N3.2 y N4.3—estaban fuertemente enriquecidos en machos y se agruparon dentro del canal ginecóforo, una ranura especializada que el macho usa para acunar a la hembra. Entre ellas, las neuronas N4.3 destacaron porque expresaban un gen llamado nrps, que codifica la enzima que produce BATT, un pequeño péptido feromonal mostrado previamente como estimulador del desarrollo sexual femenino. En otras palabras, estas células N4.3 son las “estaciones de señal” del macho para activar la fertilidad femenina.
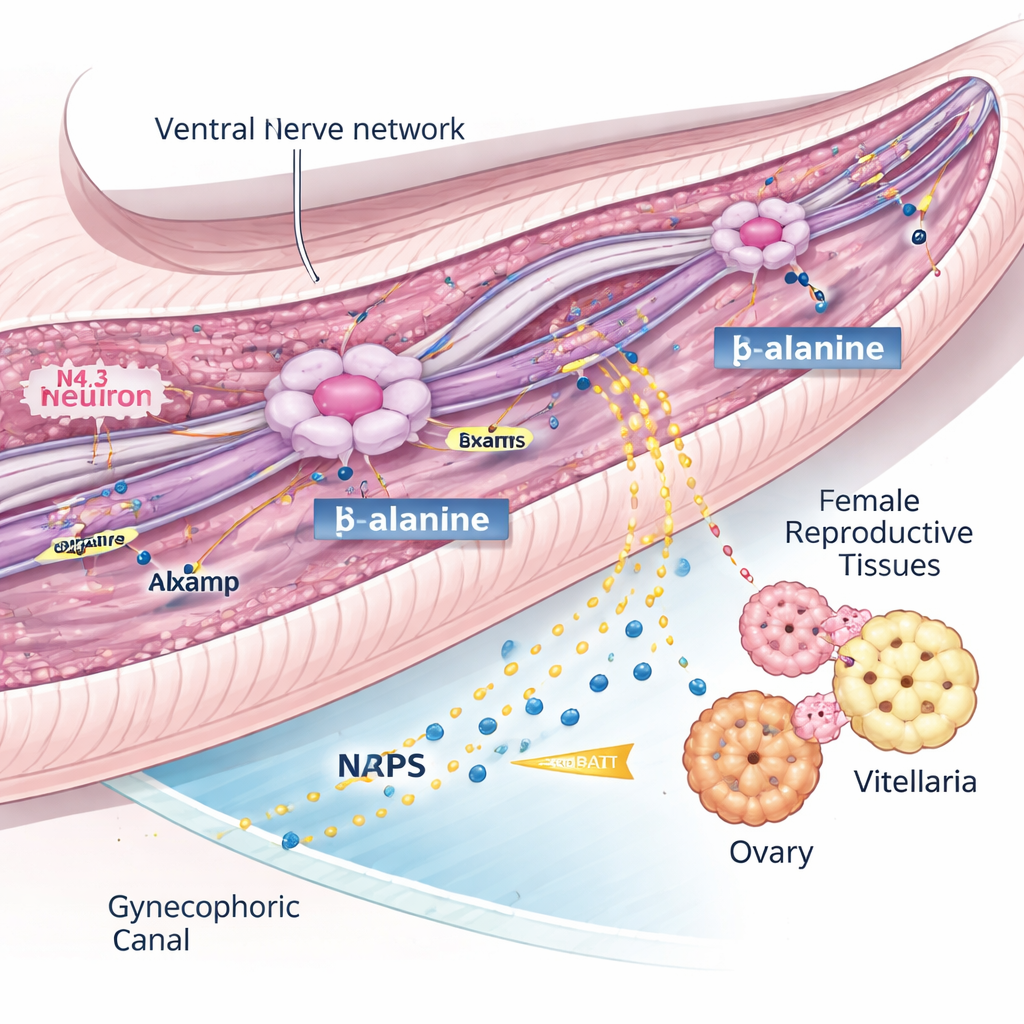
Una molécula guía que mantiene la señal
Para entender cómo funcionan estas neuronas N4.3, los investigadores buscaron genes que parecieran dirigir su desarrollo y función. Se centraron en lsamp, un gen conocido en otros animales por ayudar a las neuronas a conectarse y mantener sus axones. En los flukes machos, lsamp se activó en las mismas neuronas N4.3 que producen la enzima BATT, y su actividad aumentó de forma pronunciada a medida que los gusanos maduraban. Usando interferencia de ARN para reducir lsamp en machos, el equipo encontró que las hembras emparejadas no desarrollaban completamente sus ovarios y vitelaria y ponían casi ningún huevo. Sin embargo, las neuronas N4.3 seguían presentes, el gen nrps seguía activo y los ingredientes químicos brutos para BATT permanecían sin cambios. En su lugar, los machos con deficiencia de lsamp mostraron fibras nerviosas dañadas y transporte vesicular alterado a lo largo de microtúbulos estabilizados, y produjeron mucho menos BATT tanto dentro del cuerpo como en el medio circundante. Esto sugiere que lsamp es vital para mantener una red nerviosa ventral que entrega un precursor clave, probablemente β-alanina, a las neuronas N4.3 para que puedan sintetizar suficiente feromona que active a la hembra.
Apagar el interruptor reproductivo
Para quienes no son especialistas, el mensaje principal es que la capacidad de este parásito para causar enfermedad depende de una conversación íntima entre machos y hembras, llevada a cabo a través de una red nerviosa especializada y una diminuta feromona. El estudio muestra que una única molécula guía, lsamp, ayuda a construir y mantener el cableado nervioso ventral del macho; cuando ese cableado falla, el macho ya no puede enviar una señal química lo bastante fuerte como para madurar por completo los órganos reproductivos femeninos, y la puesta de huevos cae drásticamente. Al cartografiar las células del parásito con alta resolución y descubrir este circuito neural exclusivo de machos, el trabajo apunta a nuevas maneras de bloquear la producción de huevos—ofreciendo una estrategia potencial para frenar la esquistosomiasis en un contexto en el que el tratamiento actual depende de un único fármaco envejecido.
Cita: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Palabras clave: esquistosomiasis, transcriptómica unicelular, reproducción de parásitos, circuitos neuronales, señalización por feromonas