Clear Sky Science · es
Mecanismo de resistencia de SARS-CoV-2 a antivirales basados en análogos de nucleótidos
Cómo el virus elude medicamentos antivirales clave
El virus causante de la COVID-19 pertenece a un grupo poco común de virus de ARN que pueden corregir errores en su material genético, lo que lo hace inusualmente eficaz para resistir algunos de nuestros mejores antivirales. Este estudio profundiza en los detalles a escala atómica de cómo SARS‑CoV‑2 detecta y elimina una clase de medicamentos de uso extendido llamados análogos de nucleótidos, y explica por qué fármacos que funcionan bien contra otros virus a menudo rinden menos frente a las infecciones por coronavirus.
Un tira y afloja alrededor del ARN viral
SARS‑CoV‑2 copia su genoma de ~30.000 letras de ARN usando una gran máquina molecular llamada complejo de replicación‑transcripción. En su centro está la ARN polimerasa dependiente de ARN (RdRp), que construye nuevas cadenas de ARN, y una unidad separada, la exonucleasa (ExoN), que corrige y recorta errores. Muchas pastillas antivirales, incluidos fármacos desarrollados originalmente para la hepatitis C, imitan lo suficientemente bien los bloques de construcción naturales del ARN como para ser insertadas por la RdRp, pero con modificaciones sutiles que frenan la copia o introducen errores. Desafortunadamente, los coronavirus tienen ExoN, que puede reconocer a estos impostores una vez que están en la cadena de ARN y cortarlos, rescatando así la replicación viral.
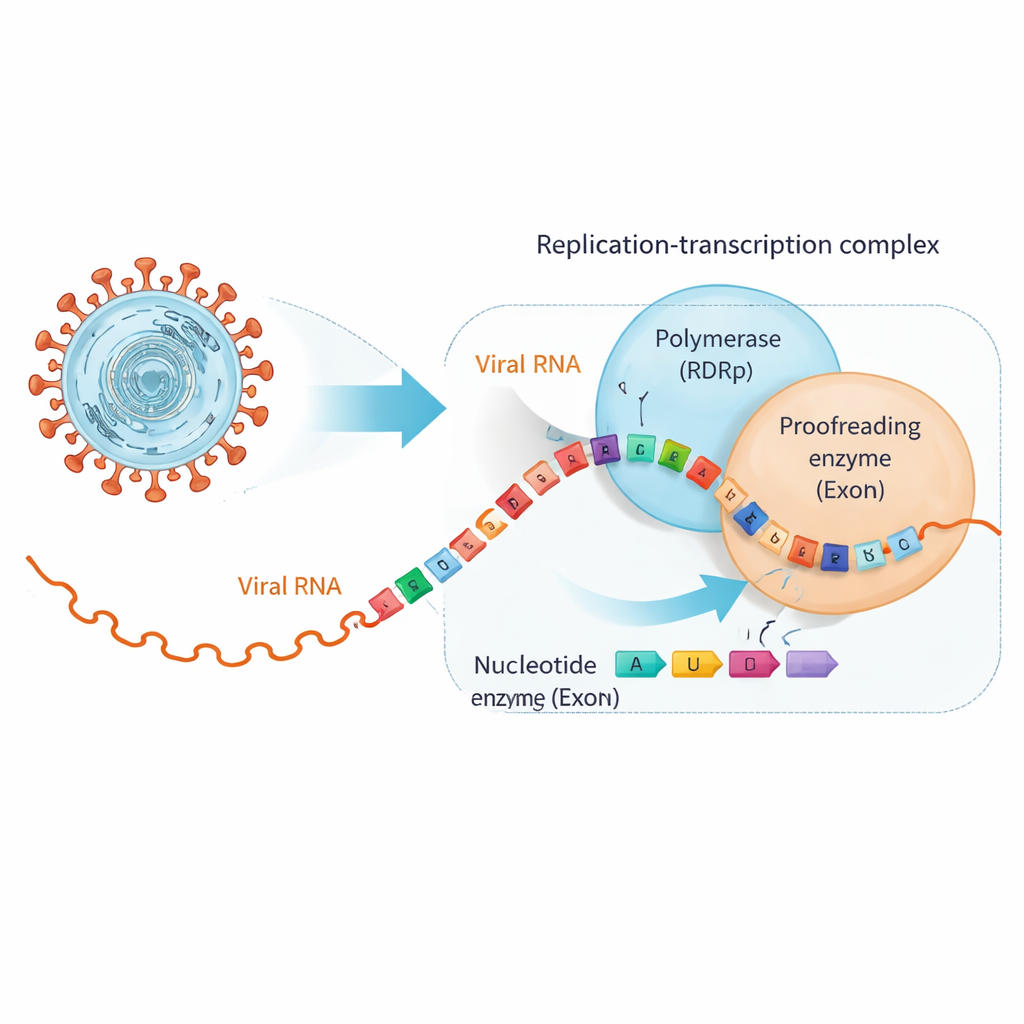
Cuando los fármacos útiles hacen que el ARN cambie de compañero
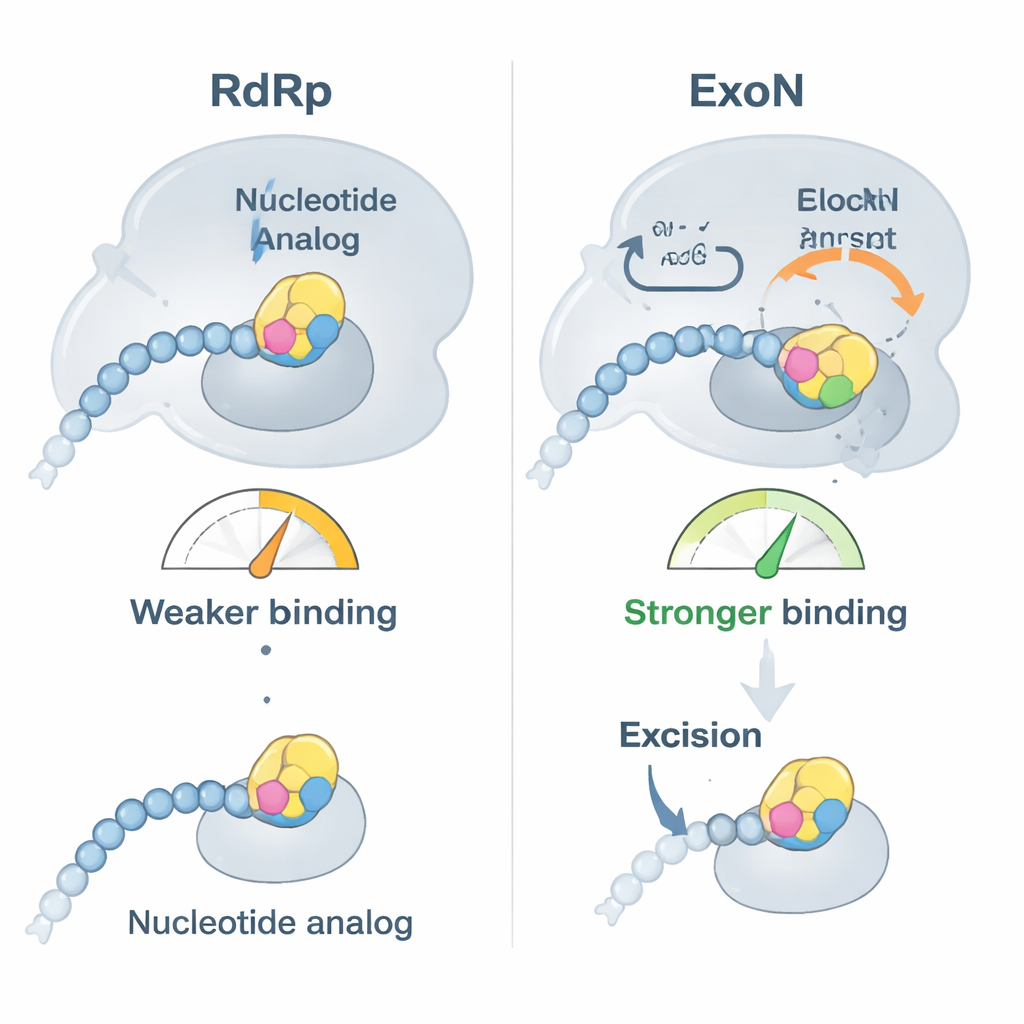
Los investigadores se centraron en dos antivirales clínicamente relevantes, bemnifosbuvir y sofosbuvir, ambos diseñados para actuar como bloques defectuosos del ARN. Primero demostraron que la polimerasa de SARS‑CoV‑2 inserta con facilidad estos análogos en el extremo de una cadena de ARN y que acto seguido la extensión de la cadena se detiene en gran medida, como se esperaba. Sin embargo, las pruebas de unión revelaron un giro: una vez que un análogo queda en la punta del ARN, éste deja de unirse con tanta firmeza a la polimerasa y, en cambio, se une más fuertemente a ExoN. En efecto, el ARN modificado por el fármaco se aleja de la ‘máquina de copia’ y se entrega al corrector, que entonces tiene la oportunidad de cortar el nucleótido problemático y permitir que la replicación continúe.
Una corrección de errores que se ralentiza pero no se detiene
Experimentos bioquímicos a lo largo del tiempo mostraron que ExoN sí elimina bemnifosbuvir y sofosbuvir del ARN, pero más despacio que al retirar nucleótidos normales. En reacciones sin células, ambos análogos bloquearon con fuerza la síntesis adicional de ARN—sin embargo, cuando se añadió ExoN activo, una fracción significativa de las cadenas de ARN detenidas fue rescatada y extendida. Un mutante de ExoN inactivo no pudo hacerlo, confirmando que la actividad correctora es responsable de deshacer gran parte del efecto de los fármacos. La presencia simultánea de la polimerasa y ExoN aceleró en realidad la eliminación de los análogos, lo que sugiere que las dos enzimas virales trabajan en conjunto para despejar obstáculos y mantener la replicación en marcha.
Observando al corrector con resolución atómica
Para entender cómo ExoN reconoce y responde a estos fármacos, el equipo usó microscopía crioelectrónica de alta resolución para resolver estructuras del complejo ExoN unido a hebras de ARN que terminaban ya sea en bemnifosbuvir o en sofosbuvir. Estas estructuras, lo bastante nítidas para distinguir grupos químicos individuales, mostraron que el anillo de azúcar modificado de cada fármaco encaja en un bolsillo hidrófobo formado por un bucle corto de la proteína ExoN. Este encaje adicional explica la mayor afinidad del ARN que contiene el fármaco por ExoN. Pero también tiene un efecto secundario inesperado: al tirar de ese bucle, los fármacos alteran la disposición precisa de un bucle catalítico cercano que mantiene una histidina clave en su lugar. Cuando esta histidina se aleja del sitio de corte, el centro activo de ExoN queda parcialmente desactivado, ralentizando pero sin impedir por completo la excisión del análogo.
Un interruptor incorporado que ajusta la corrección de errores viral
La mutación de aminoácidos individuales dentro del bucle sensible confirmó su importancia. Cambios en cuatro residuos conservados redujeron considerablemente la capacidad de ExoN para cortar tanto extremos de ARN estándar como extremos terminados en fármaco, y también alteraron cuál nucleótido final prefiere eliminar ExoN. Esto identifica al bucle como un regulador alostérico—un interruptor mecánico incorporado que detecta qué tipo de nucleótido está en la punta del ARN y ajusta la actividad de la enzima. Las estructuras muestran además que ExoN reconoce diferentes bases (A, U, C o G) mediante enlaces de hidrógeno flexibles, pero tiene más dificultades para acomodar bases similares a la guanina, lo cual es relevante porque bemnifosbuvir imita la guanosina.
Qué significa esto para futuras pastillas contra la COVID-19
Para el público general, el mensaje clave es que SARS‑CoV‑2 posee un sofisticado “corrector ortográfico” que puede extraer ciertos fármacos de su genoma después de que hayan logrado frenar la replicación. Bemnifosbuvir y sofosbuvir debilitan la máquina de copia del virus, pero al mismo tiempo dirigen el ARN hacia el corrector que puede deshacer parcialmente sus efectos. Al revelar exactamente cómo el corrector viral agarra estos fármacos y cómo un pequeño bucle regulador cambia la enzima entre estados más activos y menos activos, este trabajo ofrece una hoja de ruta para diseñar nuevos nucleótidos antivirales que o bien se unan poco a ExoN, lo bloqueen en una conformación inactiva, o exploten su dificultad para manejar estructuras parecidas a la guanina. Tales moléculas de nueva generación podrían ser mucho más difíciles de “borrar” para el virus, mejorando nuestra capacidad para tratar la COVID‑19 y futuros brotes de coronavirus.
Cita: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Palabras clave: SARS-CoV-2, resistencia antiviral, análogos de nucleótidos, corrección de errores del ARN, replicación de coronavirus