Clear Sky Science · es
El ataque de un ácido de Lewis que provoca el derrame de hidroxilo permite la electrooxidación selectiva de la urea a nitrito con producción simultánea de hidrógeno ahorradora de energía
Convertir residuos en químicos útiles y combustible limpio
La urea es más conocida como componente de la orina y los fertilizantes, pero en las aguas residuales se convierte en un contaminante persistente. Este estudio muestra cómo la urea puede transformarse de pasivo a recurso: mediante un catalizador diseñado con criterio, los autores convierten la urea en nitrito, un químico valioso para fertilizantes y medicamentos, mientras producen simultáneamente hidrógeno usando menos electricidad que la electrolisis del agua convencional. El trabajo ofrece una visión de plantas de tratamiento futuras que limpian el agua, fabrican productos útiles y generan energía limpia al mismo tiempo.
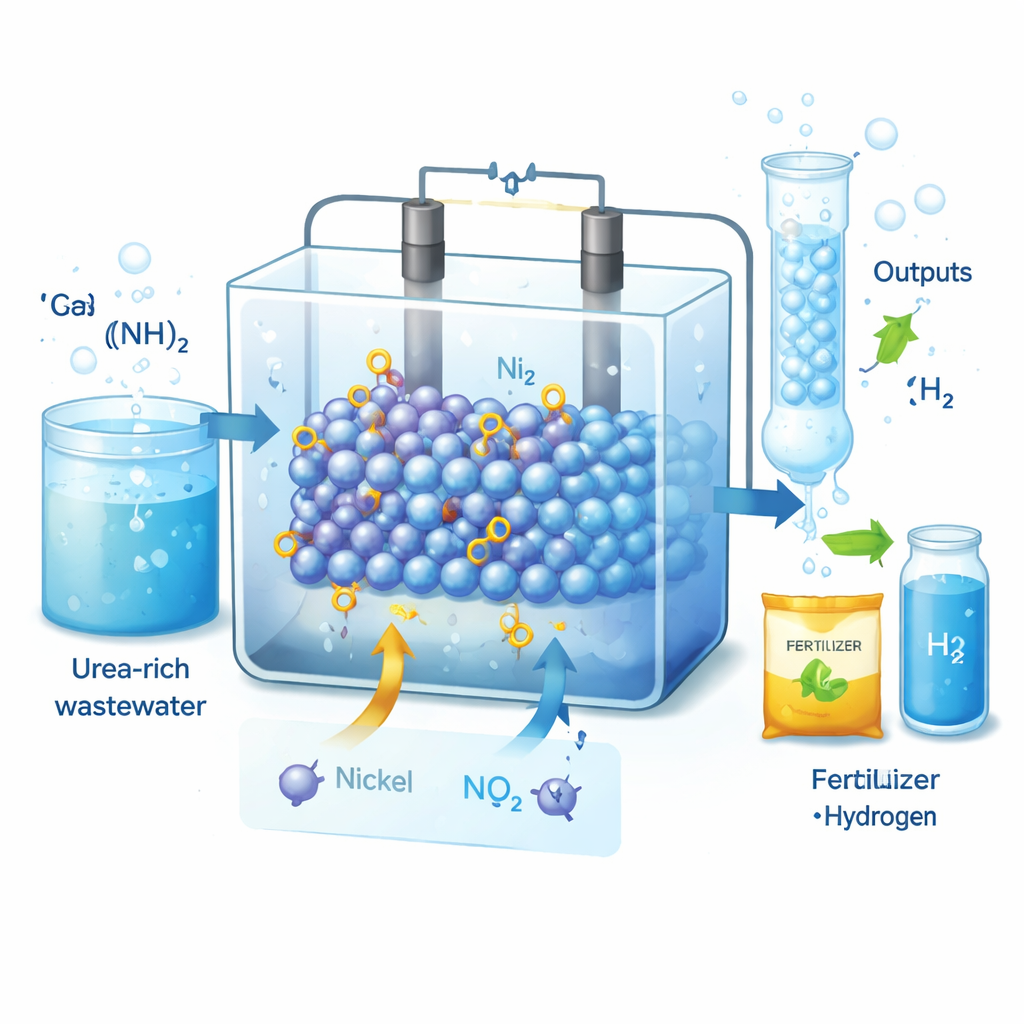
Por qué importan el nitrito y el hidrógeno
El nitrito es un ingrediente clave en la agricultura, la conservación de alimentos y la industria farmacéutica, y la demanda mundial se mide en millones de toneladas al año. Hoy la mayor parte del nitrito se produce por el proceso Ostwald, que funciona a alta temperatura, consume grandes cantidades de energía y libera óxidos de nitrógeno contaminantes. Al mismo tiempo, las aguas residuales domésticas e industriales transportan una gran carga de urea, que representa el 70–80 % de los contaminantes nitrogenados. Si esa urea pudiera transformarse electroquímicamente en nitrito produciendo además hidrógeno, podríamos limpiar el agua y suministrar dos productos de alto valor—siempre que el proceso sea suficientemente eficiente y selectivo.
Guiar las reacciones por la vía correcta
Cuando la urea se oxida en solución alcalina, puede seguir dos vías principales. Una conduce a gas nitrógeno inofensivo y dióxido de carbono; la otra, más deseable, conduce a nitrito y nitrato, que son productos comercializables. El problema es que la mayoría de los catalizadores basados en níquel, pilares de esta reacción, no son muy selectivos; tienden a producir una mezcla de productos y además desperdician energía impulsando la reacción de evolución de oxígeno, que genera oxígeno gaseoso pero no ingresos. Los autores se propusieron rediseñar la superficie catalítica de modo que los iones hidroxilo, las especies reactivas OH⁻ en medios alcalinos, se concentren y dirijan de forma que favorezcan la ruptura de enlaces carbono–nitrógeno y la formación de nitrito en lugar de permitir que los átomos de nitrógeno se acoplen para formar N₂.
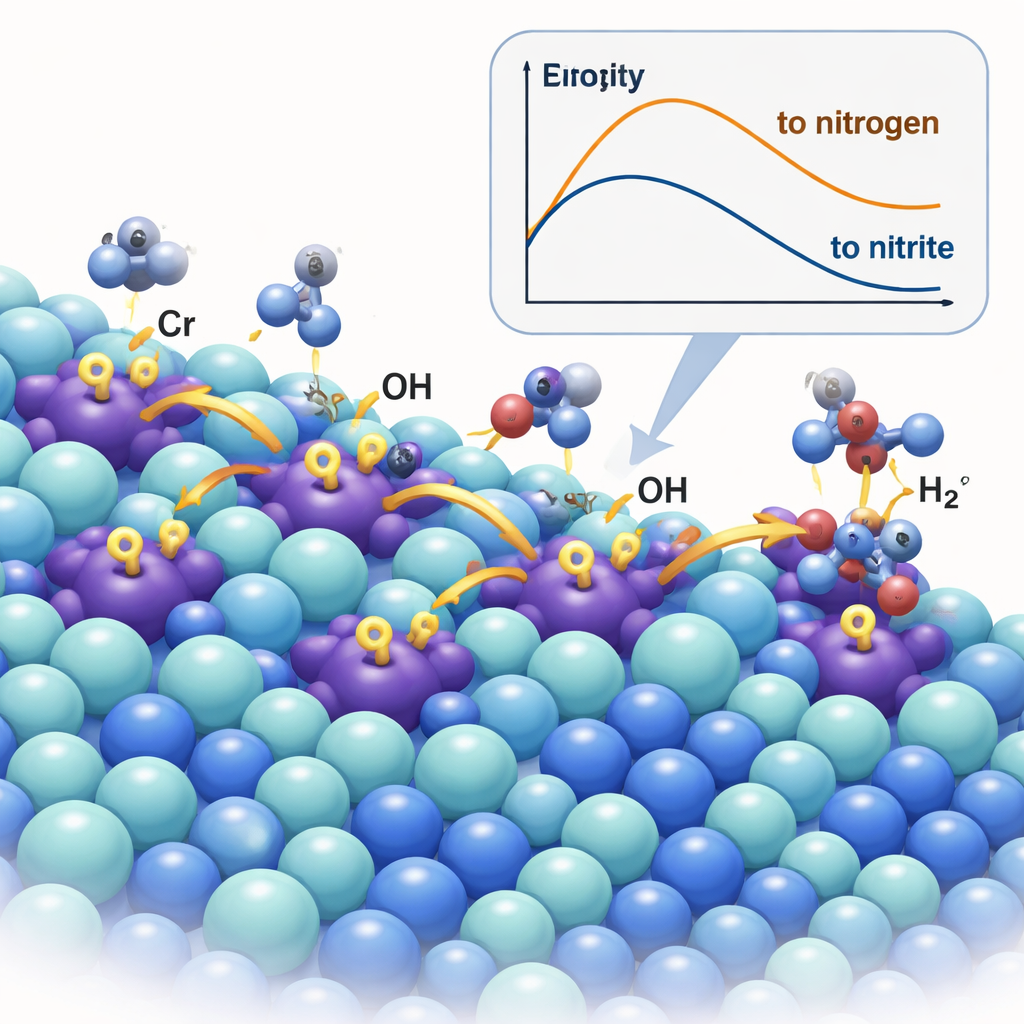
Un catalizador que bombea especies reactivas
El equipo creó un nuevo material dopando sulfuro de níquel (Ni₃S₂) con una pequeña cantidad de cromo, formando Cr–Ni₃S₂. Los iones de cromo actúan como lo que se llaman sitios de ácido de Lewis—centros pobres en electrones que atraen fuertemente a los iones hidroxilo. Con microscopía avanzada, técnicas de rayos X y espectroscopía, los investigadores confirmaron que los átomos de Cr se sitúan dentro de la red del sulfuro de níquel y la encogen y distorsionan sutilmente, cambiando la distribución electrónica. En condiciones de reacción, los sitios de cromo actúan como pequeñas bombas: capturan OH⁻ y luego lo "derraman" hacia los sitios vecinos de níquel, donde tiene lugar la oxidación de la urea. Mediciones in situ por Raman e infrarrojo, así como experimentos con etiquetado isotópico, trazaron directamente este derrame de hidroxilo de Cr a Ni y mostraron que acelera la formación de sitios activos de oxihidróxido de níquel (NiOOH) que impulsan la química deseada.
Altos rendimientos, menor energía y buena estabilidad
Porque el OH⁻ se entrega de forma eficiente a los lugares adecuados, el catalizador Cr–Ni₃S₂ convierte la urea a nitrito con una selectividad notable. A densidades de corriente relevantes para la industria, alcanza un rendimiento de nitrito de aproximadamente 121 miligramos por hora por centímetro cuadrado con eficiencias farádicas para nitrito por encima del 80 %, manteniendo la evolución de oxígeno competidora por debajo del 1,5 %. El catalizador se mantiene estable durante cientos de horas de operación continua con una lixiviación de cromo despreciable. El mismo material también reduce drásticamente el voltaje necesario cuando se empareja con un cátodo productor de hidrógeno en un dispositivo de electrólisis asistida por urea, rebajando el coste eléctrico de producir hidrógeno a unos 3,7 kilovatios-hora por metro cúbico de H₂—menos que la electrólisis alcalina convencional. Un análisis tecnoeconómico sugiere que, a 400 miliamperios por centímetro cuadrado, procesar una tonelada de urea en este sistema podría generar del orden de 1.200 dólares de valor neto cuando se contabilizan tanto el nitrito como el hidrógeno.
De la celda de laboratorio a dispositivos energéticos prácticos
Para demostrar el potencial en el mundo real, los autores construyeron una celda de flujo para electrólisis continua asistida por urea y una batería Zn–urea–aire. En la batería, reemplazar la habitual reacción de evolución de oxígeno durante la carga por la reacción de oxidación de urea redujo la tensión de carga en casi 0,3 voltios manteniendo un rendimiento estable por más de 100 horas. Esto significa que el dispositivo puede tanto depurar corrientes con urea como ofrecer almacenamiento eléctrico con mayor eficiencia energética. La misma estrategia de diseño basada en ácidos de Lewis también funcionó con otros metales como estaño y titanio, o con un anfitrión distinto como el sulfuro de cobre, lo que sugiere que el enfoque es ampliamente aplicable.
Una idea simple detrás de una reacción compleja
Para no especialistas, la idea clave es que los investigadores han aprendido a guiar dónde y cómo aterriza y se mueve un ingrediente reactivo común—el hidroxilo—en la superficie de un catalizador. Al añadir sitios de cromo que actúan como fuertes atractores y relevo para OH⁻, facilitan que las moléculas de urea se partan en nitrito en lugar de quemarse completamente a gas nitrógeno. Al mismo tiempo, esta vía requiere menos energía eléctrica y produce de forma natural hidrógeno. En esencia, el trabajo muestra que un diseño cuidadoso a escala atómica de los "patrones de tráfico" en el catalizador puede convertir las aguas residuales en una fuente tanto de productos químicos como de energía limpia.
Cita: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Palabras clave: oxidación de urea, producción de nitrito, generación de hidrógeno, electrocatalisis, valorización de aguas residuales