Clear Sky Science · es
Un atlas multi-ómico integrado revela la jerarquía de las redes regulatorias espaciotemporales de la gastrulación en ratón
Cómo un embrión construye su plano corporal
Cualquier mamífero, incluidos los humanos, empieza la vida como una pequeña bola de células que debe organizarse rápidamente en un cuerpo complejo con cabeza, cola, dorso, vientre y órganos internos. Esta transformación dramática ocurre durante una ventana breve llamada gastrulación. El artículo resumido aquí construye un mapa detallado y multinivel de este proceso en embriones de ratón, mostrando cómo genes, interruptores del ADN y señales químicas interactúan en espacio y tiempo para guiar a las células hacia sus destinos futuros.
Observando a miles de células tomar sus decisiones
Para seguir la gastrulación en acción, los investigadores analizaron más de 35.000 células individuales de embriones de ratón en cinco estadios estrechamente espaciados, desde la gastrulación temprana hasta la tardía. Para cada célula midieron no solo qué genes estaban activos, sino también qué regiones del ADN estaban abiertas y accesibles, indicio de que pueden actuar como interruptores regulatorios. Con estos datos identificaron 31 tipos celulares distintos y trazaron cómo las células tempranas y flexibles se ramifican progresivamente en las tres capas germinales principales —ectodermo, mesodermo y endodermo— que eventualmente forman todos los tejidos y órganos. También desarrollaron un nuevo método computacional, BioCRE, para conectar con mayor precisión a los genes con sus elementos de control en el ADN, revelando que muchos interruptores importantes se sitúan lejos de los genes que regulan.
Construyendo un atlas molecular 3D en el espacio real del embrión
La mayoría de los métodos de célula única pierden la posición original de cada célula en el embrión, pero la localización es crítica para comprender la patronización. El equipo superó esto alineando sus datos de célula única con un mapa tridimensional existente de la actividad génica en embriones de ratón. El resultado es ST-MAGIC, un “embrión digital” en el que cada pequeña ubicación está anotada con los probables tipos celulares presentes, los genes que expresan y la accesibilidad del ADN circundante. Este atlas muestra, por ejemplo, cómo distintos subtipos de mesodermo —los futuros corazón, músculo y tejidos de soporte— emergen en regiones diferenciadas y cómo genes de expresión amplia como Otx2 utilizan elementos regulatorios diferentes en la superficie externa del embrión (epiblasto) y en la interna (endodermo visceral).
Cuando se rompe la simetría y el lado izquierdo se diferencia del derecho
Una característica llamativa de los planos corporales es que el lado izquierdo y el derecho no son idénticos —piénsese en el corazón situado ligeramente a la izquierda. Los autores usaron su atlas espacial para acercarse al mesodermo lateral, donde aparecen por primera vez las diferencias izquierda–derecha. Encontraron asimetrías sutiles pero consistentes en qué tipos celulares se enriquecen en cada lado y en qué regiones del ADN están más abiertas. En el lado derecho, las regiones vinculadas a una vía de señalización de crecimiento llamada BMP eran más accesibles; en el izquierdo, se favorecían regiones asociadas con genes necesarios para formar segmentos y estructuras cardíacas. Algunos de estos elementos del ADN, incluidos recién descubiertos que regulan el gen Lefty2, se abren antes de que aparezcan diferencias visibles en la expresión génica, lo que sugiere que un “preparado” temprano del paisaje cromatínico prepara a cada lado del embrión para interpretar las señales de forma distinta.
Un relevo de factores guía la línea media del cuerpo
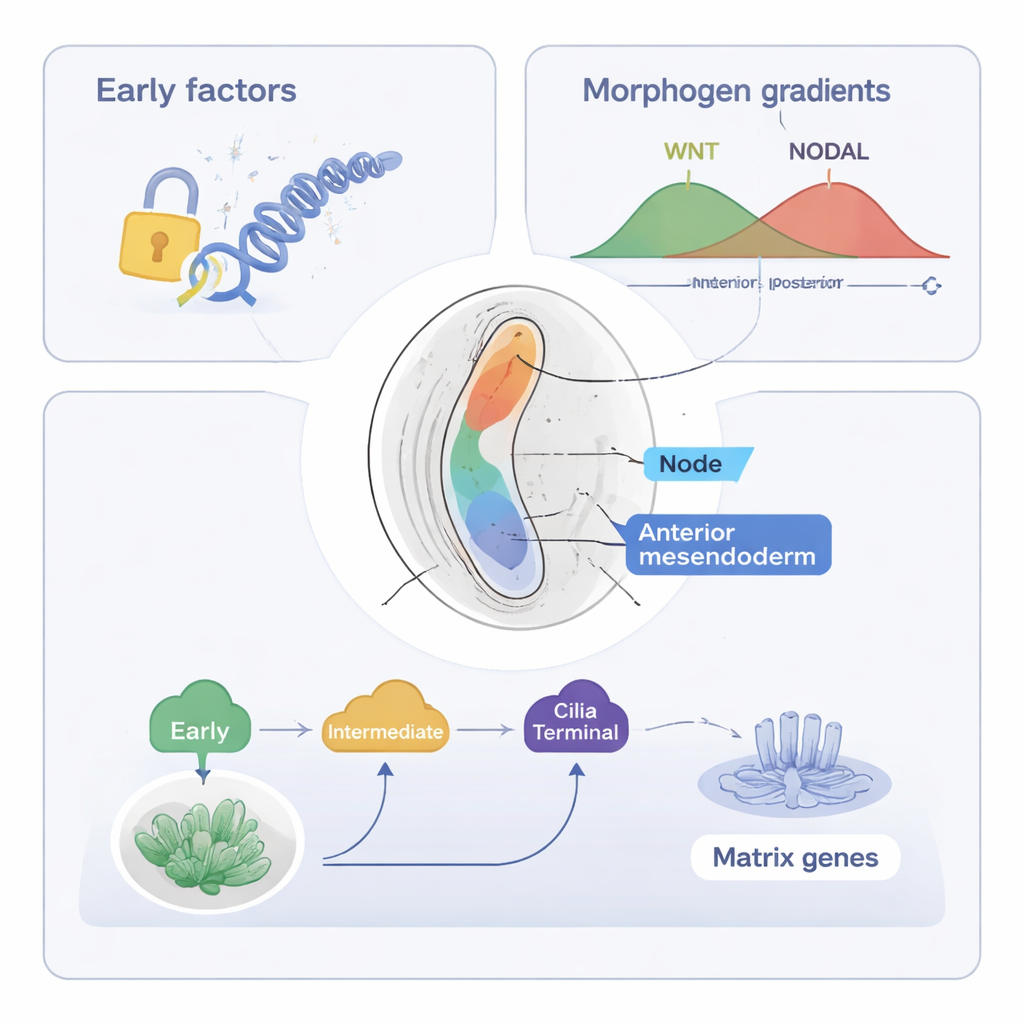
El estudio se centra luego en el mesendodermo axial, una población de células que formará la notocorda —una estructura en forma de varilla a lo largo de la línea media que ayuda a organizar la columna vertebral y el sistema nervioso. Usando sus herramientas combinadas (ST-MAGIC y una versión ampliada llamada ST-MAGIC (+)), los autores siguieron cómo estas células surgen del nódulo primitivo anterior y se dividen en dos ramas: células del nodo, que construyen una estructura ciliada importante para la detección izquierda–derecha, y mesendodermo anterior, que contribuye a tejidos de la línea media. Descubrieron un relevo jerárquico de factores de transcripción —proteínas que controlan la actividad génica. Factores tempranos, como EOMES, y factores intermedios, incluidos FOXA2 y LHX1, abren primero regiones clave del ADN y establecen la capacidad de responder a señales principales como WNT y NODAL. Más tarde, factores “terminales” como NOTO, SOX9 y un factor recientemente implicado, POU6F1, activan programas génicos especializados, por ejemplo los necesarios para cilios o la matriz extracelular.
Señales, cromatina y especialistas de acción tardía
Al integrar conjuntos de datos públicos sobre dónde se unen al ADN los efectores de las señales WNT y NODAL, los autores mostraron que la capacidad del embrión para responder a estas señales cambia en el espacio antes de que las propias fuentes de señal se desplacen. En la región preparada para convertirse en mesendodermo axial, los sitios del ADN sensibles a NODAL y WNT se abren temprano, y muchos contienen motivos para FOXA2, Zfp281 y otros reguladores, lo que sugiere control cooperativo. La eliminación experimental de los factores de acción tardía NOTO y POU6F1 en ratón perturbó la expresión de genes específicos del nodo y relacionados con cilios y acortó los cilios del nodo, sin embargo, el paisaje de ADN abierto subyacente permaneció en gran parte intacto. Esto indica que factores tempranos establecen la base epigenética, mientras que los factores tardíos refinan principalmente la expresión génica sin remodelar la cromatina.
Por qué esto importa para entender el desarrollo
Para un no especialista, este trabajo puede verse como la construcción de un “diagrama de cableado” de alta resolución sobre cómo un embrión dispone su plano corporal. Los autores muestran que las decisiones de destino celular durante la gastrulación están gobernadas no solo por qué señales están presentes, sino también por cuándo y dónde se abren los interruptores del ADN y por qué factores de transcripción actúan en secuencia. Sus atlas ST-MAGIC y ST-MAGIC (+) proporcionan un recurso para explorar estas relaciones a través del espacio y del tiempo, ofreciendo un marco que podría informar estudios sobre defectos congénitos, modelos embrionarios basados en células madre y, eventualmente, aspectos del desarrollo humano.
Cita: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Palabras clave: gastrulación, redes regulatorias génicas, multi-ómica a nivel de célula única, patronización del embrión, desarrollo del ratón