Clear Sky Science · es
La autoinhibición inter‑monómero de HEXIM1 gobierna la especificidad de unión al ARN 7SK y la inactivación de P‑TEFb
Por qué este pequeño ARN importa para el control génico
Cada célula debe decidir cuándo activar y desactivar genes, y lo hace controlando cuidadosamente una enzima que impulsa la producción de ARN. Este artículo desvela cómo una pequeña proteína llamada HEXIM1, que actúa junto con un ARN no codificante llamado 7SK, funciona como un seguro sobre esa enzima. Entender este sistema molecular de seguridad ayuda a explicar cómo nuestras células evitan una actividad génica descontrolada y también arroja luz sobre cómo virus como el VIH secuestran la misma maquinaria.
Un freno molecular sobre la expresión génica
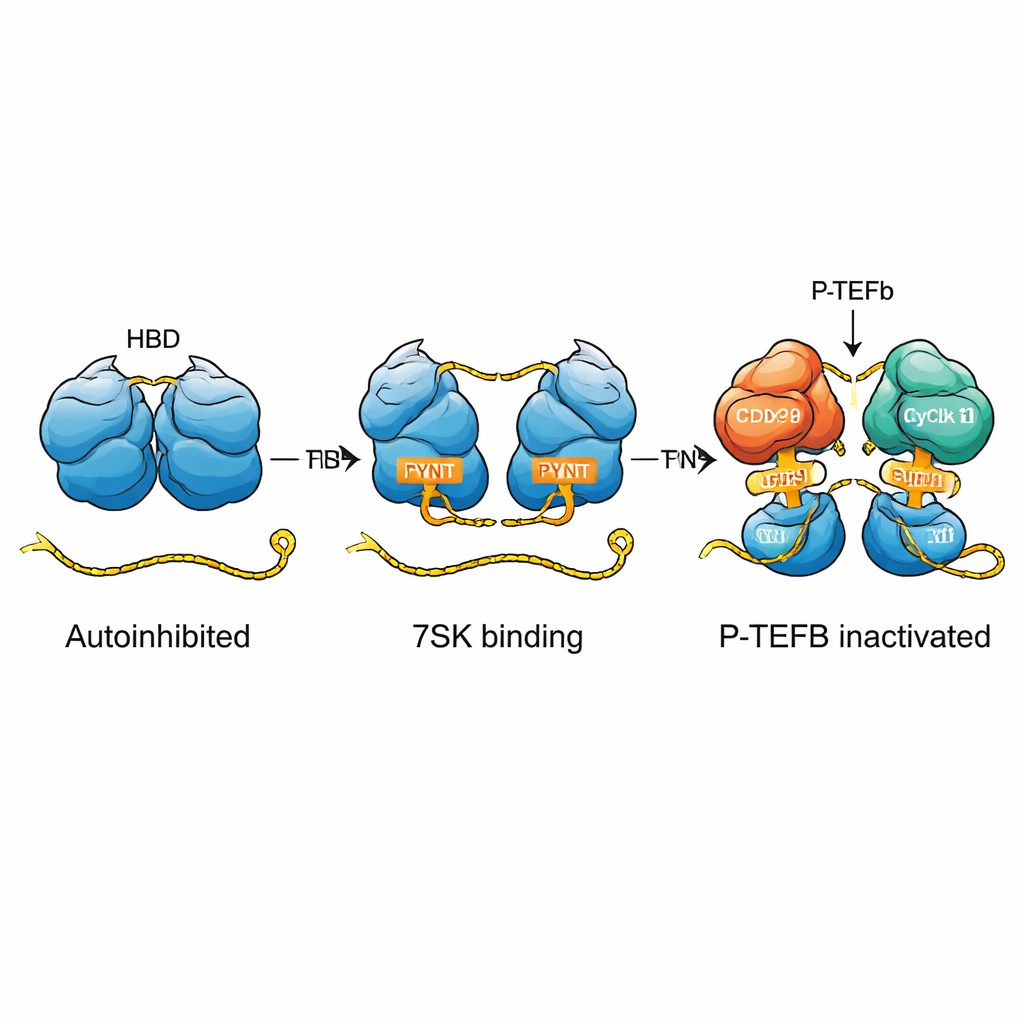
En células humanas, un paso clave de la expresión génica está controlado por un factor llamado P‑TEFb, que ayuda a la ARN polimerasa II a pasar de un estado detenido a una transcripción a toda velocidad. Las proteínas HEXIM, en particular HEXIM1, son centrales para mantener a P‑TEFb bajo control. Lo hacen dentro de un complejo grande llamado RNP 7SK, construido alrededor del ARN 7SK. Cuando HEXIM1 y 7SK se asocian, aíslan a P‑TEFb para que no pueda impulsar la transcripción. Hasta ahora, la pieza que faltaba era cómo HEXIM1 evita por sí misma captar a P‑TEFb antes de tiempo y cómo el ARN 7SK convierte a HEXIM1 de un estado inactivo a un inhibidor activo en el momento adecuado.
Una proteína que se ‘‘abraza’’ a sí misma y queda controlada
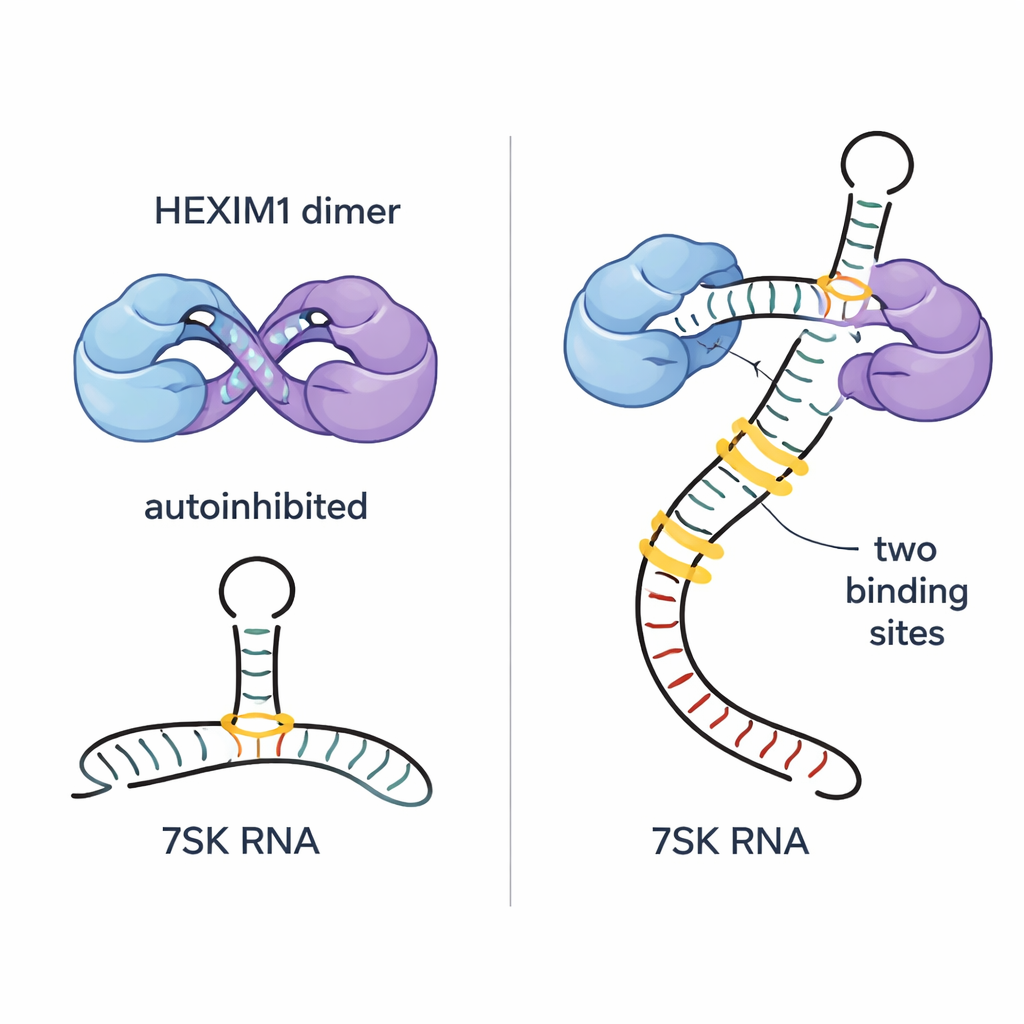
Los autores muestran que HEXIM1 forma naturalmente un dímero —dos cadenas proteicas idénticas emparejadas— y que las partes centrales flexibles de cada cadena se entrelazan en una disposición de ‘‘autoabrazo’’. En este estado, un segmento corto crucial llamado motivo PYNT, que normalmente se une y silencia la quinasa P‑TEFb, queda escondido en la interfaz entre las dos cadenas. Usando métodos sensibles de RMN y técnicas biofísicas, el equipo mapeó cómo regiones básicas (con carga positiva) y ácidas (con carga negativa) de los dos monómeros interactúan para crear este dímero autoinhibido. Esta restricción incorporada evita que HEXIM1 clampée al azar sobre P‑TEFb cuando el ARN 7SK no está presente.
Cómo desbloquea el ARN 7SK a HEXIM1
El ARN 7SK contiene varias características estructurales, incluida una larga región en tallo‑bucle llamada SL1. Al diseccionar este ARN en fragmentos más pequeños y seguir cambios sutiles en señales de RMN, los investigadores identificaron cinco posibles sitios de unión de HEXIM1 a lo largo de SL1. Dos de estos sitios destacan como puntos de acoplamiento de alta afinidad; ambos comparten una sección de doble hélice rica en A–U y una protuberancia rica en U cercana que puede formar interacciones especiales de tres bases. El equipo encontró que cada mitad del dímero HEXIM1 se une a uno de estos dos sitios fuertes en el ARN 7SK lineal. Cuando ambos sitios están ocupados, la región central de HEXIM1 se reorganiza, rompiendo los contactos del autoabrazo y exponiendo los motivos PYNT ocultos, preparando efectivamente a la proteína para capturar P‑TEFb.
Elegir la forma correcta del ARN — y evitar las incorrectas
El ARN 7SK no existe en una sola conformación; puede alternar entre una forma lineal, que presenta ambos sitios de alta afinidad, y una forma más circular con solo un sitio adecuado. Los autores muestran que la autoinhibición de HEXIM1 lo hace sorprendentemente exigente: el dímero se une débilmente a sitios individuales por sí solos, pero mucho más fuertemente y de forma cooperativa al segmento lineal completo SL1 que ofrece ambos sitios fuertes. Este requisito de doble sitio evita que HEXIM1 quede atrapado en ARNs aleatorios en otras partes de la célula y hace que su unión sea altamente específica para la conformación lineal de 7SK que ensambla el complejo represor activo. También demuestran que añadir cargas negativas cerca de la región de unión al ARN (imitando la fosforilación en una serina clave) debilita la unión al ARN sin romper completamente la autoinhibición, un posible mecanismo por el que las células liberan P‑TEFb cuando lo necesitan.
Del interruptor molecular al impacto celular
En conjunto, el estudio revela a HEXIM1 como un interruptor molecular finamente ajustado. En su estado de reposo, ‘‘autoabrazo’’, mantiene ocultos sus segmentos PYNT bloqueadores de P‑TEFb. Solo cuando encuentra ARN 7SK lineal con dos sitios de unión correctamente dispuestos la proteína cambia a un estado ‘‘activo’’, exponiendo esos segmentos para poder capturar e inactivar P‑TEFb —a menudo dos copias a la vez. Este mecanismo explica cómo las células usan un ARN pequeño y una proteína flexible para imponer un control preciso sobre la transcripción y aporta un marco más claro para entender cómo señales celulares, modificaciones químicas o proteínas virales como HIV Tat pueden inclinar la balanza entre la expresión génica detenida y la activa.
Cita: Yang, Y., Murrali, M.G., Galvan, S. et al. HEXIM1 inter-monomer autoinhibition governs 7SK RNA binding specificity and P-TEFb inactivation. Nat Commun 17, 1570 (2026). https://doi.org/10.1038/s41467-026-68285-8
Palabras clave: regulación de la transcripción, ARN 7SK, HEXIM1, P‑TEFb, HIV Tat