Clear Sky Science · es
Variantes de novo en el gen del factor de empalme SF3B1 se asocian con trastornos del neurodesarrollo
Cuando un gen altera el plano temprano del cerebro
¿Por qué algunos niños desarrollan dificultades de aprendizaje, convulsiones o problemas para alimentarse aun cuando el embarazo y el parto transcurren con normalidad? Este estudio examina un único gen, llamado SF3B1, que ayuda a las células a procesar los mensajes genéticos. Los investigadores muestran que cambios nuevos y espontáneos en este gen pueden desordenar de forma sutil cómo las células cerebrales leen las instrucciones del ADN, dando lugar a un síndrome del neurodesarrollo hasta ahora no reconocido.
Un editor maestro de los mensajes genéticos
Todas las células de nuestro cuerpo deben convertir el texto genético en bruto en instrucciones claras antes de poder fabricar proteínas. Este paso de edición, conocido como empalme de ARN, elimina segmentos no codificantes y une las piezas útiles. SF3B1 es un componente central de la “máquina” celular de empalme. Hasta ahora, las alteraciones en SF3B1 se conocían sobre todo por su papel en el cáncer, donde las células tumorales adquieren mutaciones en este gen a lo largo de la vida. El nuevo trabajo plantea otra pregunta: ¿qué sucede cuando un cambio dañino en SF3B1 está presente desde la concepción en todas las células del cuerpo?
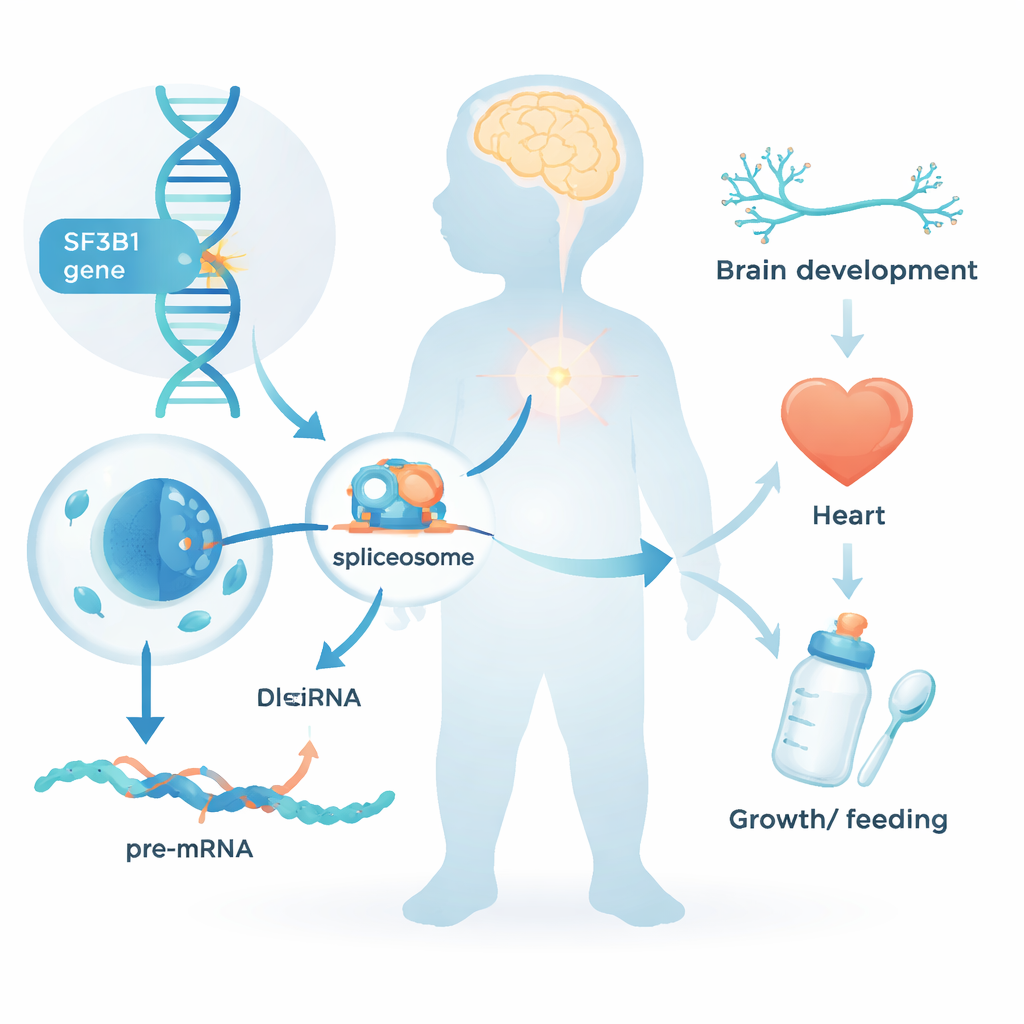
Un síndrome infantil recién reconocido
El equipo recopiló datos de 26 niños y adultos jóvenes que portaban variantes raras de SF3B1, en su mayoría surgidas de novo —es decir, no heredadas de ninguno de los padres. Casi todos presentaban problemas del neurodesarrollo: retrasos para sentarse, caminar o hablar; discapacidad intelectual, en su mayoría de grado leve a moderado; y, en alrededor de la mitad de los casos, convulsiones. Muchos mostraban hipotonía y necesitaban ayuda adicional para alimentarse, a veces mediante sonda gástrica. Las facciones faciales eran sutilmente atípicas pero no idénticas entre unos y otros; una característica sorprendentemente común fue un paladar alto o hendido. Varios participantes también tenían malformaciones cardíacas, retraso del crecimiento o microcefalia, lo que indica que el impacto de las alteraciones de SF3B1 va más allá del cerebro.
Dos clases de cambios genéticos, dos patrones clínicos
Los investigadores distinguieron entre dos tipos amplios de variantes en SF3B1. Un grupo incluía cambios de “pérdida de función”, como señales de paro prematuro, que se espera reduzcan la cantidad de proteína SF3B1 funcional. El segundo grupo contenía variantes missense, en las que se altera un único aminoácido en la proteína. Al agrupar las características clínicas de los niños, el equipo observó que aquellos con variantes missense tendían a presentar problemas más graves y complejos, incluyendo una mayor tasa de anomalías cardíacas y gastrointestinales, estatura baja y microcefalia. Las variantes de pérdida de función, en contraste, a veces se heredaban de un progenitor con afectación leve o incluso aparentemente sano, lo que sugiere que tener menos SF3B1 puede ser compatible con síntomas relativamente moderados en algunas personas.
Errores de afinado fino más que un colapso completo
Para entender qué hacen las variantes missense dentro de las células, los científicos recrearon esas variantes en líneas celulares de laboratorio. Sorprendentemente, estas proteínas SF3B1 alteradas aún podían desempeñar la función básica de empalme lo bastante bien como para rescatar a células en las que se había silenciado el SF3B1 normal. Esto descartó una explicación simple de pérdida de función. Mediante secuenciación profunda de ARN, el equipo examinó luego el conjunto completo de mensajes celulares. Encontraron que las variantes missense desplazaban sutilmente el empalme de cientos de genes, especialmente cambiando qué sitios de empalme se elegían en los extremos de los exones y provocando, en ocasiones, el salto de exones. La magnitud de la alteración fue menor que la observada con la clásica mutación asociada al cáncer SF3B1 K700E, pero aún así fue significativa: muchos genes afectados participan en el desarrollo cerebral, la conectividad neuronal y procesos fundamentales como el manejo del ARN y la síntesis de proteínas.
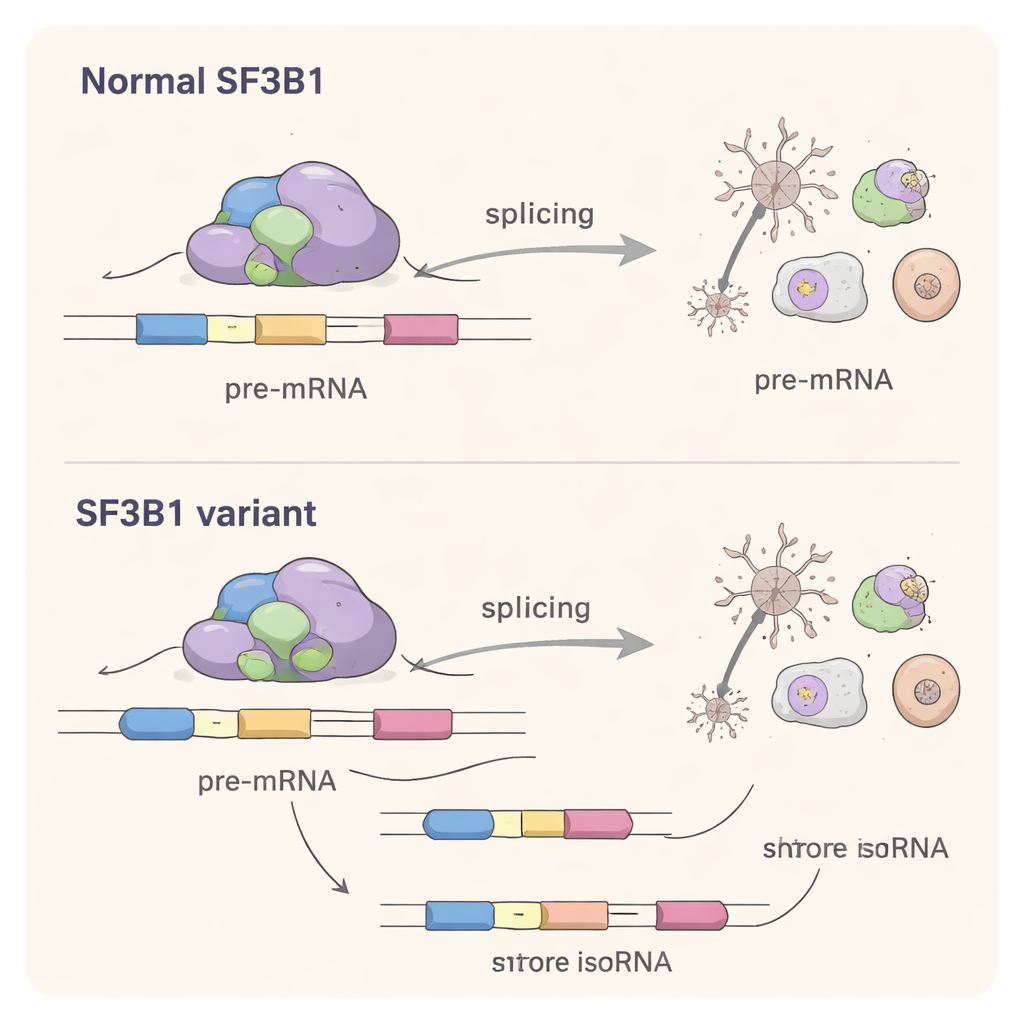
Un mecanismo compartido entre el cáncer y los trastornos cerebrales
Aunque la mayoría de las variantes de SF3B1 vinculadas al neurodesarrollo ocurren en posiciones distintas a las bien conocidas mutaciones asociadas al cáncer, perturban el mismo proceso central: el reconocimiento preciso de los sitios de empalme en el ARN. El estudio muestra que estas variantes del desarrollo tienen su propia “firma de empalme”, eligiendo sitios alternativos que a menudo están más cerca de los normales que los favorecidos en el cáncer. Esto sugiere un mecanismo de cambio de función, en el que la proteína mutada compite con la copia normal y empuja a la maquinaria de empalme hacia decisiones ligeramente erróneas en muchos genes a la vez.
Qué significa esto para las familias y la investigación futura
Para las familias afectadas, el trabajo identifica a SF3B1 como una nueva causa de trastornos del neurodesarrollo que ahora puede ser analizada en consultas genéticas, potencialmente poniendo fin a búsquedas diagnósticas prolongadas. Más ampliamente, añade a SF3B1 a una lista pequeña pero creciente de genes de empalme cuyas alteraciones pueden impulsar tanto el cáncer como los trastornos cerebrales infantiles, según cuándo y cómo se modifique el gen. Al cartografiar cómo variantes específicas de SF3B1 remodelan el empalme del ARN, el estudio sienta las bases para futuras terapias dirigidas a corregir los errores de empalme de forma precisa.
Cita: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Palabras clave: Empalme de ARN, SF3B1, Trastornos del neurodesarrollo, Variantes de novo, Espliceosomopatías