Clear Sky Science · es
Hidrogel viscoelástico que prepara macrófagos CAR para el tratamiento de la fibrosis pulmonar
Convertir a los «conserjes» del cuerpo en equipos de reparación de precisión
La fibrosis pulmonar es una enfermedad devastadora en la que el tejido pulmonar normal y elástico se reemplaza lentamente por una cicatriz rígida. Las personas tienen dificultades para respirar y, hoy por hoy, los fármacos en su mayoría solo frenan el deterioro. Este estudio explora una idea nueva: convertir las propias células limpiadoras del cuerpo, los macrófagos, en «conserjes inteligentes» y potenciar su capacidad con un gel blando especialmente diseñado. Juntos, estos enfoques ayudan a las células a localizar a los culpables que forman la cicatriz e incluso a aflojar el tejido rígido en pulmones dañados.
Cuando la curación se vuelve perjudicial
En pulmones sanos, los fibroblastos mantienen la delicada red de colágeno que sostiene los alvéolos. En la fibrosis pulmonar, estas células se vuelven hiperactivas y depositan gruesas hebras de colágeno que obstruyen los espacios aéreos. Los tratamientos actuales pueden atenuar estos procesos pero rara vez los revierten. Los autores se centran en una bandera de superficie celular llamada proteína de activación de fibroblastos (FAP), que es abundante en fibroblastos hiperactivos pero escasa en el tejido normal. Si las células inmunitarias pudieran aprender a reconocer la FAP, podrían eliminar selectivamente a los fibroblastos «desbocados» que impulsan la cicatrización, preservando a las células sanas a su alrededor.
Reprogramar macrófagos para atacar a los constructores de cicatriz
Los macrófagos son células inmunitarias nómadas que normalmente fagocitan células muertas, microbios y restos celulares. El equipo las equipó con un receptor de antígeno quimérico (CAR) que reconoce la FAP, creando macrófagos CAR (CAR‑Ms). En placas de laboratorio, estos CAR‑Ms engulleron de forma eficiente fibroblastos ricos en FAP y los eliminaron, mientras que en gran medida ignoraron células con baja expresión de FAP. También degradaron geles ricos en colágeno más vigorosamente que macrófagos no modificados, lo que sugiere un doble beneficio: eliminar las células que crean la cicatriz y descomponer directamente la matriz cicatricial. Estos efectos se observaron tanto en líneas celulares estándar como en macrófagos primarios de ratón, que se acercan más a la situación real en tejidos. 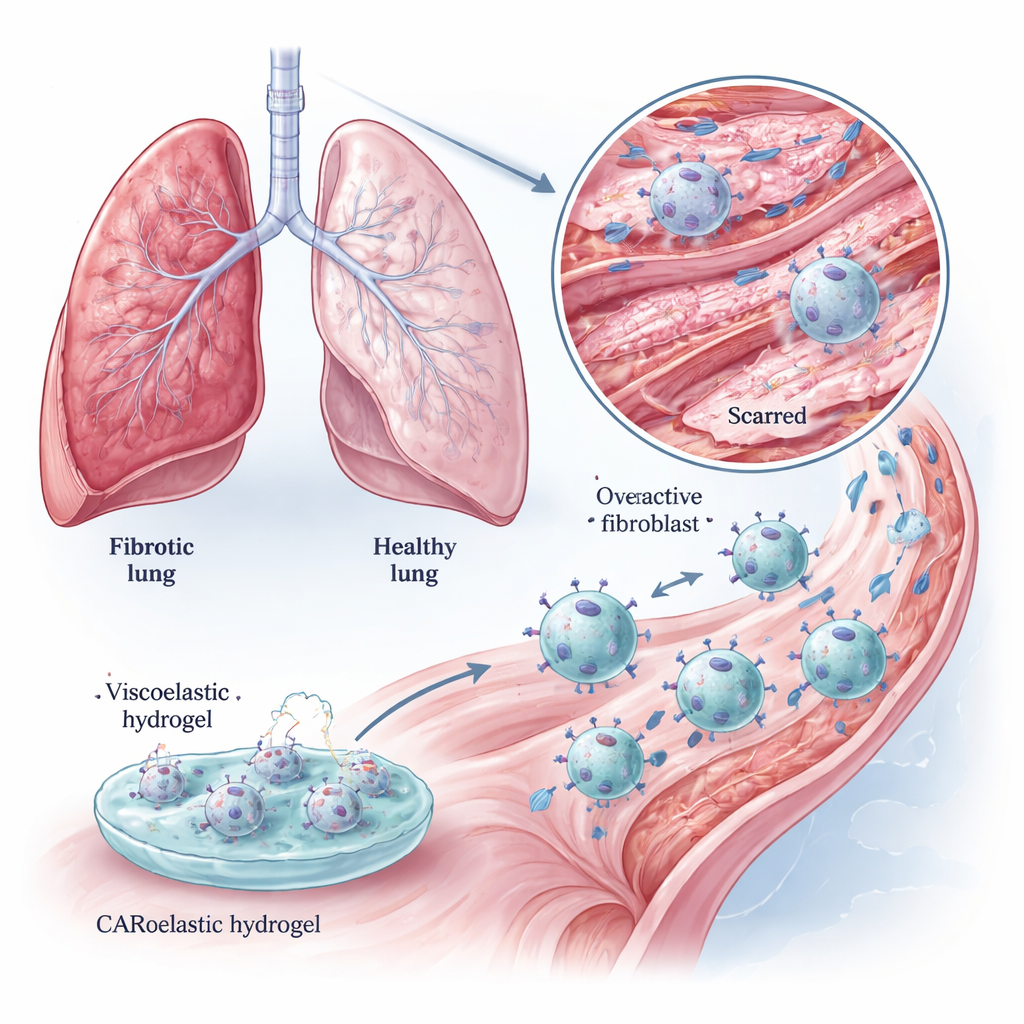
Preparar las células inmunitarias con un gel blando y viscoelástico
La ingeniería genética celular es potente pero compleja. Por ello, los investigadores preguntaron si una señal puramente física —un hidrogel blando y viscoelástico— podría ajustar adicionalmente el comportamiento de los CAR‑M. Construyeron un hidrogel de gelatina‑alginato cuyo "módulo de pérdida", una medida de cómo se relaja lentamente bajo esfuerzo, podía ajustarse finamente sin cambiar la rigidez global. Cuando los CAR‑Ms se cultivaron brevemente sobre geles con la viscoelasticidad adecuada, su capacidad para matar fibroblastos objetivo aumentó más que con estimulantes químicos habituales, y el impulso duró al menos dos días. Estos “Gel‑CAR‑Ms” también activaron genes vinculados a la activación inmune y a la remodelación tisular, mientras redujeron la expresión de genes asociados con la fibrosis, lo que sugiere que la experiencia con el gel imprimió en las células una identidad más antifibrotica.
Cómo una superficie más blanda reconfigura el comportamiento celular
Para entender por qué el gel era importante, el equipo examinó el estado físico de los receptores CAR en la superficie celular. Una sonda fluorescente reveló que los CAR‑Ms preparados en hidrogel tenían menor tensión de membrana: la «piel» exterior de la célula estaba más relajada. En estas condiciones, las moléculas CAR se dispersaron desde racimos apretados hacia unidades más aisladas y pares. Ensayos bioquímicos mostraron que estos receptores dispersos favorecían conformaciones que desencadenaban con mayor facilidad la señalización interna, especialmente a través de vías como ERK que controlan la activación y la capacidad citotóxica. Imitar la caída de tensión con una pequeña molécula reprodujo la misma dispersión de receptores y mejoró la eliminación de células diana, lo que respalda la idea de que la relajación mecánica de la membrana es suficiente para “prearmar” las células antes de que encuentren sus objetivos. 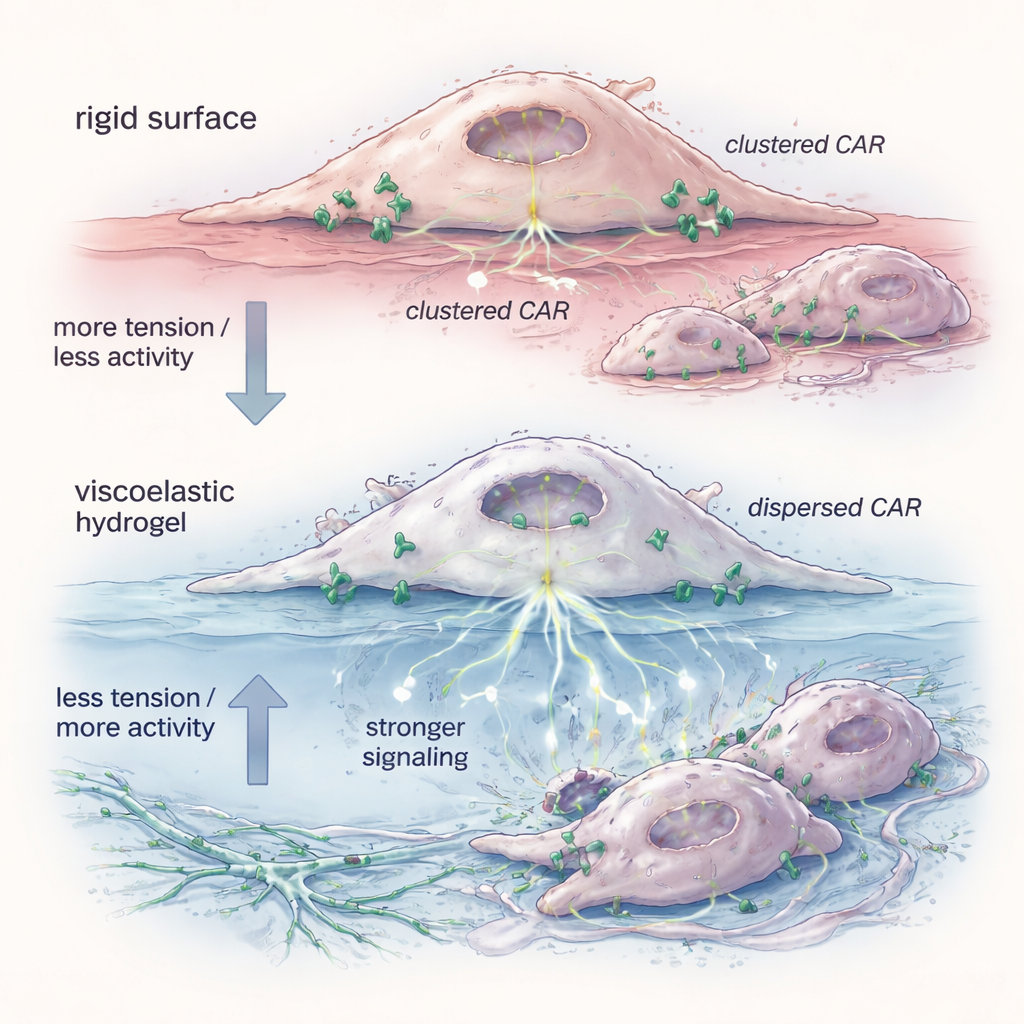
Reparando pulmones cicatrizados en ratones
La prueba definitiva fue un modelo murino de fibrosis pulmonar inducida por fármaco. Los animales recibieron macrófagos sin modificar, CAR‑Ms estándar o Gel‑CAR‑Ms preparados en hidrogel. Todos los ratones tratados mejoraron en comparación con los controles no tratados, pero los Gel‑CAR‑Ms se desempeñaron mejor: sus pulmones contenían menos colágeno, más espacios aéreos normales y menos fibroblastos positivos para FAP. Los análisis génicos del tejido pulmonar mostraron que los Gel‑CAR‑Ms atenuaron las señales inflamatorias y redujeron la expresión de genes relacionados con la cicatriz más eficazmente que los CAR‑Ms estándar. Las células rastreadas persistieron en el pulmón al menos una semana, y controles de seguridad extendidos hasta 12 semanas no revelaron daños orgánicos importantes, anomalías sanguíneas ni signos de autoinmunidad.
Una nueva dirección para las terapias celulares antifibróticas
Para no especialistas, el mensaje clave es que la combinación de ingeniería celular dirigida y materiales inteligentes puede convertir células inmunitarias innatas en herramientas altamente eficaces, sin una sobrecomplicación genética, para combatir la cicatrización. Al descansar brevemente macrófagos diseñados sobre un gel blando cuidadosamente ajustado, los investigadores «preajustaron» mecánicamente sus receptores de superficie a un modo más sensible. En ratones con fibrosis pulmonar, esto se tradujo en una mejor eliminación de fibroblastos nocivos, degradación del exceso de colágeno y restauración parcial de la estructura pulmonar normal, sin problemas de seguridad evidentes. Aunque queda mucho trabajo antes de ensayos en humanos, esta estrategia sugiere que afinar el entorno físico de las células terapéuticas podría algún día hacer los tratamientos para enfermedades fibróticas pulmonares más potentes y precisos.
Cita: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Palabras clave: fibrosis pulmonar, terapia con macrófagos CAR, hidrogel viscoelástico, proteína de activación de fibroblastos, mecano‑biología celular