Clear Sky Science · es
Base molecular para la inhibición de la metilación de novo del ADN por TCL1A
Cómo las células deciden qué recordar
Cada célula de su cuerpo contiene esencialmente el mismo ADN, sin embargo las neuronas, las células sanguíneas y las células de la piel se comportan de forma muy distinta. Una manera en que las células «recuerdan» su identidad es mediante etiquetas químicas añadidas al ADN, un proceso llamado metilación del ADN. Este estudio revela, con detalle atómico, cómo una pequeña proteína llamada TCL1A puede apagar las enzimas que escriben esas marcas de metilo. Dado que tanto la metilación del ADN como TCL1A están vinculados al cáncer y a trastornos reproductivos, comprender esta lucha molecular podría, en última instancia, inspirar nuevas terapias.
La maquinaria de etiquetado del ADN de la célula
La metilación del ADN funciona como una marca a lápiz en los márgenes del genoma, ayudando a silenciar ciertos genes y a estabilizar el genoma durante el desarrollo celular. Dos enzimas, DNMT3A y DNMT3B, son las principales «escritoras» que colocan nuevas etiquetas de metilo durante el desarrollo temprano y cuando las células madre se especializan. Si estas enzimas están mutadas o mal reguladas, el patrón de marcas en el ADN puede desordenarse, contribuyendo a síndromes del desarrollo y a cánceres hematológicos. TCL1A es una proteína conocida por su papel en los cánceres de células inmunitarias, donde con frecuencia se sobreproduce. Trabajos previos sugerían que TCL1A puede unirse a DNMT3A y DNMT3B y atenuar su actividad, pero nadie sabía exactamente cómo lograba ese bloqueo.
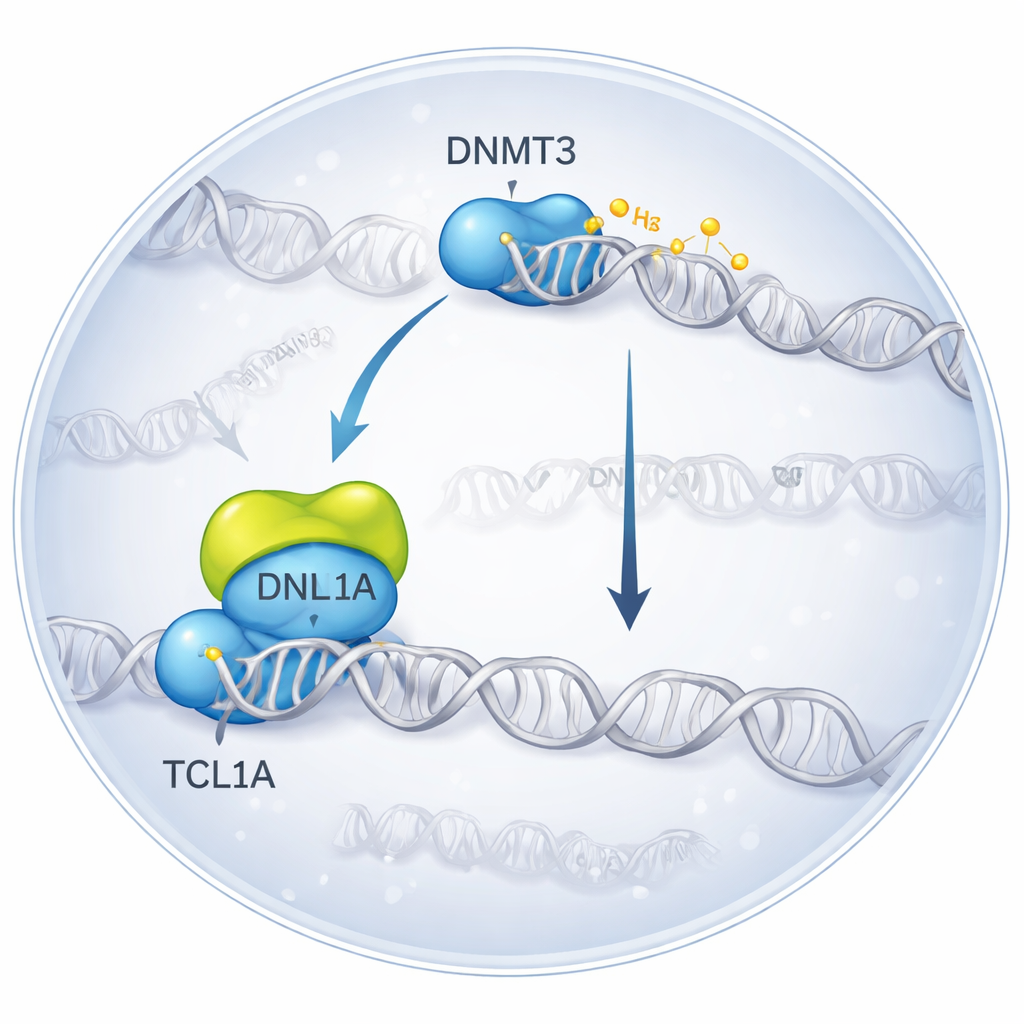
Congelando un encuentro molecular en 3D
Los investigadores usaron criomicroscopía electrónica, una técnica que toma imágenes de moléculas congeladas al instante, para visualizar el complejo formado cuando DNMT3A se une a TCL1A. Encontraron que dos moléculas de DNMT3A se emparejan, y a cada lado un dímero de TCL1A se acopla sobre la porción catalítica de DNMT3A—la misma región que normalmente interacciona con proteínas auxiliares y con el ADN. Esta superficie de unión se solapa con el lugar donde otro socio, DNMT3L, suele engancharse para potenciar la actividad de DNMT3A. En pruebas bioquímicas, añadir TCL1A redujo drásticamente la capacidad de metilar ADN tanto de DNMT3A como de DNMT3B, incluso en presencia de DNMT3L, lo que confirma que el complejo estructural corresponde a un estado fuertemente inhibido.
Un cambio de forma que atasca la enzima
Al observar con más detalle, el equipo vio que la unión de TCL1A no se limita a cubrir el sitio activo como una tapa. En su lugar, desencadena un cambio sutil pero de gran alcance en la conformación de DNMT3A. Dos regiones flexibles de la enzima, conocidas como el lazo de reconocimiento del objetivo y el lazo catalítico, se desplazan respecto a las posiciones que ocupan cuando DNMT3A está unida al ADN. En la forma activa, estos lazos se recuestan contra el ADN y forman un bolsillo para una pequeña molécula combustible llamada SAM, que dona el grupo metilo. Con TCL1A adherida, el lazo catalítico se pliega dentro del bolsillo de SAM y lo bloquea, dificultando además que el ADN alcance la enzima. Mediciones de unión confirmaron que DNMT3A asociado a TCL1A ya no puede unirse de forma detectable ni al ADN ni a SAM.
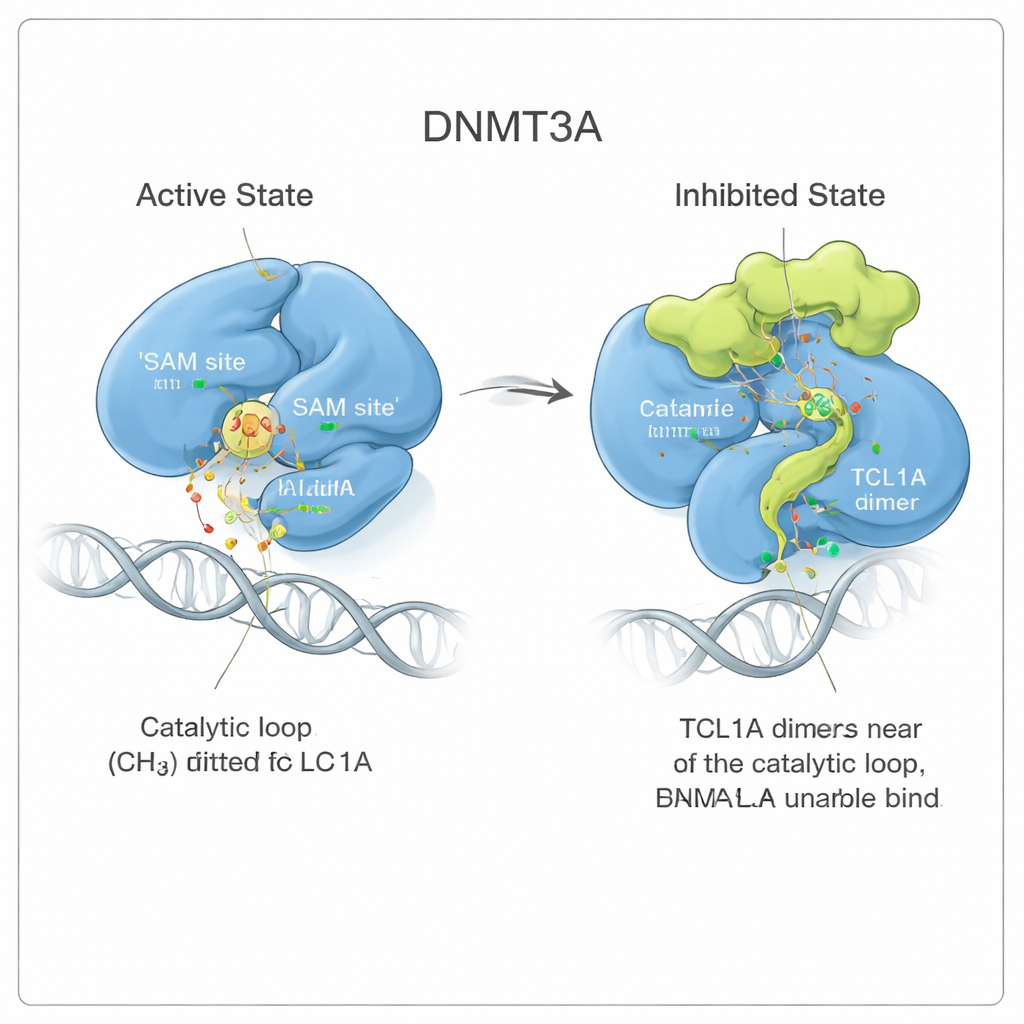
Observando un bloqueo dinámico en movimiento
Para entender cuán estable es esta conformación inhibida, los autores realizaron largas simulaciones de dinámica molecular, esencialmente películas basadas en física de las moléculas en solución. Cuando DNMT3A estaba unida a su activador DNMT3L, el lazo catalítico permanecía firme en su posición activa. Cuando TCL1A estaba presente, ese lazo se volvió mucho más móvil, aleteando pero ocupando repetidamente el bolsillo de SAM como algas marinas que giran y aun así obstruyen un desagüe. Este movimiento constante redujo el espacio disponible para SAM más de diez veces, apoyando un modelo en el que TCL1A explota la flexibilidad natural de DNMT3A para imponer una forma de inhibición dinámica, más que rígida.
Consecuencias para las células en desarrollo y la enfermedad
El equipo preguntó luego qué significa este bloqueo molecular para células reales. Diseñaron células madre embrionarias de ratón para que produjeran TCL1A humano durante una etapa en la que las células normalmente aumentan la metilación del ADN al comenzar a diferenciarse. El mapeo de la metilación a nivel del genoma mostró que las células que sobreexpresaban TCL1A no adquirieron el habitual alto nivel de metilación del ADN, pareciéndose mucho a las células en las que se eliminaron los genes Dnmt3a y Dnmt3b. Una versión mutante de TCL1A que se une pobremente a las enzimas DNMT3 tuvo poco efecto, subrayando que la interacción física es clave. Estos hallazgos vinculan el mecanismo estructural con amplios cambios epigenéticos en todo el genoma.
Qué significa esto para la salud
En conjunto, el trabajo revela cómo TCL1A puede actuar como un freno potente sobre las enzimas que colocan nuevas marcas de metilación en el ADN. Al acoplarse en una interfaz crítica, TCL1A repositiona los lazos flexibles de DNMT3A y DNMT3B de modo que ya no pueden unirse a su plantilla de ADN ni a su combustible químico, llevando a una pérdida global de marcas de metilo en las células. En el desarrollo normal, este tipo de control fino puede ayudar a equilibrar cuándo y dónde se añade la metilación. Cuando TCL1A está mal localizado o sobreproducido, como en ciertos cánceres hematológicos y en raros trastornos reproductivos, ese mismo mecanismo puede descarrilar el programa epigenético de la célula. Comprender esta interacción a resolución atómica abre la puerta al diseño de moléculas que imiten o contrarresten los efectos de TCL1A, potencialmente restaurando patrones saludables de metilación del ADN.
Cita: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Palabras clave: Metilación del ADN, DNMT3A, TCL1A, Epigenética, Cáncer