Clear Sky Science · es
Métodos de suministro de muestras para cristalografía de proteínas con rayos X con especial atención al consumo de muestra
Ver las moléculas en acción
La cristalografía de rayos X permite a los científicos ver la disposición de los átomos en las proteínas, las pequeñas máquinas que impulsan la vida. Un enfoque más reciente, denominado cristalografía serial, va un paso más allá: puede capturar “películas moleculares” de proteínas en acción, como enzimas procesando un fármaco o proteínas fotosintéticas dividiendo el agua. Pero hay un problema. Muchas proteínas importantes son difíciles de producir y cristalizar, y los experimentos actuales pueden consumir desde miligramos hasta gramos de material precioso. Este artículo de revisión plantea una pregunta aparentemente sencilla: ¿cómo podemos llevar cristales a haces de rayos X potentes desperdiciando la menor cantidad de muestra posible?
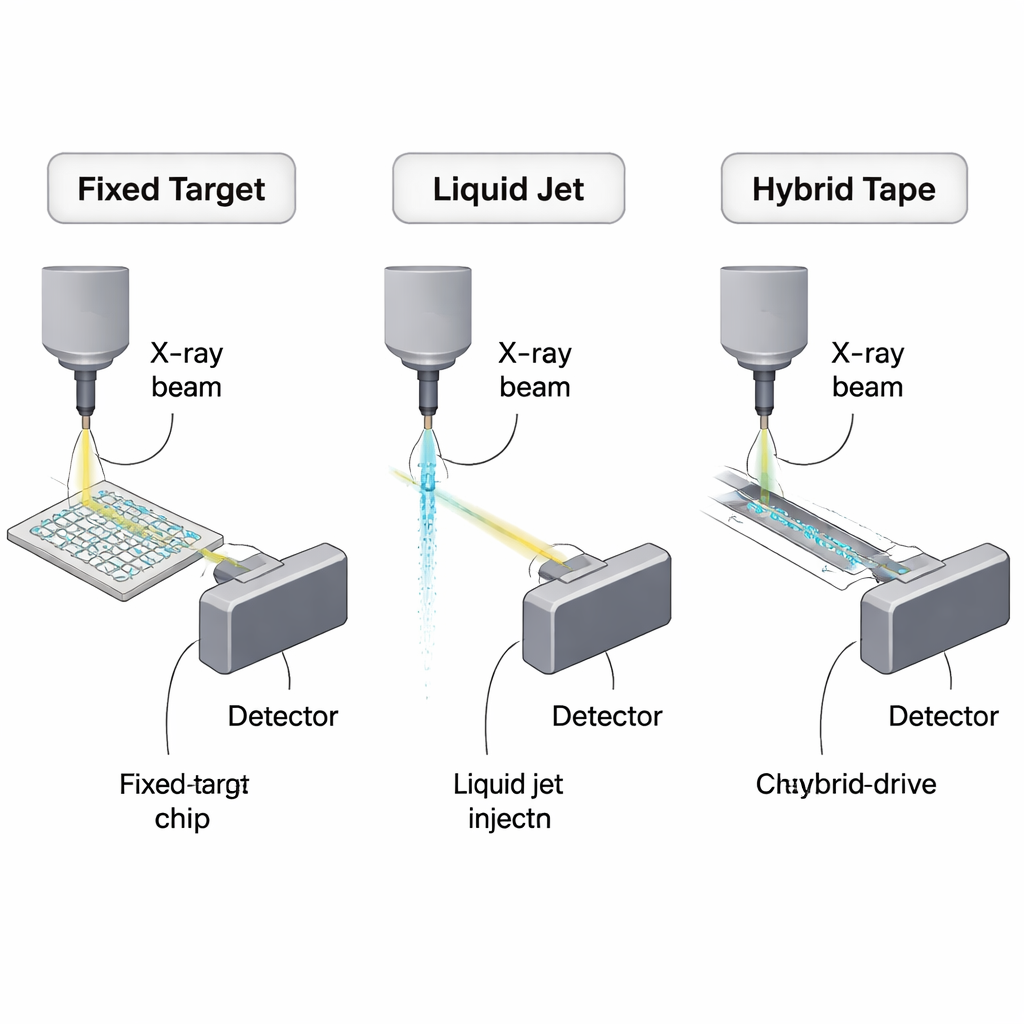
Por qué la cristalografía serial necesita mejor entrega
La cristalografía tradicional se basaba en un único cristal grande rotado en un haz de rayos X. La cristalografía serial cambia el planteamiento: en lugar de un cristal grande, miles de microcristales, cada uno usado una sola vez, se lanzan o se escanean mediante pulsos de rayos X ultrabrillantes procedentes de sincrotrones o láseres de electrones libres de rayos X (XFEL). Esto permite recoger datos a temperatura ambiente y obtener “instantáneas” rápidas de reacciones químicas, pero también implica reponer cristales constantemente a tasas que siguen trenes de pulsos de rayos X que pueden alcanzar millones de pulsos por segundo. Gran parte de la suspensión de cristales nunca llega a encontrarse con el haz y se desecha, por lo que reducir el consumo de muestra se ha convertido en un desafío técnico y económico central para el campo.
Objetivos fijos: microchips que exprimen cada gota
Una estrategia importante consiste en inmovilizar microcristales sobre soportes sólidos pequeños llamados objetivos fijos. En lugar de rociar cristales frente al haz, los investigadores los disponen en matrices sobre chips de silicio o polímero y mueven el chip para que cada cristal pase por el foco de rayos X una vez. En un experimento mental en el mejor de los casos, unos 10.000 microcristales de una proteína modelo podrían, en principio, aportar un conjunto de datos completo usando solo unos 450 nanogramos de proteína. Los dispositivos reales no son todavía tan ahorradores, pero ya reducen las necesidades a decenas de microgramos hasta unas pocas décimas de miligramo, órdenes de magnitud mejores que los primeros experimentos seriales. La revisión compara mallas de silicio, películas poliméricas ultrafinas y chips plásticos multicapa, valorando sus fortalezas (bajo ruido de fondo por dispersión, crecimiento de cristales en el chip, compatibilidad con estudios a temperatura ambiente) frente a problemas prácticos como la deshidratación, la dispersión no deseada del material del chip y el volumen “muerto” adicional introducido por pipeteo manual.
Chorros líquidos y corrientes viscosas: rápidos pero glotones
Otra familia de métodos mantiene los cristales suspendidos en líquido y los entrega de forma continua a través del haz. Boquillas virtuales gas‑dinámicas crean chorros extremadamente finos que pueden seguir el ritmo de los trenes de pulsos rápidos de los XFEL, convirtiéndolos en una herramienta de trabajo para estudios con resolución temporal y experimentos de mezcla‑e‑inyección donde las reacciones se desencadenan por mezcla rápida justo antes de la exposición. Sin embargo, porque los chorros funcionan de forma continua, la mayor parte del flujo nunca coincide con un pulso de rayos X. Incluso con ajustes cuidadosos, los experimentos prácticos consumen mucho más proteína que el mínimo teórico: típicamente decenas a cientos de microlitros de lodo cristalino concentrado. Para mitigar esto, se han desarrollado diseños más eficientes, como boquillas de doble flujo que envuelven la corriente de cristales con un líquido sacrificial, inyectores por electrohilado “MESH” que funcionan a tasas de flujo menores, y extrusores de alta viscosidad que empujan cristales embebidos en geles o fases cúbicas lipídicas a microlitros por minuto o menos. Estos métodos viscosos son especialmente valiosos para proteínas de membrana frágiles y para estudios a temperatura ambiente en sincrotrones, pero sus corrientes más gruesas aumentan la dispersión de fondo y son menos adecuados para las fuentes de rayos X más rápidas.
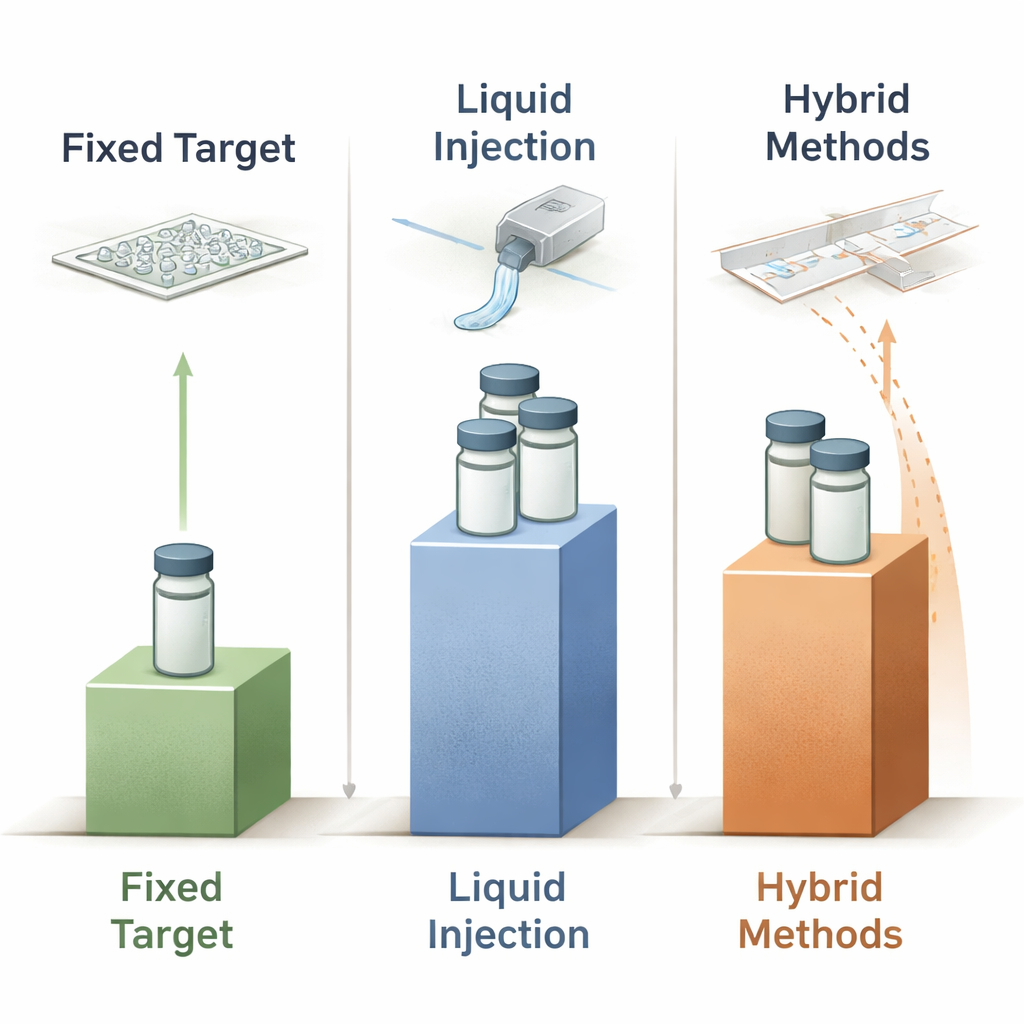
Gotas, cintas e híbridos: sincronizando pulsos uno a uno
Una tercera clase, cada vez más creativa, de enfoques “híbridos” combina soportes sólidos con entrega controlada de líquido o gotas. Los sistemas de cinta, por ejemplo, depositan gotas o tiras líquidas finas sobre una película polimérica en movimiento que pasa por el haz; sincronizar el movimiento permite sondear pasos de reacción o exposición a gases en retardos definidos. Los sistemas de gota bajo demanda van más lejos, usando dispositivos acústicos o piezoeléctricos para expulsar gotas de nanolitro o incluso picolitro solo cuando se espera un pulso de rayos X, reduciendo drásticamente el desperdicio. Algunos diseños mezclan una gota de ligando en una gota precolocada que contiene cristales en la cinta justo antes de que alcance el haz, permitiendo enzymología con resolución temporal y reactivos cuidadosamente racionados. Otros híbridos, como el método LAMA en chip, añaden gotas diminutas de sustrato directamente sobre cristales precolocados en chips de objetivo fijo. A lo largo de estos diseños, el uso reportado de proteína abarca un rango amplio: desde niveles cercanos al miligramo hasta algunos miligramos para series temporales completas, mostrando tanto la promesa como los retos de ingeniería actuales para sincronizar gotas, cristales y pulsos de rayos X.
¿Qué tan cerca estamos del mínimo teórico?
Al comparar docenas de experimentos publicados en objetivos fijos, inyectores líquidos y sistemas híbridos, los autores muestran que ningún método existente se acerca al ideal de 450 nanogramos; incluso los mejores dispositivos todavía sobrepasan ese valor por aproximadamente dos órdenes de magnitud. Sin embargo, emergen tendencias claras. Los objetivos fijos suelen usar la menor cantidad de proteína y son atractivos siempre que la mezcla con resolución temporal no sea esencial o pueda implementarse en el chip. Los chorros líquidos siguen dominando los estudios XFEL con requisitos temporales más exigentes, pero siguen siendo intensivos en muestra, especialmente cuando se requieren muchos puntos temporales. Los esquemas híbridos de gotas y cinta ofrecen algunos de los mayores ahorros relativos, en particular cuando la sincronización de las gotas está estrechamente sincronizada con la fuente de rayos X. De cara al futuro, el artículo sostiene que el progreso vendrá de un mejor control microfluídico, de la automatización para eliminar pasos de manipulación derrochadores y del uso de fuentes compactas de rayos X y optimización basada en datos para codiseñar experimentos y sistemas de entrega que acerquen el consumo de proteína cada vez más al límite teórico.
Cita: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Palabras clave: cristalografía serial, cristalografía de proteínas con rayos X, entrega de muestras, láser de electrones libres de rayos X, microfluidos