Clear Sky Science · es
La reducción de RAD23A prolonga la vida y atenúa la patología en un modelo de ratón de la proteinopatía por TDP-43
Por qué esta investigación importa a familias y pacientes
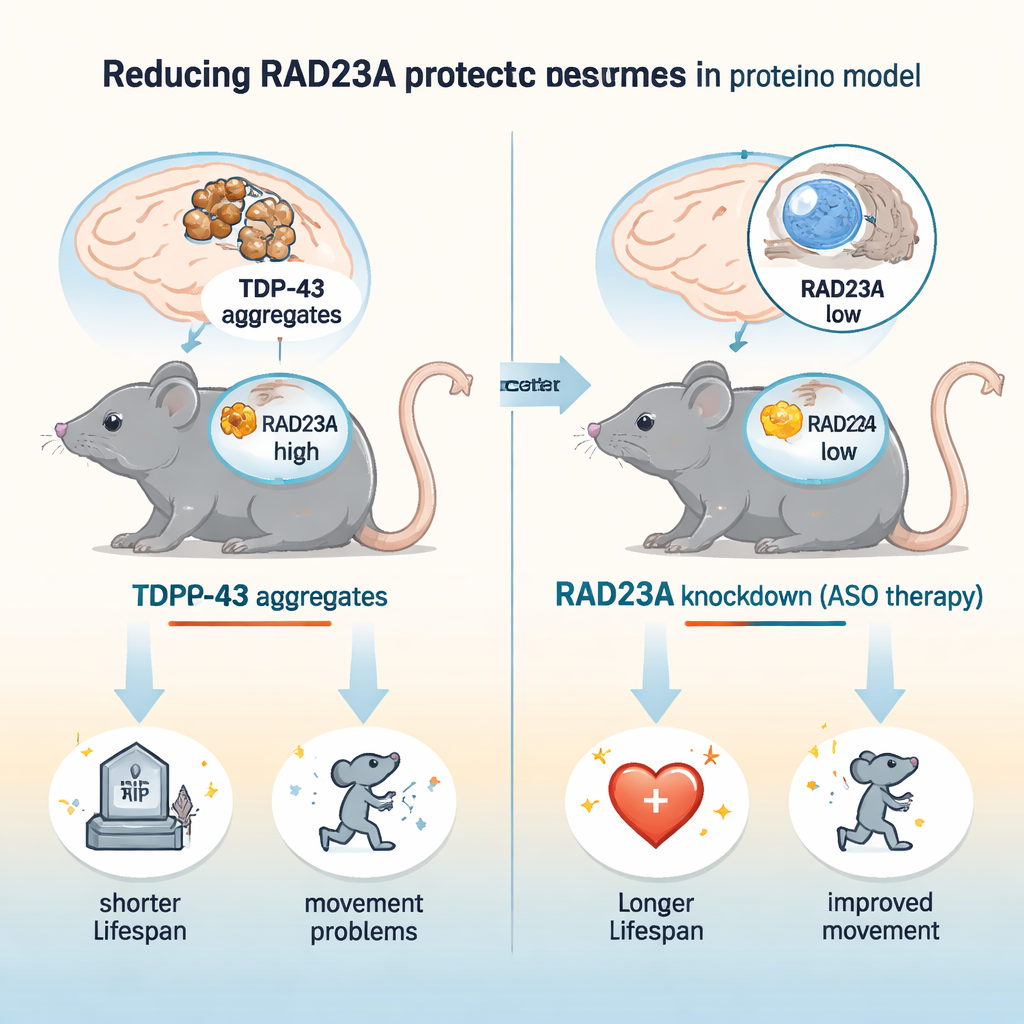
Muchas formas de demencia y de enfermedad de la motoneurona, incluidas la esclerosis lateral amiotrófica (ELA) y la demencia frontotemporal (DFT), implican proteínas en las células cerebrales que se pliegan mal, se agrupan y, de forma gradual, intoxican las neuronas. Uno de los culpables clave es una proteína llamada TDP-43, que normalmente ayuda a gestionar el ARN pero se vuelve tóxica cuando se agrega. Este estudio plantea una pregunta esperanzadora: ¿podemos hacer que las células cerebrales sean más resistentes reduciendo otra proteína, RAD23A, que participa en el manejo de proteínas dañadas? Los autores muestran en ratones que bajar los niveles de RAD23A puede prolongar la vida, mejorar el movimiento y disminuir el daño cerebral en un modelo de enfermedad impulsada por TDP-43, lo que sugiere una nueva estrategia terapéutica.
Un atasco de tráfico de proteínas en neuronas enfermas
Las enfermedades neurodegenerativas suelen caracterizarse por montones de proteínas mal plegadas que la maquinaria de eliminación de la célula no consigue limpiar. En la ELA y la DFT, TDP-43 sale del núcleo, forma agregados pegajosos y queda fuertemente etiquetada con ubiquitina, una señal que normalmente dirige las proteínas al proteasoma, la trituradora principal de la célula. RAD23A es una de varias proteínas “shuttle” que pueden transportar carga etiquetada con ubiquitina hasta el proteasoma. Sin embargo, trabajos previos en gusanos y neuronas en cultivo sugirieron que perder proteínas similares a RAD23 podría, en realidad, proteger frente al daño inducido por TDP-43, una paradoja que este estudio se propuso explorar en un cerebro mamífero vivo.
Disminuir RAD23A en un modelo de ratón con TDP-43
Los investigadores utilizaron un modelo de ratón bien establecido, llamado TAR4/4, que sobreexpresa TDP-43 humano en neuronas y desarrolla problemas de movimiento, curvatura espinal, temblor y muerte temprana, reflejando rasgos claves de la ELA/DFT. Redujeron RAD23A de dos maneras: inyectando a ratones recién nacidos oligonucleótidos antisentido (ASO) que reducen el ARN de Rad23a, y mediante el cruce con ratones portadores de una deleción genética de Rad23a. Un único tratamiento con ASO redujo los niveles de RAD23A en cerebro y médula espinal en aproximadamente tres cuartas partes. En estos ratones con TDP-43, la disminución de RAD23A alargó la supervivencia en torno a un 50% y retrasó el inicio y la gravedad de los problemas de marcha, el temblor, la curvatura espinal y el plegamiento de las extremidades posteriores. Curiosamente, una pérdida genética completa de RAD23A no aportó un beneficio adicional, lo que sugiere que la reducción parcial es óptima y que la ausencia total a largo plazo puede desencadenar cambios compensatorios.
Menos inflamación, mejor manejo de proteínas y un genoma más tranquilo
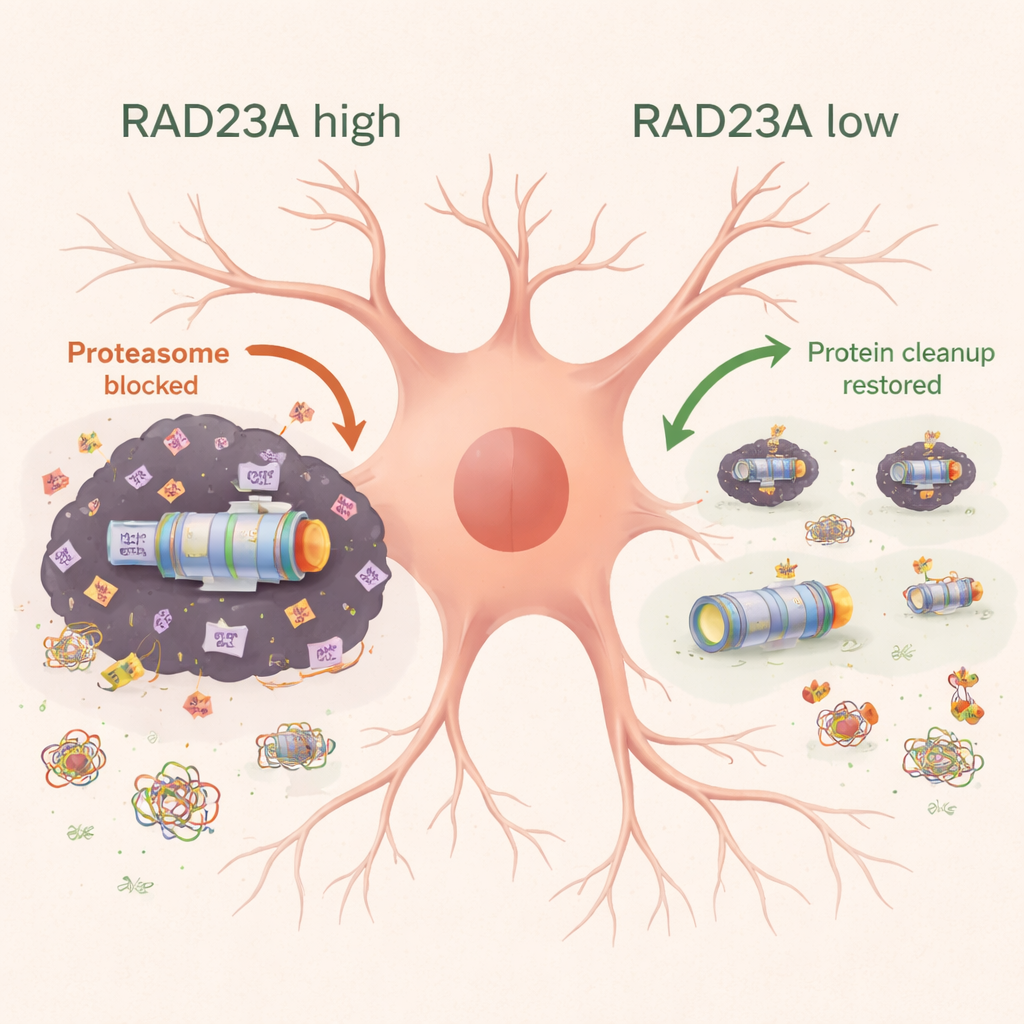
El examen microscópico de la corteza motora mostró que los ratones con TDP-43 perdían neuronas y desarrollaban una fuerte activación de astrocitos y microglía, las células de apoyo e inmunitarias del cerebro. Reducir RAD23A preservó el número de neuronas y disminuyó marcadores de inflamación y muerte celular. Los análisis bioquímicos revelaron que la sobreproducción de TDP-43 saturaba las células con proteínas etiquetadas por ubiquitina e insolubles en detergente y arrastraba subunidades del proteasoma hacia estos agregados, debilitando la capacidad celular para eliminar proteínas dañadas. La reducción de RAD23A disminuyó la carga total de proteínas ubiquitinadas, mantuvo más proteasomas en el grupo soluble y funcional, y restauró varios tipos de actividad proteasomal hacia niveles normales. Al mismo tiempo, la inhibición de RAD23A redujo tanto las formas totales como las agregadas de TDP-43, incluido un fragmento particularmente tóxico de 25 kilodaltons, y desplazó a TDP-43 desde el citoplasma de vuelta al núcleo. El secuenciamiento de ARN a nivel genómico mostró que miles de cambios en la expresión génica desencadenados por TDP-43 se invirtieron parcialmente cuando se redujo RAD23A, especialmente genes implicados en la función neuronal, la producción de energía mitocondrial y rutas de eliminación de agregados como la agrefagia.
Remodelando el proteoma “insoluble” oculto
Para examinar más de cerca los agregados persistentes que resisten los detergentes habituales, el equipo utilizó espectrometría de masas con isótopos pesados para catalogar las proteínas atrapadas en la fracción insoluble de la corteza de ratón. La expresión de TDP-43 humano atrajo componentes del proteasoma, proteínas del citoesqueleto y del transporte, y otra maquinaria celular. Cuando se redujo RAD23A, la composición global de este proteoma insoluble cambió: se secuestraron menos proteínas relacionadas con el proteasoma y el transporte, mientras que algunas proteínas ribosomales y relacionadas con el estrés aumentaron en los agregados. Es notable que este remodelado no reflejó simplemente cambios en los niveles de ARN, lo que sugiere que RAD23A influye principalmente en cómo las proteínas existentes se distribuyen entre estados solubles y agregados, en lugar de cuánto se sintetiza de cada proteína.
Qué podría significar esto para futuras terapias
En conjunto, estos hallazgos sitúan a RAD23A como un regulador potente del control de calidad de proteínas en neuronas bajo estrés. Al reducir parcialmente RAD23A en un modelo de ratón impulsado por TDP-43, los autores consiguieron reducir los agregados proteicos tóxicos, restablecer la actividad de la maquinaria de eliminación de proteínas, mitigar cambios perjudiciales en la expresión génica, limitar la inflamación cerebral y prolongar la vida y la función motora. Dado que la acumulación anómala de TDP-43 es frecuente tanto en formas hereditarias como esporádicas de ELA, DFT y trastornos relacionados, dirigirse a RAD23A con fármacos antisense compatibles con humanos podría ofrecer una forma de proteger neuronas sin bloquear directamente a TDP-43, que es una proteína esencial. Aunque queda mucho por probar en otros modelos y en humanos, este trabajo identifica a RAD23A como una diana prometedora en una vía común de la neurodegeneración.
Cita: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Palabras clave: TDP-43, ELA, agregación de proteínas, proteasoma, terapia antisense