Clear Sky Science · es
El centro nervioso de la ingeniería de órganos
Por qué conectar los órganos importa
Los científicos se acercan a la posibilidad de fabricar órganos de reemplazo en el laboratorio para abordar la grave escasez de corazones, hígados, riñones y otros donantes. Pero la mayoría de los órganos artificiales se centran en los vasos sanguíneos y pasan por alto otro ingrediente crucial: los nervios. Este artículo de revisión explica por qué el cableado eléctrico del cuerpo es esencial para el crecimiento de los órganos, su funcionamiento cotidiano y la curación, y cómo los investigadores están aprendiendo a entretejer redes nerviosas en órganos cultivados en el laboratorio.
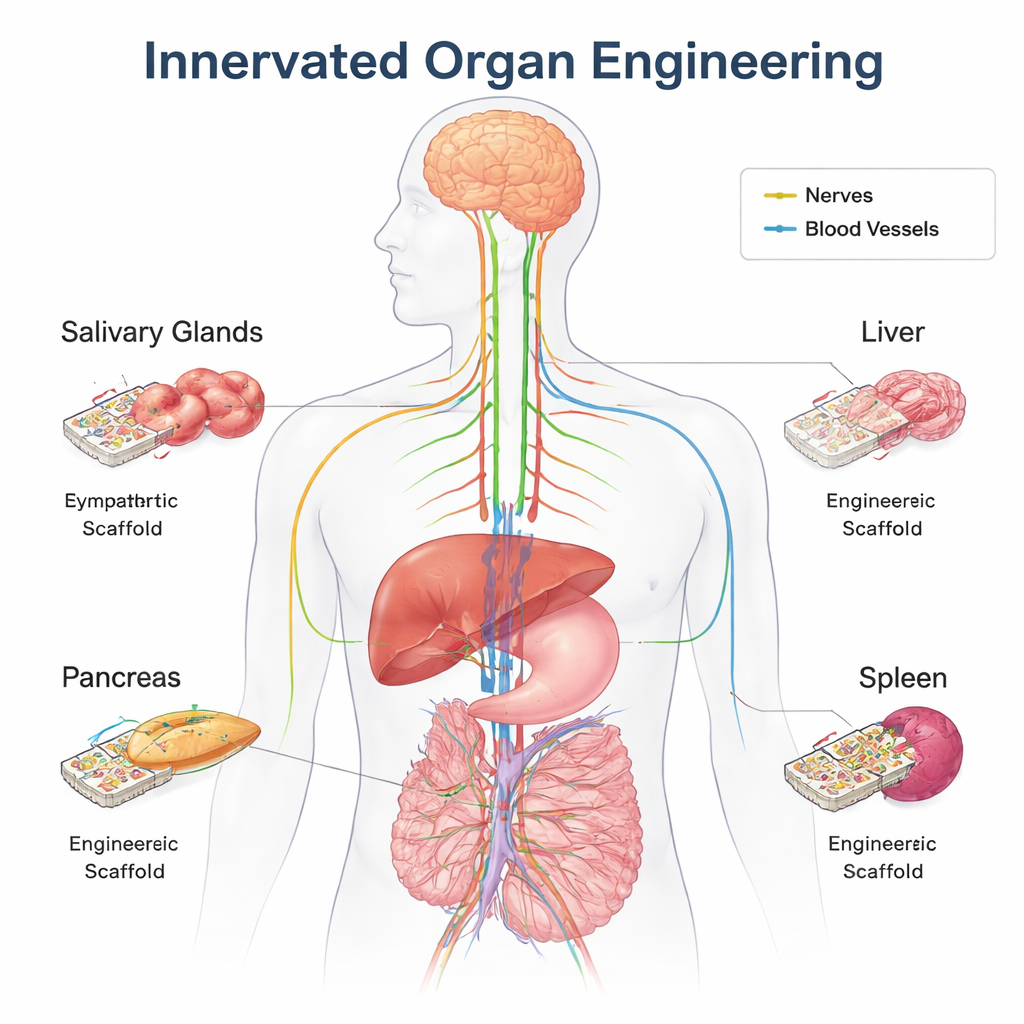
La red de control oculta del cuerpo
Cada órgano importante está atravesado por fibras nerviosas que se comunican constantemente con el cerebro y la médula espinal. A través del sistema nervioso autónomo—las ramas de “lucha o huida” y “descanso y digestión”—estos nervios regulan silenciosamente la glucosa en sangre, la digestión, las respuestas inmunitarias, el flujo sanguíneo y más. Lo hacen enviando mensajeros químicos como la acetilcolina y la norepinefrina, y detectando cambios como estiramiento, temperatura o niveles de nutrientes. Más allá del control diario, los nervios también ayudan a moldear los órganos antes del nacimiento, guían la cicatrización y sostienen las células madre que reparan los tejidos. En muchos sitios, los nervios crecen junto a los vasos sanguíneos, usando señales guía similares, de modo que el cableado y la plomería se desarrollan juntos.
Por qué los trasplantes sobreviven sin nervios—pero los órganos de laboratorio no
Los trasplantes tradicionales de órganos suelen implantarse sin sus nervios originales. Un hígado o un riñón trasplantado puede seguir funcionando porque recibe hormonas y otras señales por el torrente sanguíneo, y con el tiempo pueden crecer nuevas fibras nerviosas desde el receptor. Ese “periodo de gracia” no existe para los órganos diseñados desde cero. Estas construcciones típicamente carecen de la mezcla completa de tipos celulares maduros y de la matriz de soporte compleja que tiene un órgano natural. Las conexiones nerviosas precisas son especialmente importantes para coordinar las muchas células especializadas dentro de órganos como el páncreas, el hígado, las glándulas salivales y el bazo. Los autores sostienen que, para la ingeniería de órganos de abajo hacia arriba—donde los órganos se ensamblan desde pequeños bloques—la inervación planificada debe tratarse como un requisito de diseño, no como un complemento opcional.
Cómo los nervios moldean cuatro órganos clave
La revisión explora en detalle cómo los nervios influyen en cuatro órganos de ejemplo. En el páncreas, las fibras simpáticas y parasimpáticas ayudan a esculpir la arquitectura de los islotes productores de insulina durante el desarrollo y más adelante afinan la liberación de insulina y glucagón según fluctúe la glucemia. En las glándulas salivales, la entrada parasimpática temprana mantiene vivas a las células madre epiteliales y guía la ramificación de los conductos que finalmente secretan saliva; cortar estos nervios en el momento equivocado interrumpe la formación glandular normal. Los nervios del hígado detectan niveles de sal, agua, azúcares y grasas en la sangre y ajustan el metabolismo, la presión arterial y la regeneración tras una lesión. En el bazo, las fibras simpáticas se comunican directamente con las células inmunitarias, modulando la inflamación y ayudando al organismo a responder a infecciones y al estrés. En todos estos órganos, la pérdida o el cableado erróneo de los nervios se asocia con diabetes, problemas digestivos, enfermedades hepáticas y alteraciones de la inmunidad.
Construir órganos con cableado incorporado
Para incorporar la inervación en órganos bioingenierizados, los científicos combinan bioimpresión 3D avanzada, diseños inteligentes de andamiaje y células nerviosas derivadas de células madre. La bioimpresión por extrusión y basada en luz puede colocar distintos tipos celulares y materiales en patrones precisos, mientras que hidrogeles y polímeros especializados se ajustan para soportar fibras nerviosas largas y ramificadas. Estudios ya han creado redes neuronales impresas, unidades nervio–músculo y tejidos miniatura con semejanza cerebral que muestran actividad eléctrica realista. Los autores trazan planos prácticos para versiones inervadas del páncreas, la glándula salival, el hígado y el bazo: aislar o derivar las células clave del órgano, mezclarlas con neuronas autonómicas (simpáticas y parasimpáticas) en bioinks compatibles, imprimirlas en estructuras con forma de órgano y madurarlas en biorreactores para que los nervios puedan extenderse en el tejido antes de la implantación.
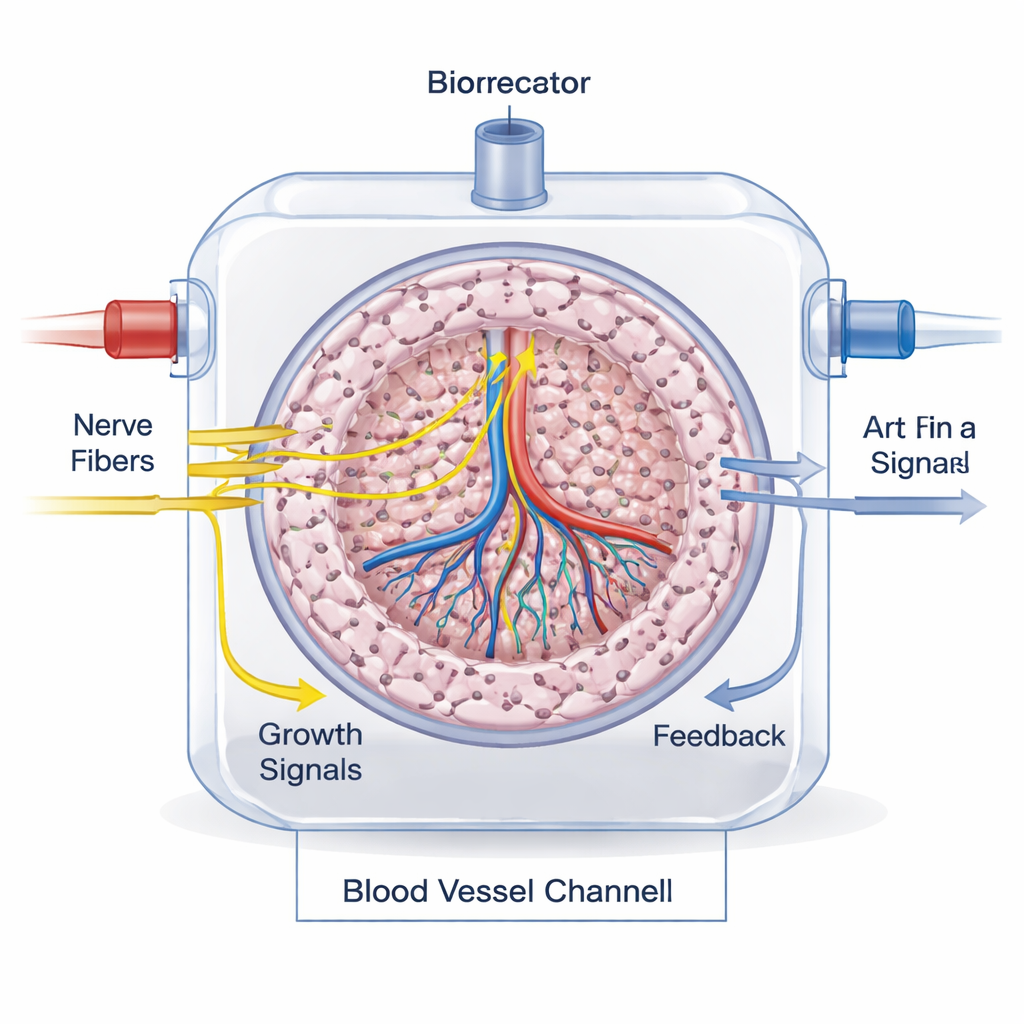
Medir si el cableado funciona
Comprobar que los nervios están realmente integrados y son funcionales es un desafío importante. En el laboratorio, los investigadores tiñen proteínas específicas de nervios, miden neurotransmisores con pruebas bioquímicas y usan imágenes en vivo para observar el crecimiento de axones y la respuesta celular. Las plataformas microfluídicas “órgano en un chip” ayudan a modelar un flujo sanguíneo realista y la señalización nervio–órgano. En animales y, eventualmente, en pacientes, la inervación puede seguirse combinando tinciones tisulares, trazadores nerviosos y métodos de imagen modernos como MRI, CT y PET con compuestos radiactivos especializados que resaltan fibras simpáticas o parasimpáticas.
De la idea a la terapia
El artículo concluye que los nervios no son un lujo sino un requisito central para órganos artificiales verdaderamente funcionales. Para pasar de demostraciones prometedoras en el laboratorio a terapias reales, el trabajo futuro debe mejorar la bioimpresión a gran escala de redes nerviosas intrincadas, refinar las fuentes celulares (especialmente neuronas autonómicas derivadas de células madre humanas) y desarrollar herramientas clínicas de imagen prácticas para monitorizar la integración neural tras la implantación. Si se superan estos obstáculos, los órganos de próxima generación podrían no solo reemplazar tejido perdido sino integrarse sin fisuras en los circuitos de control del propio cuerpo, ofreciendo tratamientos más fiables y realistas para la diabetes, la insuficiencia hepática, los trastornos de boca seca, las deficiencias inmunitarias y más allá.
Cita: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Palabras clave: ingeniería de órganos, inervación, biofabricación, bioimpresión 3D, sistema nervioso autónomo