Clear Sky Science · es
Histología óptica de superresolución en muestras embebidas en parafina y fijadas con formalina: desafíos y oportunidades
Ver más en muestras de tejido conservadas
Los hospitales de todo el mundo conservan finas rebanadas de órganos de pacientes en bloques de cera para que enfermedades como el cáncer o el daño renal puedan estudiarse durante años. Este artículo de revisión explica cómo nuevos tipos de microscopios ópticos están convirtiendo esas muestras rutinarias en ventanas potentes sobre la enfermedad, revelando detalles mucho más pequeños de lo que pueden ver los microscopios hospitalarios estándar. Estos avances podrían ayudar a los médicos a detectar enfermedades antes, comprender cómo progresan y ajustar los tratamientos con mayor precisión.
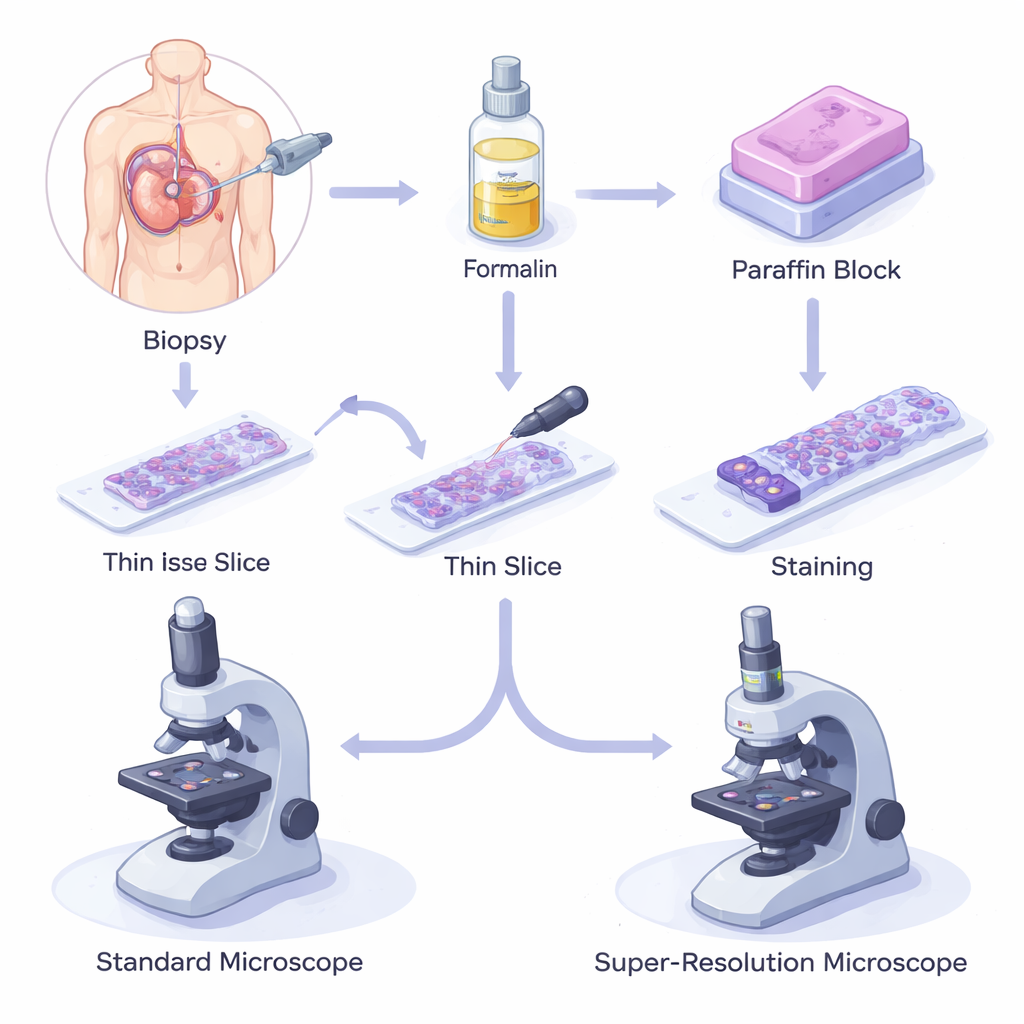
Cómo los tejidos preservados en cera impulsan la medicina moderna
Cuando un paciente se somete a una biopsia, se extrae un pequeño fragmento de tejido, se fija con un químico llamado formalina para detener la degradación y luego se embebe en parafina. El bloque se corta en secciones tan finas como un cabello, se coloca sobre portaobjetos de vidrio, se tiñe y se examina con un microscopio óptico. Este método de tejido fijado con formalina y embebido en parafina (FFPE) es barato, fiable y puede conservar muestras durante décadas a temperatura ambiente. Como resultado, millones de muestras FFPE se almacenan en biobancos de todo el mundo, apoyando desde la biología básica hasta estudios avanzados de genética y proteínas, y formando la columna vertebral del diagnóstico y pronóstico modernos.
Por qué los microscopios ordinarios ya no son suficientes
Los microscopios ópticos tradicionales están limitados por la física de la luz: los detalles más pequeños de aproximadamente 250 nanómetros se difuminan. Muchas estructuras relacionadas con enfermedades —como los finos filtros del riñón, las conexiones entre células nerviosas o pequeños cambios en la arquitectura del ADN dentro del núcleo— están por debajo de ese límite. El flujo de trabajo actual suele combinar microscopía óptica estándar para una visión general con microscopía electrónica para detalles a escala nanométrica, pero ese enfoque es lento, caro y requiere preparaciones de muestra totalmente distintas. Por ello, clínicos e investigadores buscan un sistema único y flexible que pueda escanear grandes áreas con rapidez y, al mismo tiempo, acercarse para ver características a escala nanométrica en las mismas secciones FFPE que ya utilizan.
Nuevas formas de afinar la imagen
En las últimas dos décadas, varias familias de microscopios de “superresolución” han superado la barrera de resolución tradicional utilizando marcadores fluorescentes y óptica ingeniosa. Los métodos de localización de moléculas individuales alternan moléculas encendidas y apagadas y precisan sus posiciones una por una; la iluminación estructurada proyecta patrones de luz en franjas sobre el tejido y usa el cálculo para recuperar detalles más finos; la supresión por emisión estimulada crea un pequeño punto luminoso usando un haz en forma de dona; y los enfoques basados en fluctuaciones analizan sutiles parpadeos en la imagen para inferir la estructura. Una estrategia distinta, llamada microscopía de expansión, evita la óptica compleja al hinchar físicamente el tejido en un gel, de modo que los microscopios ordinarios pueden ver detalles antes invisibles. Estos métodos ya se han aplicado a muestras FFPE de mama, colon, páncreas, riñón, cerebro, piel, placenta y otros órganos, revelando cómo cambian las mitocondrias en tumores, cómo fallan los filtros renales y cómo se forman agregados de proteínas en la enfermedad de Alzheimer.
Obstáculos en el camino hacia el uso cotidiano
A pesar de su promesa, estas técnicas aún no están listas para convertirse en herramientas rutinarias en la mayoría de los laboratorios de patología. Muchos sistemas de superresolución son lentos, cubren campos de visión muy pequeños o requieren decenas de miles de imágenes para construir una sola imagen de alta definición, lo que es impráctico cuando un patólogo debe evaluar grandes áreas de tejido. Los propios tejidos FFPE son ópticamente difíciles: dispersan la luz, presentan autofluorescencia y pueden ocultar las moléculas que deben etiquetarse, todo lo cual puede causar imágenes borrosas o estructuras artefactuales. Algunos métodos exigen tintes especiales, tampones personalizados o tratamientos químicos en varios pasos que no encajan fácilmente en los flujos de trabajo histológicos estándar. Además, los instrumentos comerciales son caros y complejos de operar, y los datos resultantes requieren un procesamiento computacional intensivo y almacenamiento.
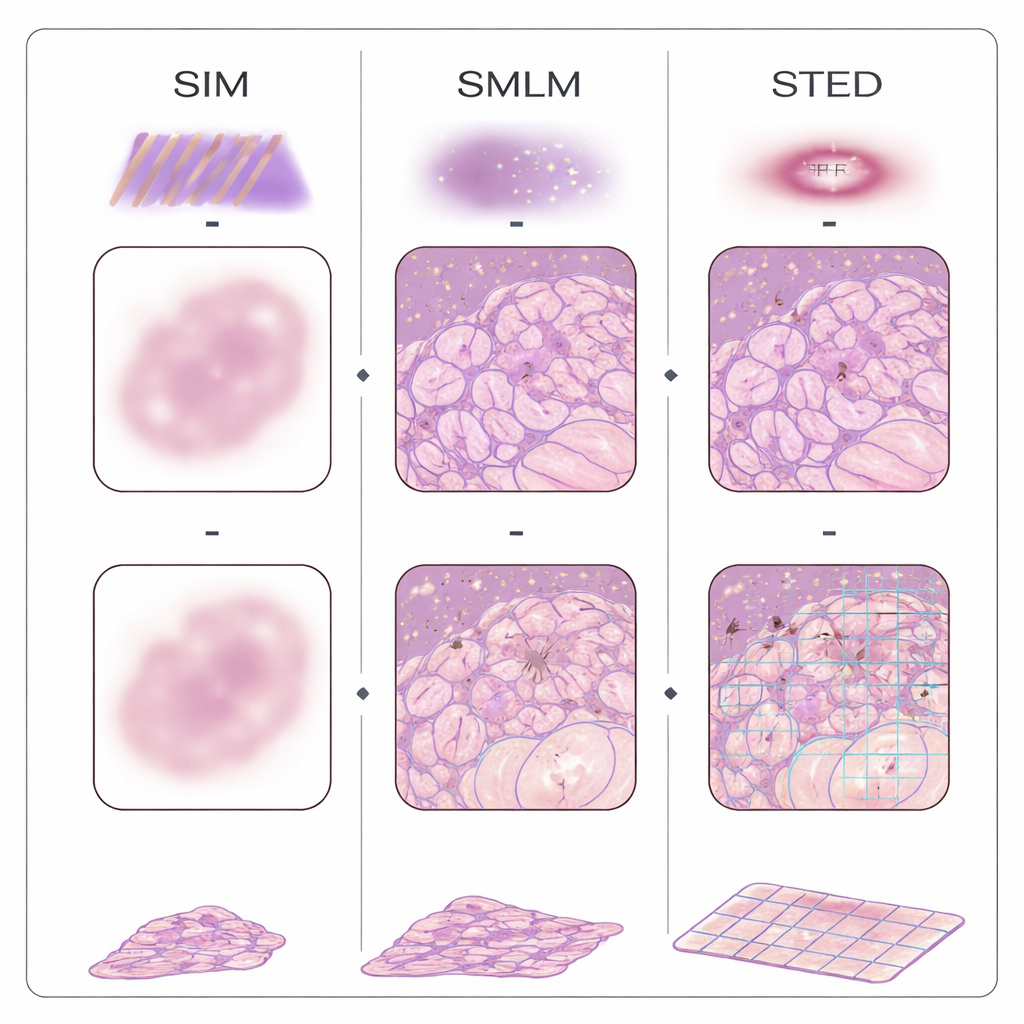
Combinar óptica inteligente y software inteligente
Para superar estos obstáculos, los investigadores están combinando una mejor óptica con imagen sin etiqueta y con inteligencia artificial. Métodos de alto rendimiento y limitados por difracción como la ptychografía de Fourier y la microscopía óptica no lineal pueden escanear rápidamente secciones FFPE grandes, incluso sin teñir, y proporcionar mapas cuantitativos de la estructura tisular. Las plataformas de patología digital ahora capturan portaobjetos enteros a alta resolución y emplean aprendizaje automático para detectar tumores y puntuar biomarcadores como HER2, Ki‑67 y PD‑L1. Modelos de aprendizaje profundo pueden incluso convertir imágenes de baja resolución en vistas de superresolución, reduciendo potencialmente la necesidad de parte del hardware especializado y aprovechando mejor los archivos de biopsias existentes.
Qué significa esto para los pacientes futuros
Los autores concluyen que la verdadera “histología de superresolución” de muestras FFPE —que combine detalle a escala nanométrica, alta velocidad, coste razonable y compatibilidad con las rutinas de laboratorio actuales— aún no se ha materializado por completo, pero está al alcance. A medida que los métodos ópticos se vuelvan más rápidos y robustos, y el análisis basado en IA madure, estas herramientas podrían revelar cambios sutiles y tempranos en los tejidos que hoy pasan desapercibidos, mejorar la precisión diagnóstica y orientar decisiones de tratamiento más personalizadas. A largo plazo, convertir cada bloque de cera archivado en un mapa de alta definición de la enfermedad podría transformar tanto la investigación como la atención clínica.
Cita: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Palabras clave: microscopía de superresolución, tejido FFPE, patología digital, imagen óptica, diagnóstico del cáncer