Clear Sky Science · es
Nanoenzimas que amplían los límites de la biocatálisis
Pequeños ayudantes que aceleran la química
Desde la elaboración de cerveza hasta la digestión de la cena, nuestra vida depende de ayudantes invisibles llamados catalizadores que aceleran las reacciones químicas. Durante más de un siglo se creyó que los catalizadores biológicos eran únicamente proteínas frágiles y, más tarde, ARN catalítico. Esta revisión presenta las “nanoenzimas”: diminutas partículas diseñadas que se comportan como enzimas pero están hechas de materiales robustos como metales, óxidos y carbono. Pueden resistir el calor, el frío y condiciones adversas, y están empezando a transformar nuestra visión de la química en sistemas vivos, en la enfermedad, en la industria e incluso en el origen de la vida.
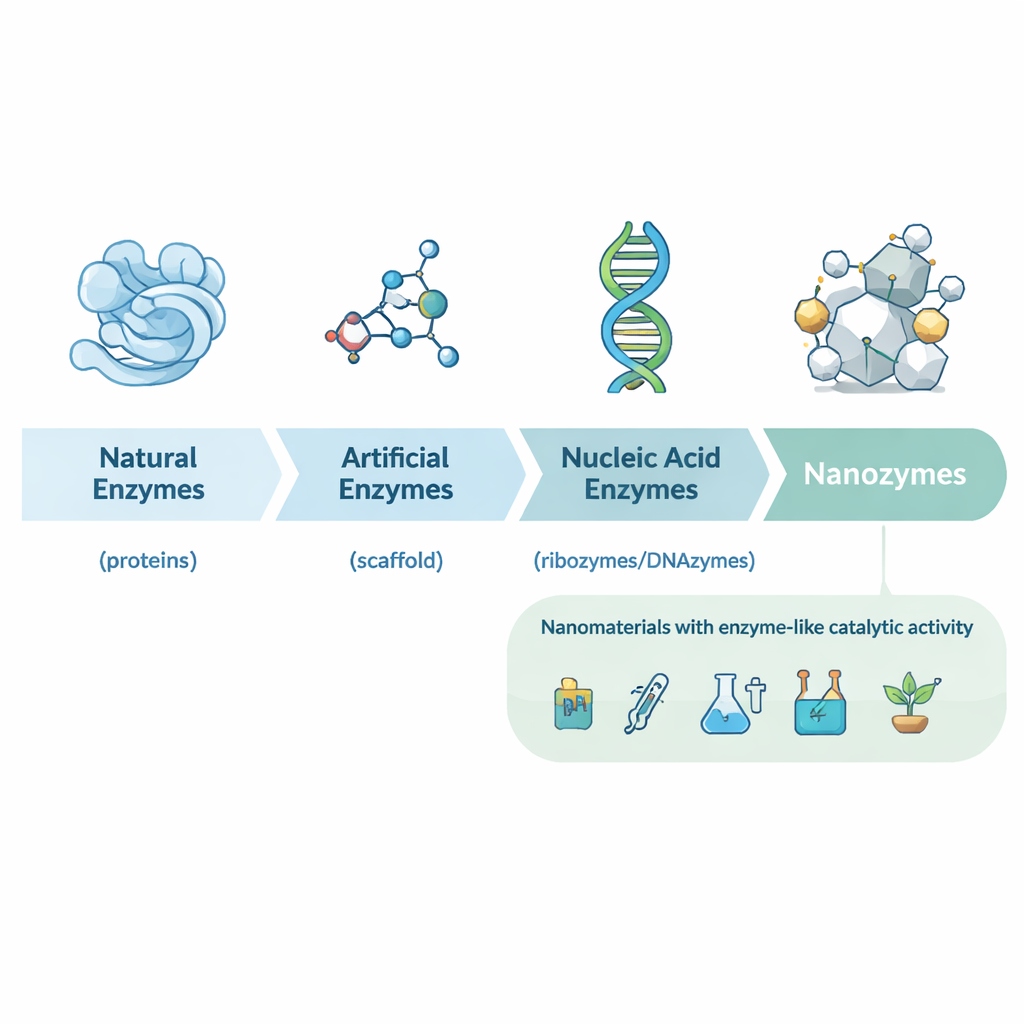
De las enzimas naturales a los nanocatalizadores diseñados
El artículo recorre primero la historia de la biocatálisis, desde los primeros descubrimientos de enzimas proteicas en la levadura y los jugos gástricos hasta los ribozimas (ARN catalítico) y una amplia gama de enzimas artificiales construidas a partir de pequeñas moléculas y anticuerpos. Estos catalizadores tradicionales son potentes pero a menudo caros, inestables y difíciles de producir a gran escala. A principios de los años 2000, los investigadores descubrieron que algunos nanomateriales —por ejemplo, nanopartículas de óxido de hierro— podían imitar el comportamiento de enzimas clásicas como la peroxidasa de rábano picante. Esto dio lugar al concepto de nanoenzimas: partículas a escala nanométrica cuya propia estructura les confiere actividad semejante a la de las enzimas, en lugar de depender de proteínas o pequeños catalizadores unidos a ellas.
Qué hace diferentes a las nanoenzimas
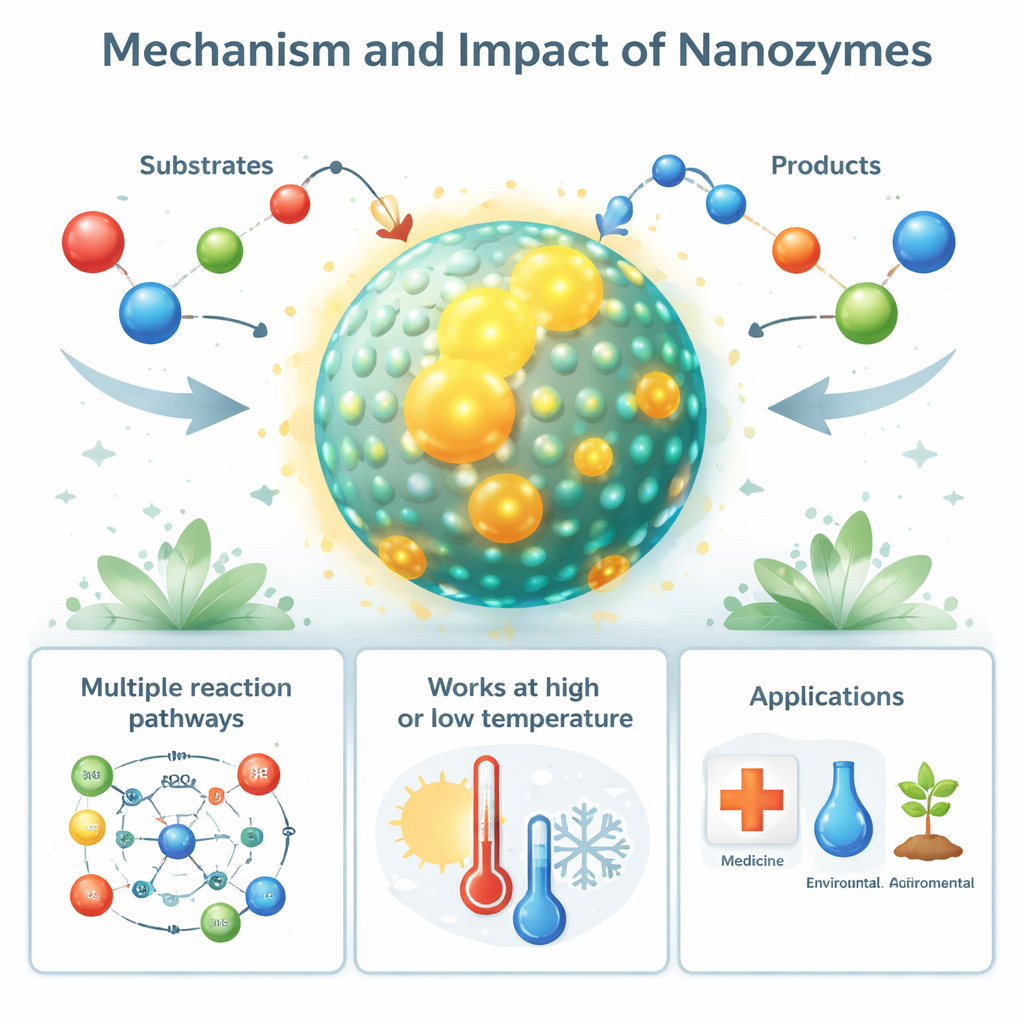
A diferencia de las enzimas, que tienen un único y preciso bolsillo activo, las nanoenzimas exponen numerosos puntos activos a lo largo de sus superficies. Esos puntos pueden localizarse en aristas cristalinas, defectos o interfaces entre dos materiales y, en conjunto, pueden procesar muchas moléculas a la vez. Un único sitio activo en una nanoenzima suele ser menos eficiente que el de una enzima, pero una sola nanopartícula puede albergar miles de esos sitios, de modo que su potencia catalítica global puede igualar o superar a la de enzimas naturales. Su actividad también puede ajustarse cambiando el tamaño, la forma, el dopado químico y los recubrimientos superficiales, de manera similar a modificar la arquitectura y el cableado de una pequeña máquina. Al estar hechas de sólidos robustos en lugar de proteínas plegadas y delicadas, las nanoenzimas siguen funcionando a temperaturas altas, bajas o en niveles salinos elevados que inhabilitarían rápidamente a la mayoría de las enzimas.
Cómo funcionan las nanoenzimas y cómo se miden
Los autores muestran que las nanoenzimas a menudo siguen las mismas reglas cinéticas básicas que los bioquímicos usan para las enzimas, como el comportamiento de Michaelis–Menten, donde la velocidad de reacción depende de lo fácil que sea para un catalizador unirse y convertir su sustrato. Pero hay giros importantes. Una partícula puede albergar múltiples tipos de sitios activos, por lo que una sola nanoenzima puede llevar a cabo reacciones diferentes o incluso contrapuestas, como tanto producir como destruir especies reactivas de oxígeno. Esto puede producir curvas cinéticas complejas “no académicas” que ocultan múltiples procesos bajo una tendencia suave. La revisión explica cómo los investigadores descomponen estos comportamientos, estiman cuántos sitios activos existen realmente y comparan la actividad global de diferentes nanoenzimas usando unidades estandarizadas, todo lo cual es crucial para convertir un material prometedor en una herramienta fiable.
De nanoenzimas naturales a usos en el mundo real
De forma intrigante, el comportamiento similar a las nanoenzimas no se limita al laboratorio. Ciertas nanoestructuras biológicas, como las jaulas proteicas llenas de hierro (ferritina) y las partículas magnéticas en bacterias (magnetosomas), actúan como nanoenzimas naturales que ayudan a controlar las especies reactivas de oxígeno dañinas. Incluso fibras proteicas relacionadas con enfermedades, como los depósitos de amiloide en la enfermedad de Alzheimer, pueden adoptar actividad peroxidasa parecida a la de las nanoenzimas y dañar las células vecinas. En el ámbito aplicado, las nanoenzimas sintéticas se usan como sustitutos más baratos y resistentes de las enzimas en pruebas diagnósticas, biosensores y ensayos industriales. Su capacidad para generar o eliminar especies reactivas de oxígeno se aprovecha para destruir células tumorales y bacterias, proteger tejidos del estrés oxidativo y ayudar a cultivos a resistir la sequía, la salinidad y la contaminación.
Diseñando la próxima generación de catalizadores inteligentes
De cara al futuro, los autores resaltan desafíos clave: identificar las estructuras atómicas exactas que actúan como sitios activos, mejorar la selectividad de las reacciones para que las nanoenzimas actúen solo donde y cuando se desee, y garantizar la seguridad y la estabilidad dentro del cuerpo. Señalan técnicas avanzadas de imagen, simulaciones a nivel cuántico y aprendizaje automático como herramientas potentes para predecir y optimizar el rendimiento de las nanoenzimas. Debido a que las nanoenzimas pueden funcionar en condiciones extremas, responder a la luz, al calor, al sonido o a campos magnéticos, y a veces realizar varias reacciones en secuencia, podrían sustentar nuevas terapias, tecnologías medioambientales y procesos industriales. La revisión concluye que las nanoenzimas amplían la propia definición de biocatálisis e incluso podrían ofrecer pistas sobre cómo catalizadores primitivos impulsaron la química de la vida temprana.
Cita: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Palabras clave: nanoenzimas, biocatálisis, nanopartículas, imitadores de enzimas, especies reactivas de oxígeno