Clear Sky Science · es
Detección por nanoporo de la conformación de proteínas y péptidos para aplicaciones en punto de atención
Por qué las formas minúsculas de las proteínas podrían cambiar tu próxima revisión médica
Con el envejecimiento de las poblaciones, enfermedades como el Alzheimer, el Parkinson, las cardiopatías y el cáncer son cada vez más frecuentes. Muchas de estas dolencias comienzan cuando proteínas vitales y pequeños fragmentos proteicos (péptidos) cambian sutilmente de forma mucho antes de que aparezcan los síntomas. Las pruebas clínicas actuales suelen medir cuánto de un biomarcador está presente, no si su forma es normal o está alterada. Este artículo explora una tecnología llamada detección por nanoporo, que puede “sentir” eléctricamente la forma y la química de moléculas proteicas individuales, y sostiene que podría convertirse en la base de futuras pruebas en el punto de atención que se ejecuten en minutos en un pequeño dispositivo.
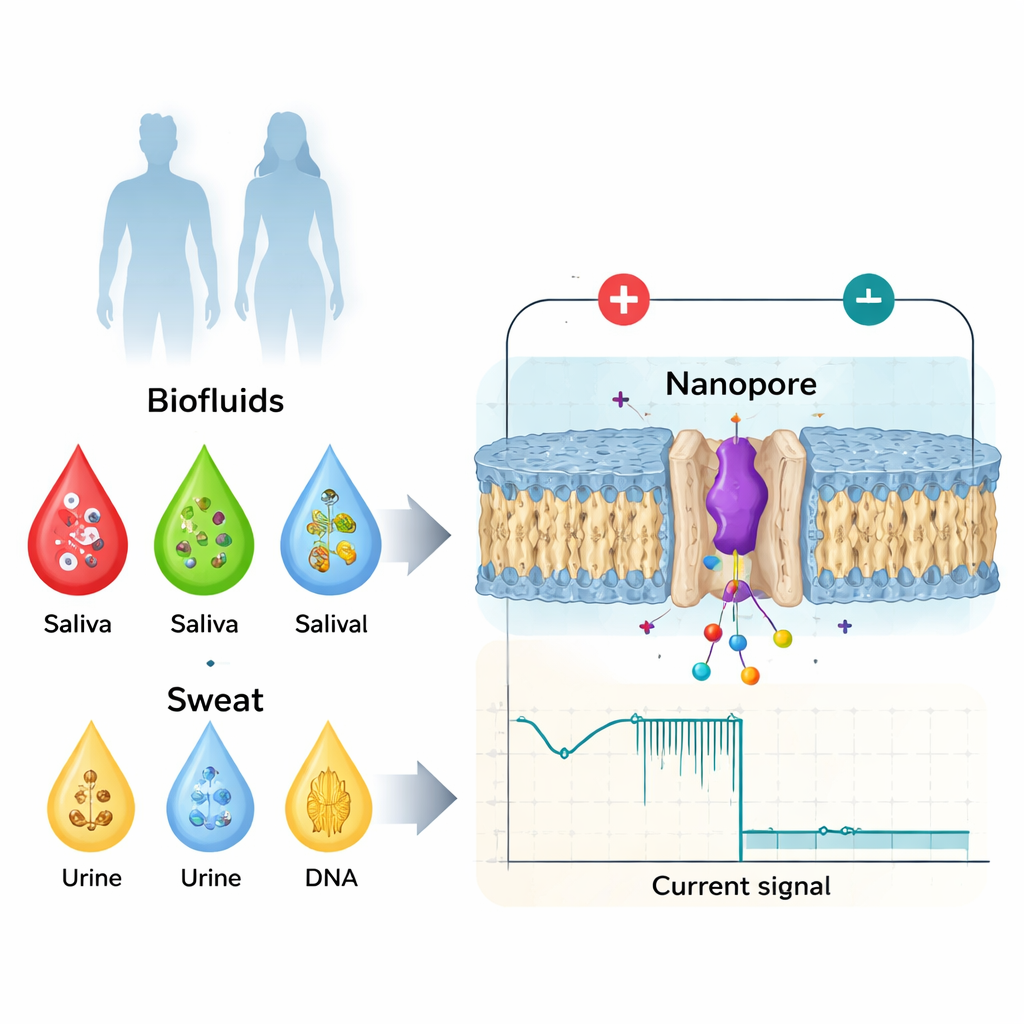
De los análisis sanguíneos simples a los biomarcadores sensibles a la conformación
Los médicos ya utilizan numerosos biomarcadores obtenidos de sangre, saliva, orina o sudor—como proteínas, hormonas o moléculas pequeñas—para monitorizar la salud y la enfermedad. Tradicionalmente, el foco ha estado en cambios evidentes: copias adicionales de una proteína, ADN dañado o la presencia de un componente viral. Pero la biología resulta ser más sutil. La misma proteína puede activarse o desactivarse por pequeños cambios en su estructura, por etiquetas químicas añadidas tras su síntesis o por versiones en espejo de sus bloques constituyentes. Estos cambios diminutos pueden alterar cómo una proteína se une a sus socios, forma agregados o transmite señales, y se asocian con problemas de coagulación, enfermedades neurodegenerativas y cáncer. Herramientas hospitalarias estándar como la espectrometría de masas, los ensayos basados en anticuerpos y la imagen de alta resolución son potentes, pero son caras, lentas, requieren personal altamente cualificado y, en general, no pueden desplegarse como dispositivos sencillos y rápidos en el punto de atención.
Lo que hace diferente a un nanoporo
La detección por nanoporo da la vuelta al problema. En lugar de promediar sobre billones de moléculas, examina una a la vez mientras atraviesa un agujero diminuto en una membrana de solo unos pocos millonésimos de milímetro de ancho. Se aplica un voltaje para que los iones fluyan a través del poro y generen una corriente eléctrica estable. Cuando una proteína o un péptido entra en el poro, bloquea parcialmente esa corriente. La profundidad de la caída de corriente, la duración y los detalles finos de su forma dependen del tamaño, la carga y la conformación (su plegamiento tridimensional) de la molécula. Mediante el diseño cuidadoso del poro—empleando proteínas diseñadas o materiales de estado sólido—los investigadores pueden confinar biomoléculas individuales el tiempo suficiente para crear “huellas” eléctricas ricas que distinguen no solo entre proteínas diferentes, sino también entre variantes sutiles del mismo biomarcador.
Leer cambios relevantes para la enfermedad, molécula a molécula
La revisión destaca cómo los nanoporos ya se han utilizado para resolver diferencias médicamente importantes que otros métodos tienen dificultades para detectar. Pueden distinguir péptidos que difieren en un solo aminoácido, detectar variantes de hemoglobina relacionadas con la enfermedad directamente en sangre y separar péptidos cortos de tipo hormonal que varían por un único bloque constituyente o incluso por la forma en espejo de ese bloque. Los nanoporos también pueden detectar modificaciones postraduccionales—pequeñas etiquetas químicas como grupos fosfato, azúcares o sulfatos—que ayudan a controlar si proteínas implicadas en el Alzheimer, el Parkinson, la coagulación sanguínea o el cáncer se comportan de forma normal o patológica. En algunos experimentos, una única enzima o proteína de unión se mantiene dentro del poro, y los cambios en su señal eléctrica revelan, en tiempo real, cómo se une a socios o realiza reacciones, exponiendo potencialmente rutas disfuncionales en la enfermedad.
Hacia pruebas rápidas junto a la cama del paciente
Puesto que cada evento de bloqueo corresponde a una molécula, los dispositivos de nanoporo pueden ser extremadamente sensibles, detectando apenas miles de copias de un biomarcador en un fluido complejo. Los autores discuten estrategias para superar obstáculos clave de uso clínico: aumentar la tasa de captura de moléculas raras, estabilizar membranas o usar poros híbridos sólido–biológicos, y aplicar aprendizaje automático para clasificar automáticamente patrones eléctricos complejos en categorías diagnósticas claras. También muestran cómo enfoques indirectos—como unir etiquetas de ADN o socios de unión—pueden amplificar señales débiles o permitir la medición simultánea de múltiples biomarcadores, preservando al mismo tiempo gran parte del detalle conformacional que hace únicos a los nanoporos.
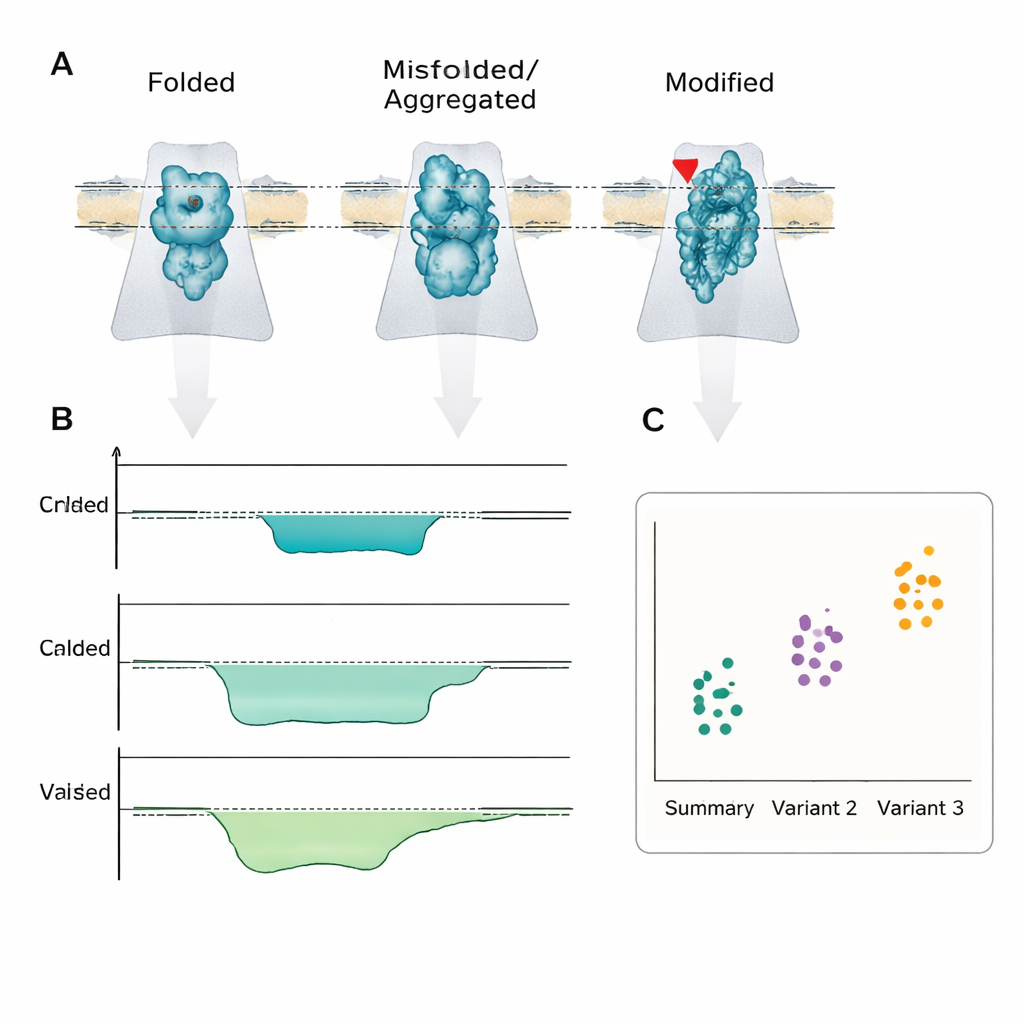
Lo que esto podría significar para los pacientes
El mensaje central es que la enfermedad a menudo está impulsada menos por la cantidad de proteína presente y más por qué forma o versión química está presente. La detección por nanoporo es una de las pocas tecnologías capaces de leer directamente estas diferencias a nivel de molécula única, con la rapidez y sencillez suficientes para integrarse en dispositivos portátiles. Aunque quedan importantes desafíos de ingeniería y estandarización, los autores sostienen que, al igual que los secuenciadores de ADN por nanoporo han entrado en la clínica, los sensores de proteínas y péptidos basados en nanoporos podrían finalmente proporcionar pruebas rápidas junto a la cama que no solo indiquen “algo va mal”, sino que también revelen el plegamiento o la modificación molecular exacta detrás de la condición del paciente.
Cita: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Palabras clave: detección por nanoporo, biomarcadores proteicos, diagnóstico en el punto de atención, modificaciones postraduccionales, enfermedades conformacionales