Clear Sky Science · es
Un largo camino hacia genomas de plantas medicinales fiables y completos
Por qué los mapas del ADN de las plantas importan para la salud humana
Muchos de los medicamentos más potentes de hoy —desde fármacos contra el cáncer como el paclitaxel hasta analgésicos como la morfina y el antipalúdico artemisinina— proceden de plantas. Sin embargo, para la mayoría de las plantas medicinales los científicos aún carecen de un “manual de instrucciones” completo de su ADN. Esta reseña explica cómo las nuevas tecnologías genómicas están transformando nuestra capacidad para leer esos manuales, por qué los genomas vegetales actuales a menudo siguen siendo incompletos o defectuosos, y cómo genomas verdaderamente precisos podrían desbloquear mejores fármacos, una producción más sostenible y una conservación mejorada de especies valiosas.
La promesa de leer los planos de las plantas medicinales
Durante milenios, las personas han confiado en remedios herbales, y la farmacología moderna sigue extrayendo en gran medida de los productos naturales vegetales. Estas moléculas especializadas —alcaloides, terpenoides, compuestos fenólicos y muchas otras— se sintetizan mediante vías metabólicas complejas codificadas en el ADN de las plantas. Hasta hace poco, los científicos tenían que reconstruir estas vías con herramientas lentas y laboriosas como el trazado isotópico y la clonación gen por gen. La llegada de la secuenciación de ADN asequible y de alto rendimiento cambió el panorama. Para febrero de 2025, se habían secuenciado genomas de 431 plantas medicinales (en 203 especies), lo que dio a los investigadores una forma sistemática de buscar genes de vías, entender cómo se regulan los compuestos valiosos y explorar cómo evolucionaron estas químicas.
Un auge en la secuenciación, pero muchos genomas imperfectos
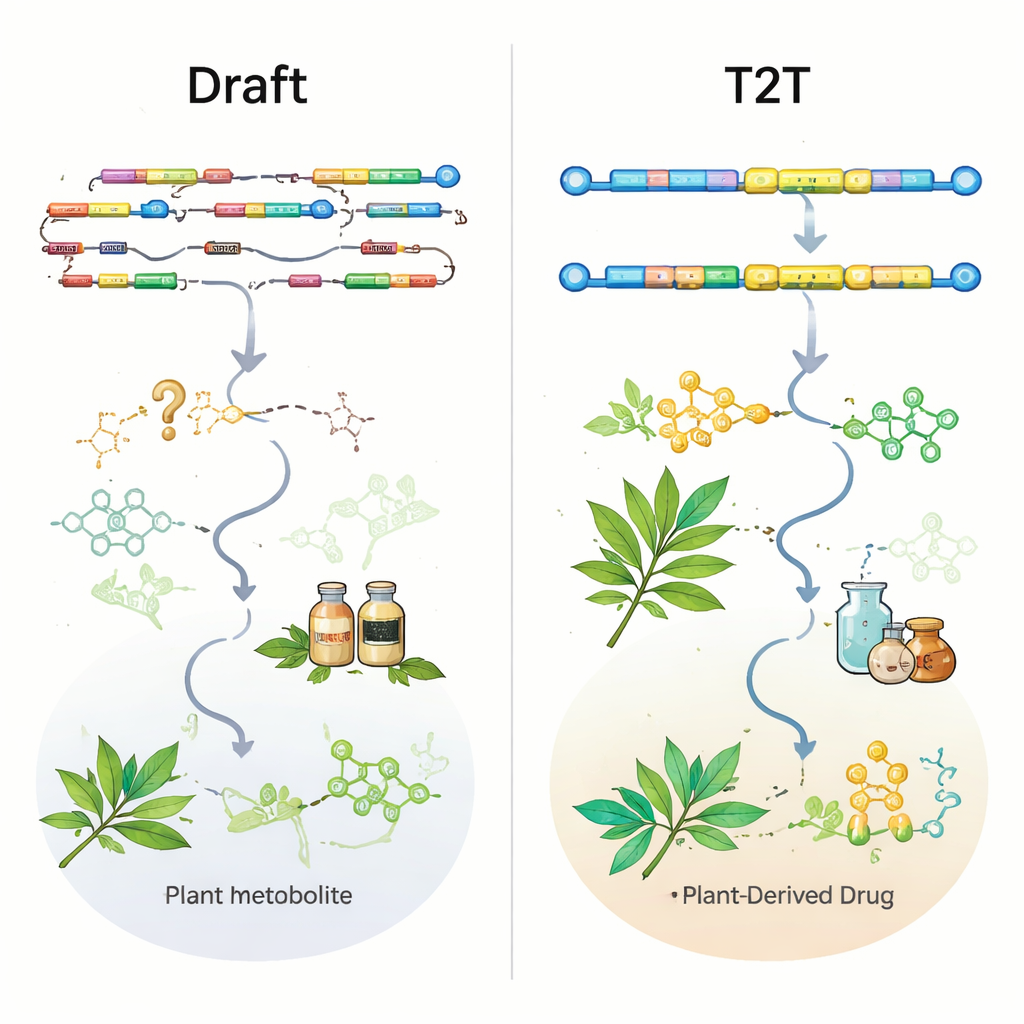
Las tecnologías de lecturas largas de PacBio y Oxford Nanopore, combinadas con datos de lecturas cortas de Illumina y métodos de mapeo a nivel cromosómico como Hi‑C, han mejorado drásticamente la calidad de los genomas vegetales. Casi la mitad de todos los ensamblajes de plantas medicinales se publicaron en los últimos tres años, y la mayoría de los genomas recientes ya se construyen a escala cromosómica. Sin embargo, la reseña muestra que la cantidad ha superado a la calidad. Más de la mitad de los genomas existen solo como una versión inicial, muchos permanecen a nivel de borrador, y solo 11 plantas medicinales tienen ensamblajes “de telómero a telómero” (T2T) sin huecos que capturen completamente los centrómeros y otras regiones repetitivas. Métricas estándar como N50 (una medida de contigüidad) y las puntuaciones BUSCO (una medida de genes conservados) parecen prometedoras en general, pero pueden enmascarar lagunas críticas precisamente donde residen genes biosintéticos clave.
Lagunas ocultas donde deberían estar los genes de la medicina
Para evaluar cuán útiles son realmente los genomas actuales, los autores examinaron genes de vías conocidos y validados experimentalmente en nueve plantas medicinales bien estudiadas. Incluso en algunos ensamblajes a nivel cromosómico, enzimas importantes para compuestos como los ginsenósidos en el ginseng o la artemisinina en Artemisia annua estaban completamente ausentes o solo parcialmente capturadas. En otros casos, los genes estaban presentes en la secuencia genómica cruda pero ausentes o truncados en las anotaciones génicas oficiales, lo que dificultaba encontrarlos. Un ejemplo llamativo proviene de la hierba productora de cumarinas Peucedanum praeruptorum: un genoma cromosómico más antiguo rompió un gen clave y pasó por alto otros dos; un ensamblaje T2T más reciente no solo restauró esos genes sino que además reveló que varios de ellos se sitúan juntos en un cúmulo génico biosintético muy compacto. Este tipo de mapa de cúmulos es exactamente lo que los investigadores necesitan para diseñar plantas o microbios que produzcan medicamentos con mayor eficiencia.
Por qué los genomas de las plantas son tan difíciles de ensamblar
Las plantas medicinales plantean desafíos especiales que van más allá de los de muchas especies de cultivo. Sus genomas a menudo presentan altos niveles de heterocigosidad (muchas diferencias de ADN entre las dos copias de cada cromosoma), poliploidía frecuente (múltiples juegos de cromosomas) y grandes fracciones de ADN repetitivo—características que confunden a los algoritmos de ensamblaje y provocan rupturas o uniones incorrectas. Alrededor de un tercio de las plantas medicinales secuenciadas tienen genomas con más del 70 % de contenido repetitivo, y más de una cuarta parte muestran heterocigosidad muy alta. Criar líneas altamente endogámicas o aislar tejido haploide puede ayudar, pero esto es lento, caro o biológicamente difícil para muchas especies. Nuevas estrategias que ensamblan cada haplotipo parental por separado, y algoritmos más potentes ajustados a genomas ricos en repeticiones y poliploides, están empezando a aliviar estos obstáculos, pero aún no son rutinarios.
De los genomas a nuevos medicamentos y direcciones futuras
Cuando los genomas son lo bastante buenos, se convierten en motores poderosos de descubrimiento. Los investigadores pueden combinar datos de genoma completo con transcriptómica, metabolómica y biología sintética para identificar enzimas, genes reguladores y cúmulos génicos biosintéticos que controlan la producción de compuestos de alto valor. Estas ideas ya han permitido la reconstrucción de vías vegetales complejas—como las del vinblastina, el paclitaxel y muchos otros fármacos—en levaduras o plantas modelo, abriendo un camino hacia la bioproducción estable y a gran escala. De cara al futuro, los autores abogan por un cambio de “un genoma aproximado por especie” a múltiples ensamblajes de alta calidad, T2T y resueltos por haplotipo que capturen la diversidad intraespecífica, al estilo de los pan‑genomas en la investigación de cultivos. Acoplar estos genomas de referencia con re‑secuenciados a gran escala, fenotipado avanzado y las emergentes transcriptómicas espacial y de célula única debería iluminar cómo el ambiente, el tipo celular y las redes génicas interactúan para moldear la química medicinal.
Qué significa esto para los pacientes y el planeta
El mensaje central de la reseña es que genomas fiables y completos de plantas medicinales no son un lujo; son la base para convertir siglos de conocimiento herbal en terapias modernas y precisas. Mejores genomas ayudarán a los científicos a encontrar pasos faltantes en las vías de los fármacos, diseñar suministros más seguros y abundantes de medicamentos críticos e identificar especies alternativas que puedan producir los mismos compuestos. También guiarán la conservación y el uso sostenible de plantas medicinales amenazadas, la mayoría de las cuales aún carecen de recursos genómicos. En resumen, completar el trabajo de mapear con precisión estos genomas podría acelerar el descubrimiento de fármacos, estabilizar las cadenas de suministro y preservar la diversidad botánica—todo lo cual beneficia en última instancia la salud humana.
Cita: Cheng, LT., Wang, ZL., Zhu, QH. et al. A long road ahead to reliable and complete medicinal plant genomes. Nat Commun 16, 2150 (2025). https://doi.org/10.1038/s41467-025-57448-8
Palabras clave: genómica de plantas medicinales, conjuntos génicos biosintéticos, genomas de telómero a telómero, biosíntesis de productos naturales, biología sintética