Clear Sky Science · es
Iluminando el impacto de la acetilación N-terminal: desde la proteína hasta la fisiología
Cómo pequeñas etiquetas químicas pueden alterar el comportamiento de las proteínas
Cada célula de tu cuerpo está repleta de proteínas que deben plegarse correctamente, dirigirse al lugar adecuado, ensamblarse en máquinas moleculares y ser eliminadas cuando están dañadas. Este artículo de revisión explora un cambio químico sutil pero enormemente común en un extremo de muchas proteínas —llamado acetilación N-terminal— y muestra cómo esta pequeña “tapa” ayuda a controlar desde el crecimiento celular y las respuestas al estrés hasta el desarrollo cardíaco y la función cerebral.
La tapa proteica que la mayoría de nosotros no conocía
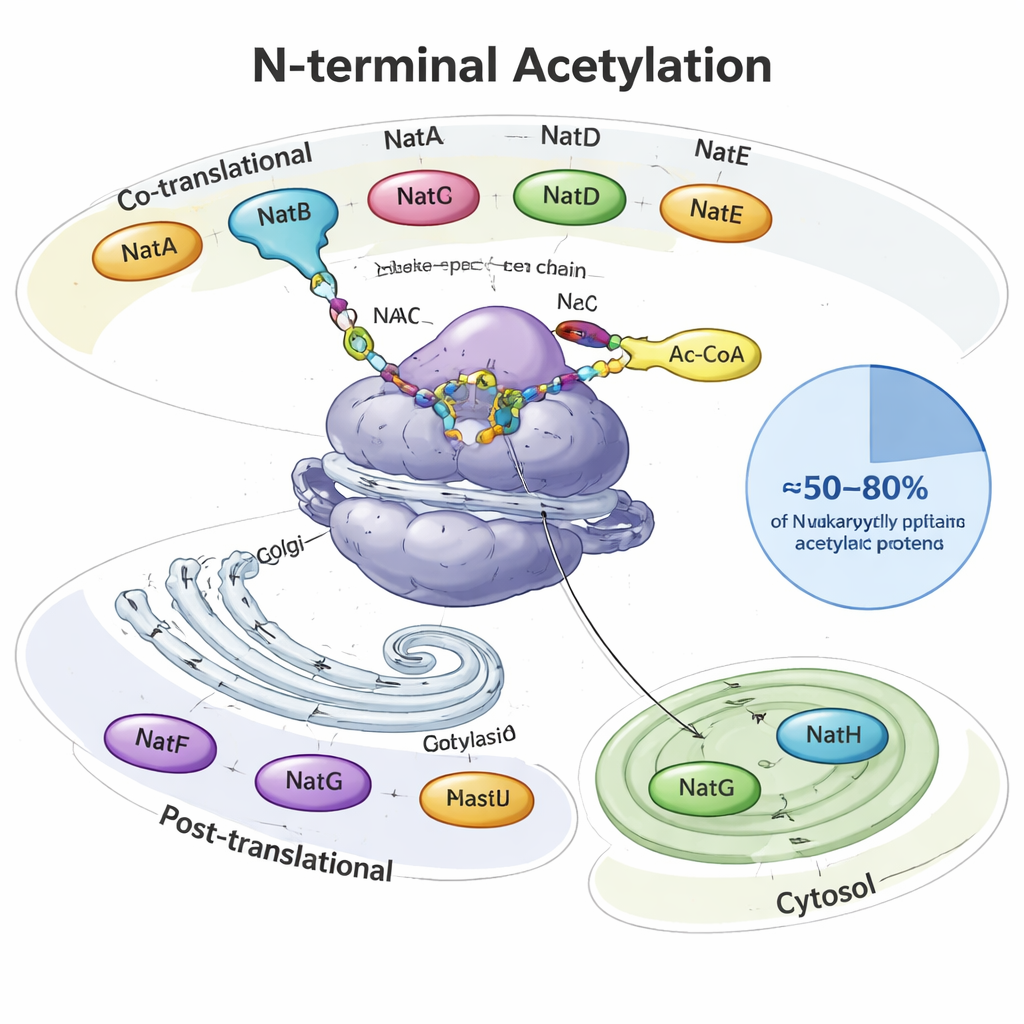
Cuando se sintetiza una proteína, emerge de la maquinaria de producción celular, el ribosoma, como un hilo en crecimiento. En su inicio —el extremo N— muchas proteínas eucariotas reciben un grupo acetilo, una diminuta tapa de dos carbonos. Enzimas especializadas llamadas acetiltransferasas N-terminales (NATs) realizan este trabajo, usando una molécula metabólica común (acetil‑CoA) como donante. En levaduras, plantas y animales, ocho tipos principales de NAT (NatA–NatH) se reparten la tarea. Algunas actúan mientras la proteína aún se está produciendo, otras actúan después y se localizan en lugares específicos como el aparato de Golgi o los plastidios vegetales. En conjunto modifican aproximadamente entre la mitad y cuatro quintas partes de todas las proteínas celulares, cada NAT reconociendo secuencias iniciales preferidas de dos a cuatro aminoácidos.
Muchas enzimas, cada una con su especialidad
NatA, NatB y NatC son las trabajadoras principales, actuando directamente en el ribosoma y cubriendo grandes porciones del “acetiloma N-terminal”. Solo NatA puede modificar alrededor del 40% de las proteínas humanas, normalmente aquellas cuya metionina inicial ha sido recortada. NatB y NatC actúan sobre proteínas que conservan su metionina inicial, pero difieren en qué aminoácidos vecinos prefieren. Otras NATs son más selectivas: NatD se centra en unas pocas histonas que empaquetan el ADN, NatF apunta a proteínas transmembrana en el Golgi, NatG actúa dentro de plastidios vegetales, y NatH (NAA80) completa un proceso especial de maduración en dos pasos sobre la actina, un componente principal del esqueleto celular. El artículo reúne estudios estructurales y bioquímicos que muestran cómo subunidades accesorias anclan estas enzimas a los ribosomas o membranas y afinan sobre qué proteínas actúan.
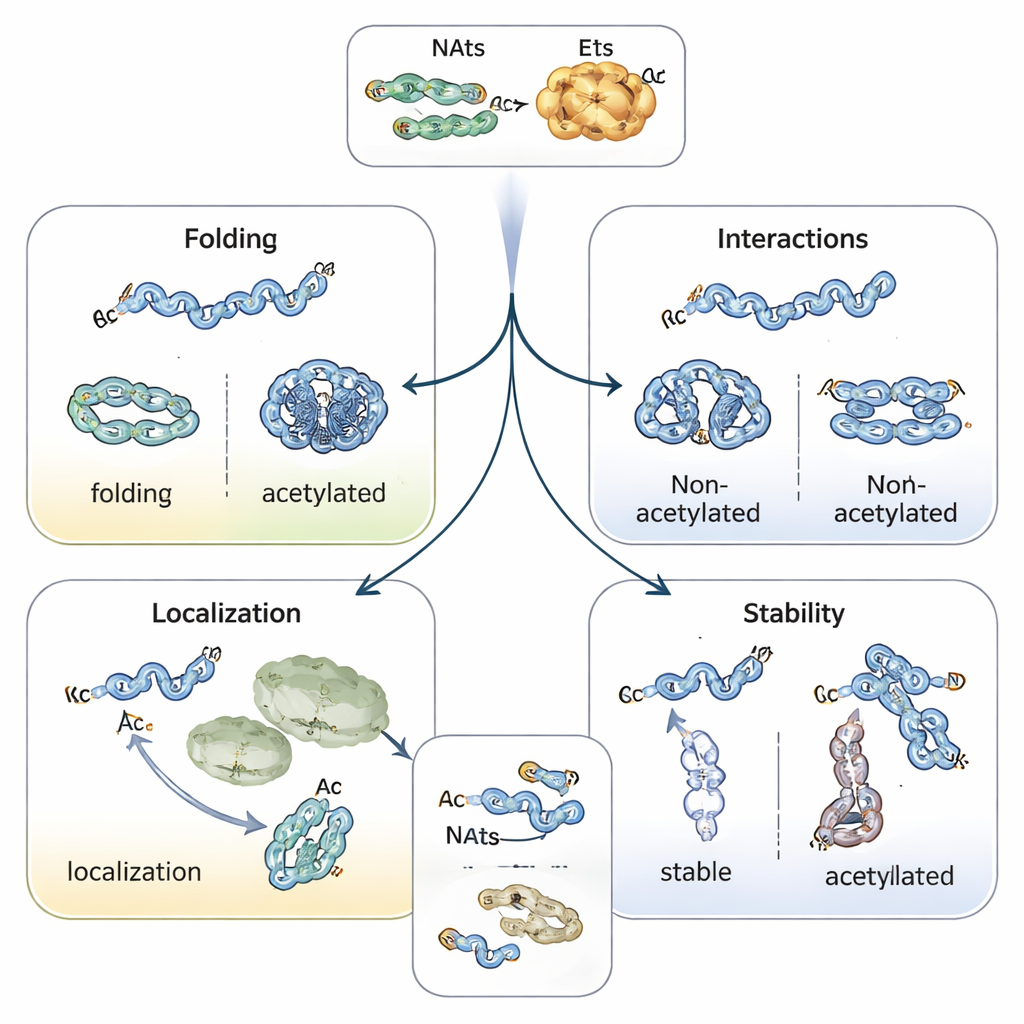
Dirección del plegamiento, la localización y la vida útil de las proteínas
Agregar una tapa acetilo cambia la naturaleza química del inicio de la proteína, estabilizando a menudo estructuras helicoidales e influyendo en cómo se pliegan las proteínas. Por ejemplo, la proteína vinculada al Parkinson alfa‑sinucleína tiende a agregarse menos y adoptar una conformación más segura cuando su extremo N está acetilado. La tropomiosina, una compañera de la actina, se une y regula los filamentos de actina mucho mejor cuando está correctamente acetilada. En plantas y animales, la acetilación N-terminal puede funcionar como una especie de etiqueta de dirección, ayudando a las proteínas a localizarse en cloroplastos, lisosomas o el Golgi. Quizá lo más llamativo es su papel en determinar cuánto tiempo sobreviven las proteínas: un extremo N desprotegido puede ser interpretado como una “señal de degradación” por las enzimas que etiquetan con ubiquitina, mientras que la acetilación puede enmascarar esa señal y estabilizar la proteína —o, en algunos casos, crear una etiqueta condicional que solo se reconoce cuando la proteína está mal plegada o no forma el complejo correcto.
De la fisiología celular al desarrollo y la enfermedad
Dado que la acetilación N-terminal afecta a tantas proteínas, alterar las NATs tiene consecuencias amplias para organismos enteros. Eliminar NatA, NatB o NatC en especies modelo a menudo provoca defectos graves en el desarrollo, respuestas alteradas al estrés o incluso letalidad, mientras que enzimas más especializadas como NatF y NatH generan problemas más específicos como calcificaciones cerebrales o pérdida auditiva. En humanos, mutaciones heredadas en varios genes NAT subyacen a síndromes raros de neurodesarrollo con discapacidad intelectual, defectos cardíacos o debilidad muscular. La misma maquinaria está frecuentemente sobreactiva en cánceres, donde niveles elevados de NAT se correlacionan con mal pronóstico y pueden impulsar el crecimiento tumoral, la metástasis y la resistencia a terapias. Los cambios en la acetilación N-terminal también influyen en proteínas propensas a agregarse como la alfa‑sinucleína y la huntingtina, vinculando esta modificación a mecanismos de enfermedades neurodegenerativas.
Direcciones futuras y promesa médica
Los autores concluyen que, aunque ahora conocemos la mayoría de las enzimas centrales que añaden estas tapas N‑terminales, todavía entendemos solo una fracción de los objetivos proteicos específicos y de las reglas regulatorias. Un tema principal es que la acetilación en el inicio de la proteína a menudo la protege de una destrucción prematura, al tiempo que crea señales dependientes del contexto para el control de calidad. Identificar qué ligasas de ubiquitina leen qué patrones N‑terminales y descubrir si existe alguna enzima capaz de eliminar estas tapas son preguntas clave abiertas. Dado que las NATs se sitúan en la intersección de la estabilidad proteica, la regulación génica y las respuestas al estrés celular, los inhibidores selectivos de NAT —y quizás en el futuro herramientas que modifiquen la acetilación N‑terminal de proteínas específicas relacionadas con la enfermedad— emergen como vías prometedoras para nuevas terapias en cáncer, enfermedades cardíacas y neurodegeneración.
Cita: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Palabras clave: modificación de proteínas, acetilación N-terminal, control de calidad de proteínas, enfermedad neurodegenerativa, biología del cáncer