Clear Sky Science · es
La metilación m6A del ARN modula la respuesta antiviral en la enfermedad celíaca
Cuando un virus y el gluten se alían
La enfermedad celíaca suele entenderse como un problema alimentario sencillo: comer gluten y el intestino se daña. Este estudio revela una historia más compleja, en la que un virus intestinal común y una pequeña etiqueta química en nuestras moléculas de ARN actúan conjuntamente para empujar al sistema inmune hacia un daño persistente. Entender esta capa oculta de control puede ayudar a explicar por qué solo algunas personas desarrollan enfermedad celíaca y señalar nuevos tratamientos que vayan más allá de la dieta sin gluten. 
Una etiqueta oculta en nuestros mensajes genéticos
Nuestras células leen genes constantemente y los copian en ARN, breves “mensajes” que indican a la célula qué proteínas producir. Esos mensajes no son fijos; pueden llevar marcas químicas que actúan como resaltadores, cambiando la intensidad con la que se lee un mensaje. Una de las marcas más comunes se llama m6A, un pequeño cambio en las letras del ARN. Se sabe que los virus alteran estas marcas en células infectadas, y trabajos previos ya habían vinculado m6A con la forma en que el gluten desencadena inflamación en el intestino celíaco. Los autores de este artículo se preguntaron si un cambio en m6A inducido por virus podría ayudar a voltear al sistema inmune de la tolerancia alimentaria al ataque.
Evidencia en pacientes con enfermedad celíaca
Los investigadores examinaron primero sangre y biopsias intestinales de personas con enfermedad celíaca activa y de controles no celíacos. Encontraron que los pacientes celíacos tenían niveles más altos de anticuerpos contra reovirus, un virus de ARN de doble cadena que infecta el intestino, lo que sugiere una exposición más frecuente o más intensa. En el tejido intestinal de estos pacientes, genes clave de alerta antiviral, especialmente uno llamado IRF7, estaban activados a niveles mayores, junto con moléculas inflamatorias como STAT1 y la quimiocina atractora de células inmunes CXCL10. Al mismo tiempo, la maquinaria que añade y lee las marcas m6A mostraba mayor actividad, y los niveles totales de m6A en el ARN eran más altos. La expresión de genes antivirales aumentó y disminuyó en paralelo con genes relacionados con m6A, lo que sugiere que el mismo sistema de control podría estar impulsando tanto la defensa viral como el daño autoinmune.
Cómo el gluten amplifica la alarma viral
Para indagar causa y efecto, el equipo construyó un modelo similar a la celiaquía en células intestinales cultivadas en el laboratorio. Imitaron una infección viral usando un ARN de doble cadena sintético y luego añadieron fragmentos de gluten digerido similares a los que aparecen en el intestino después de una comida. El análogo viral por sí solo elevó tanto IRF3 como IRF7, dos interruptores maestros de las respuestas antivirales. Pero cuando se añadió gluten encima, IRF7 mostró un aumento adicional notable, mientras que IRF3 no. Los investigadores descubrieron que, en estas condiciones, las marcas m6A aumentaron en una región específica del ARN de IRF7, y que ese ARN interactuaba físicamente con una enzima que escribe m6A (METTL3) y con una que la borra (ALKBH5). Aumentar m6A, ya sea añadiendo más METTL3 o reduciendo ALKBH5, elevó aún más los niveles de IRF7, vinculando directamente la sinergia virus‑más‑gluten con esta modificación del ARN. 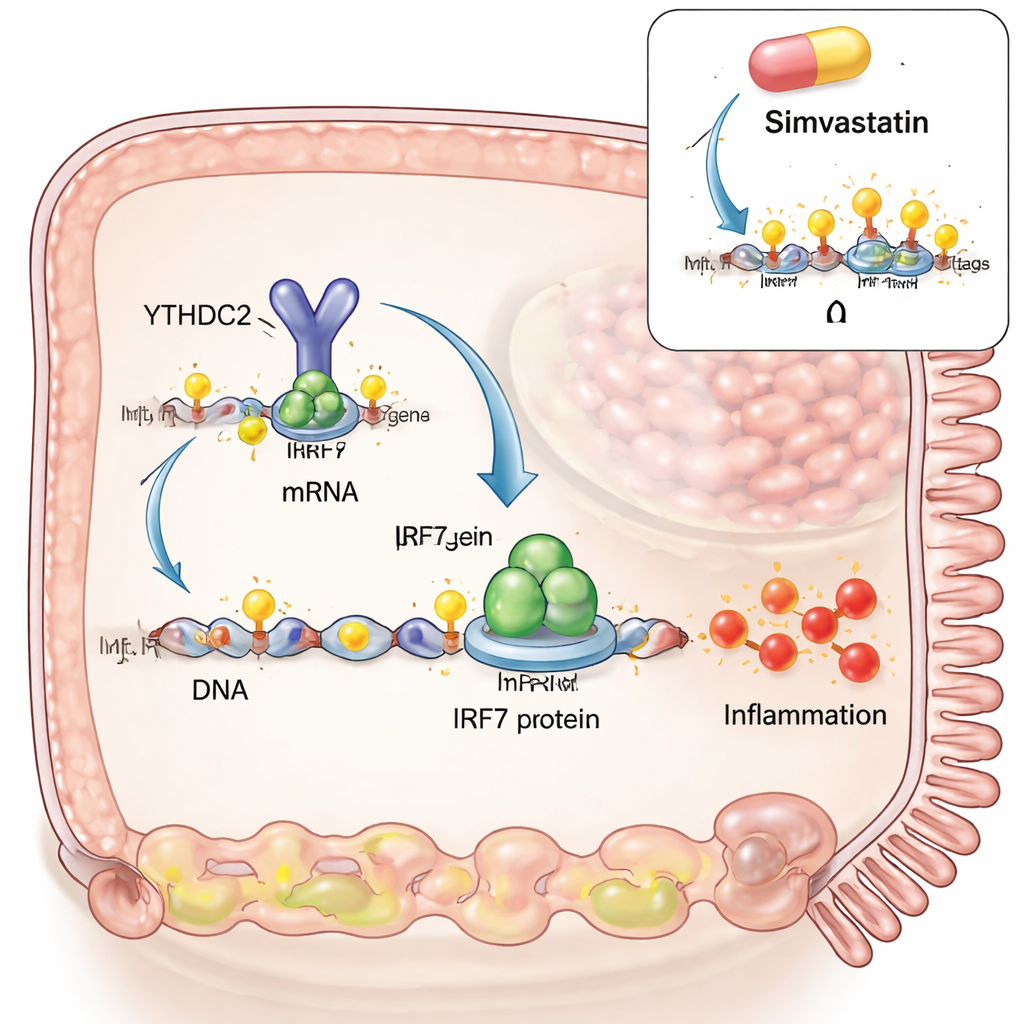
El intermediario molecular y un fármaco sorprendente
A continuación, los autores investigaron cómo las marcas m6A en el ARN de IRF7 cambian efectivamente el comportamiento celular. Diseñaron una versión del ARN de IRF7 con el mismo código proteico pero sin los sitios de m6A. Ese ARN produjo cantidades similares de transcrito, pero mucha menos proteína IRF7, y no activó los genes inflamatorios descendentes como STAT1 y CXCL10. El eslabón perdido fue una proteína lectora llamada YTHDC2, que normalmente se une a m6A dentro de la región codificante y ayuda a impulsar la traducción eficiente en proteína. Sin los sitios de m6A, YTHDC2 ya no podía unirse al ARN de IRF7. Bloquear la enzima escritora METTL3 en el modelo celular redujo la proteína IRF7 y CXCL10, disminuyendo la salida inflamatoria. Un fármaco reductor del colesterol, la simvastatina, que se ha mostrado recientemente capaz de reducir m6A en otros tejidos, también disminuyó m6A en el ARN de IRF7, redujo la proteína IRF7 en células y atenuó genes relacionados con IRF7 en biopsias intestinales de pacientes celíacos obtenidas y cultivadas ex vivo. Comparaciones de gran escala de expresión génica sugirieron que la simvastatina desplaza el tejido celíaco hacia un perfil más parecido al de pacientes en dieta sin gluten.
Qué significa esto para las personas con enfermedad celíaca
Este trabajo dibuja un panorama en el que un virus intestinal y el gluten actúan conjuntamente sobre una capa de control del ARN muy fina. En individuos susceptibles, la infección viral parece aumentar el etiquetado m6A del ARN de IRF7 en células intestinales. La exposición al gluten amplifica esa señal etiquetada, llevando a más proteína IRF7, alarmas antivirales más intensas y niveles más altos de mensajeros inflamatorios que contribuyen al ataque autoinmune sobre el revestimiento intestinal. Al reducir las marcas m6A —ya sea genéticamente o con un fármaco como la simvastatina— la reacción en cadena puede suavizarse, al menos en modelos de laboratorio y ex vivo. Para el público general, el mensaje clave es que la enfermedad celíaca no trata solo de lo que se come, sino también de cómo las infecciones y las sutiles marcas químicas en el ARN moldean la decisión del sistema inmune de tolerar o atacar. Apuntar a estas marcas de ARN podría algún día complementar la dieta sin gluten e inspirar nuevos tratamientos para una gama más amplia de enfermedades autoinmunes.
Cita: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Palabras clave: enfermedad celíaca, metilación del ARN, inmunidad antiviral, IRF7, simvastatina