Clear Sky Science · es
CRISPR-AuNP: optimización fisicoquímica de una plataforma de nanopartículas de oro para la edición génica no viral, modular y rentable en CPHs
Llevar la edición génica a más pacientes
Herramientas de edición genética como CRISPR ya han cambiado la vida de personas con enfermedades sanguíneas hereditarias, pero los tratamientos siguen siendo costosos, técnicamente exigentes y en gran medida limitados a unos pocos centros especializados. Este artículo describe una nueva forma de entregar CRISPR a las células madre formadoras de sangre mediante partículas diminutas a base de oro que se pueden mezclar en una bancada de laboratorio en apenas un par de horas. El objetivo es hacer que los enfoques de edición génica potentes sean más simples, baratos y fáciles de desplegar en más lugares del mundo.
Por qué importan las células madre sanguíneas
Las células madre y progenitoras formadoras de sangre viven en la médula ósea y reponen continuamente todos los distintos tipos de células sanguíneas del organismo. Si los médicos pueden corregir de forma segura las mutaciones causantes de enfermedad en estas células, un tratamiento único podría proporcionar una cura de por vida para afecciones como la anemia falciforme y ciertas inmunodeficiencias. Hoy, la forma más común de introducir CRISPR en estas células depende de la electroporación, un proceso que utiliza pulsos eléctricos para abrir poros en las membranas celulares. Aunque potente, la electroporación es agresiva para las células, requiere equipos caros y reactivos especializados, y no se escala ni exporta fácilmente a entornos con recursos limitados. Los vectores virales más seguros son excelentes para muchas terapias génicas, pero son menos adecuados para la entrega de CRISPR porque siguen produciendo las herramientas de edición durante demasiado tiempo, lo que aumenta el riesgo de cambios fuera del objetivo.
Construir un vehículo de entrega diminuto de oro
Los investigadores se propusieron mejorar un sistema de nanopartículas de oro previamente descrito que portaba componentes de CRISPR en su superficie. En diseños anteriores, el ARN que guía a la proteína de corte de CRISPR hacia su blanco estaba anclado directamente al núcleo de oro y luego se emparejaba con la proteína Cas9. Esto funcionó razonablemente bien para un tipo de enzima CRISPR, pero rindió mal con Cas9, que es central en muchas estrategias terapéuticas. Al examinar de cerca cómo se comportan Cas9 y su ARN guía bajo las condiciones ácidas usadas durante el ensamblaje de las partículas, el equipo descubrió que el dímero de ARN guía se volvía inestable sobre la superficie de oro, lo que llevaba a que quedara poco o ningún Cas9 activo unido a la partícula. La microscopía confocal también sugirió que el recubrimiento polimérico destinado a ayudar a las partículas a escapar de compartimentos celulares se desprendía antes de poder cumplir su función.
Rediseño progresivo de la plataforma
Para superar estos problemas, los científicos reconstruyeron el sistema desde cero en tres etapas. Primero, en lugar de anclar ARN desnudo al oro y luego añadir la proteína, formaron complejos ribonucleoproteicos completos de CRISPR (proteína más ARN guía) antes de ponerlos en contacto con la superficie de oro. Identificaron una condición ligeramente ácida que permitía que estos complejos se unieran a las partículas manteniendo al mismo tiempo la actividad de la proteína de corte. A continuación, envolvieron las partículas cargadas con polímeros especialmente diseñados que combinaban cadenas cargadas positivamente—necesarias para escapar de los compartimentos celulares—con segmentos flexibles y hidrófilos de polietilenglicol que evitan la agregación. Midiendo el tamaño, la carga superficial y el contenido proteico, demostraron que podían cargar de forma reproducible decenas de complejos CRISPR por partícula manteniendo la estabilidad en solución.
Rompiendo las defensas celulares
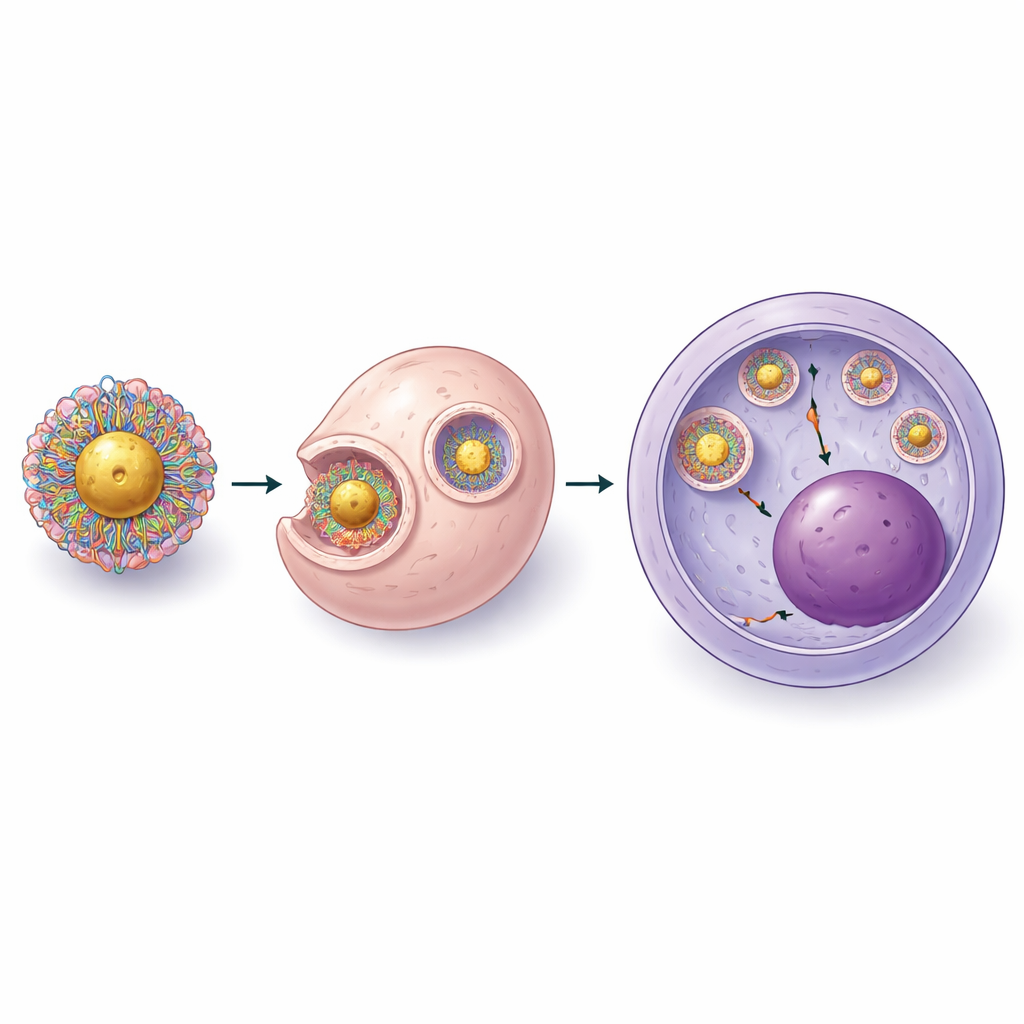
Incluso con una mejor carga, las partículas de segunda generación seguían encontrando un obstáculo clave: sacar a CRISPR de las vesículas internas de la célula hacia la parte donde reside el ADN. Por ello, el equipo afinó sistemáticamente la química de la capa polimérica y la proporción entre grupos positivos del polímero y grupos negativos del complejo CRISPR. Descubrieron que añadir más cadenas cortas de polietilenglicol y un número controlado de anclas que contienen azufre mejoraba tanto la estabilidad de las partículas como su capacidad para perturbar las membranas endosómicas sin dañar las células. En el diseño final de tercera generación, primero crearon complejos compactos de CRISPR y polímero, y luego los unieron a núcleos de oro concentrados. La microscopía electrónica mostró una fina capa de CRISPR y polímero alrededor de cada esfera de oro, y la imagen en células madre vivas confirmó que la carga podía escapar al interior celular y alcanzar el núcleo.
Resultados de edición con múltiples herramientas CRISPR
Para evaluar el rendimiento de las partículas optimizadas, los investigadores dirigieron su actuación contra un gen llamado beta-2-microglobulina, que produce una proteína presente en la superficie de casi todas las células sanguíneas y que puede medirse fácilmente por citometría de flujo. Usando su plataforma de oro de tercera generación, lograron más del 10% de interrupciones precisas de este gen en células madre y progenitoras sanguíneas humanas primarias—niveles considerados relevantes para muchas aplicaciones terapéuticas—manteniendo una alta supervivencia celular. Aunque esta eficiencia es menor que la alcanzable con electroporación, el sistema basado en oro no requirió equipo especializado y causó un estrés mínimo a las células. Es importante destacar que la misma plataforma pudo usarse con diferentes proteínas CRISPR, incluidas Cas9, Cas12a y una enzima más reciente llamada Cas12a-M29-1, con niveles de edición similares y sin toxicidad detectable, lo que subraya la naturaleza modular del diseño.
Qué podría significar esto para terapias futuras
En términos sencillos, este trabajo muestra que es posible construir un transportador pequeño y cuidadosamente diseñado a base de oro que puede llevar herramientas CRISPR a células madre sanguíneas sensibles sin electricidad ni virus, usando materiales comerciales por menos de setenta dólares por cada millón de células. Si bien se necesitan mejoras adicionales para igualar la eficiencia de los mejores métodos clínicos actuales, particularmente para enfermedades que exigen niveles muy altos de células corregidas, esta plataforma ensamblada en bancada reduce las barreras prácticas para realizar edición génica sofisticada. Con refinamientos continuos y pruebas de seguridad, tales nanopartículas podrían ayudar a extender los beneficios de las terapias basadas en CRISPR más allá de los centros especializados, haciendo que los tratamientos curativos sean más accesibles para pacientes en todo el mundo.
Cita: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Palabras clave: Edición génica CRISPR, nanopartículas de oro, células madre hematopoyéticas, entrega no viral, nanomedicina