Clear Sky Science · es
Replanteando la genómica de la distrofia muscular facioescapulohumeral en la era del telómero a telómero: trampas en el paisaje oculto de los repeticiones D4Z4
Por qué importa esta historia sobre una enfermedad muscular
La distrofia muscular facioescapulohumeral (FSHD) es una de las enfermedades hereditarias de desgaste muscular más comunes, que a menudo debilita los músculos de la cara y los hombros en adultos jóvenes por lo demás sanos. Durante años, los científicos se centraron en un único tramo de ADN cercano al extremo del cromosoma 4 como el culpable. Este nuevo estudio muestra que el panorama es mucho más complejo: repeticiones de ADN similares están dispersas por todo el genoma y muchas pruebas de laboratorio estándar no pueden diferenciarlas. Entender este paisaje oculto es esencial para un diagnóstico preciso, mejor investigación y, en última instancia, terapias más seguras.
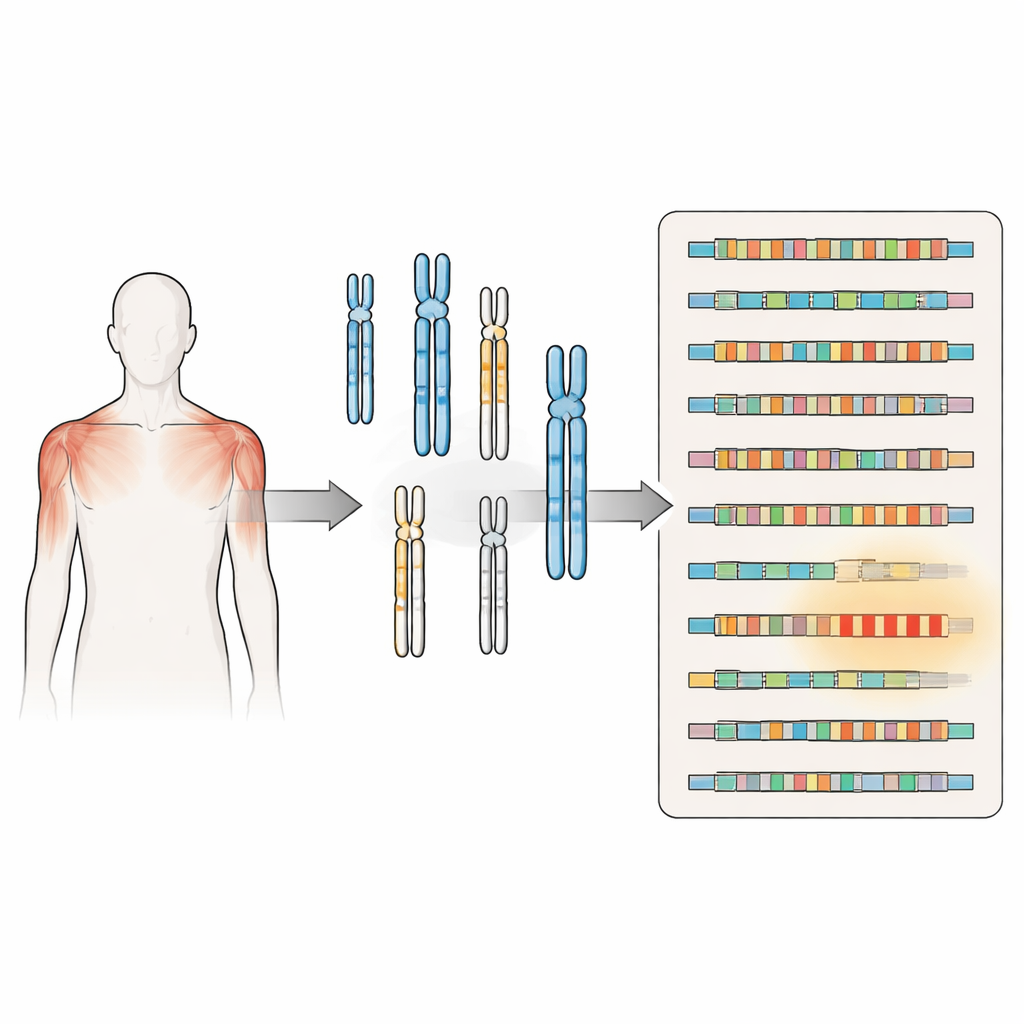
Una mirada más detallada a un trastorno muscular desconcertante
La FSHD lleva tiempo asociada con el acortamiento de una secuencia repetida de ADN llamada D4Z4 cerca del extremo del cromosoma 4. Cuando esta región de repeticiones se reduce por debajo de cierto tamaño y se sitúa sobre un fondo genético concreto, permite la producción de una proteína llamada DUX4, que puede dañar las células musculares. Una segunda forma de la enfermedad surge cuando los genes que normalmente mantienen esta región fuertemente empaquetada y silenciada están mutados, permitiendo de nuevo la aparición de DUX4. Ambas vías convergen en el mismo problema: un gen que debería estar en gran parte apagado en el músculo adulto se vuelve esporádicamente activo, contribuyendo a la debilidad y la atrofia muscular.
Repeticiones ocultas en todo el genoma
Los mapas del genoma humano previos eran incompletos, especialmente en regiones ricas en ADN repetitivo en los extremos de los cromosomas y cerca de los centrómeros. Utilizando el nuevo ensamblaje del genoma humano telómero a telómero, que llena estas lagunas, los autores volvieron a escanear todo el genoma usando la secuencia D4Z4 del cromosoma 4 como plantilla de búsqueda. Descubrieron agrupaciones y copias aisladas de repeticiones similares a D4Z4 en al menos diez cromosomas adicionales. Algunas de estas repeticiones son estructuralmente completas y se sitúan junto a señales que podrían estabilizar ARN similares a DUX4, lo que sugiere que podrían producir proteínas relacionadas o moléculas de ARN en las condiciones adecuadas.
Cuando las pruebas de laboratorio ven más de un lugar a la vez
La investigación y el diagnóstico de la FSHD suelen basarse en pruebas que amplifican fragmentos específicos de ADN o ARN con secuencias cortas de cebadores, una estrategia conocida como PCR. Estos cebadores se diseñaron originalmente bajo la suposición de que las repeticiones D4Z4 existían solo en los cromosomas 4 y 10. Combinando predicciones informáticas con experimentos en células que portan cromosomas humanos individuales, los autores muestran que muchos conjuntos de cebadores ampliamente usados se unen no solo a la región vinculada a la enfermedad en el cromosoma 4, sino también a repeticiones semejantes dispersas por el genoma. Los cebadores dirigidos al principal exón de DUX4 o a los ARN largos no codificantes vecinos amplifican con frecuencia productos de varios cromosomas a la vez, haciendo imposible saber dónde se originó realmente una señal determinada.
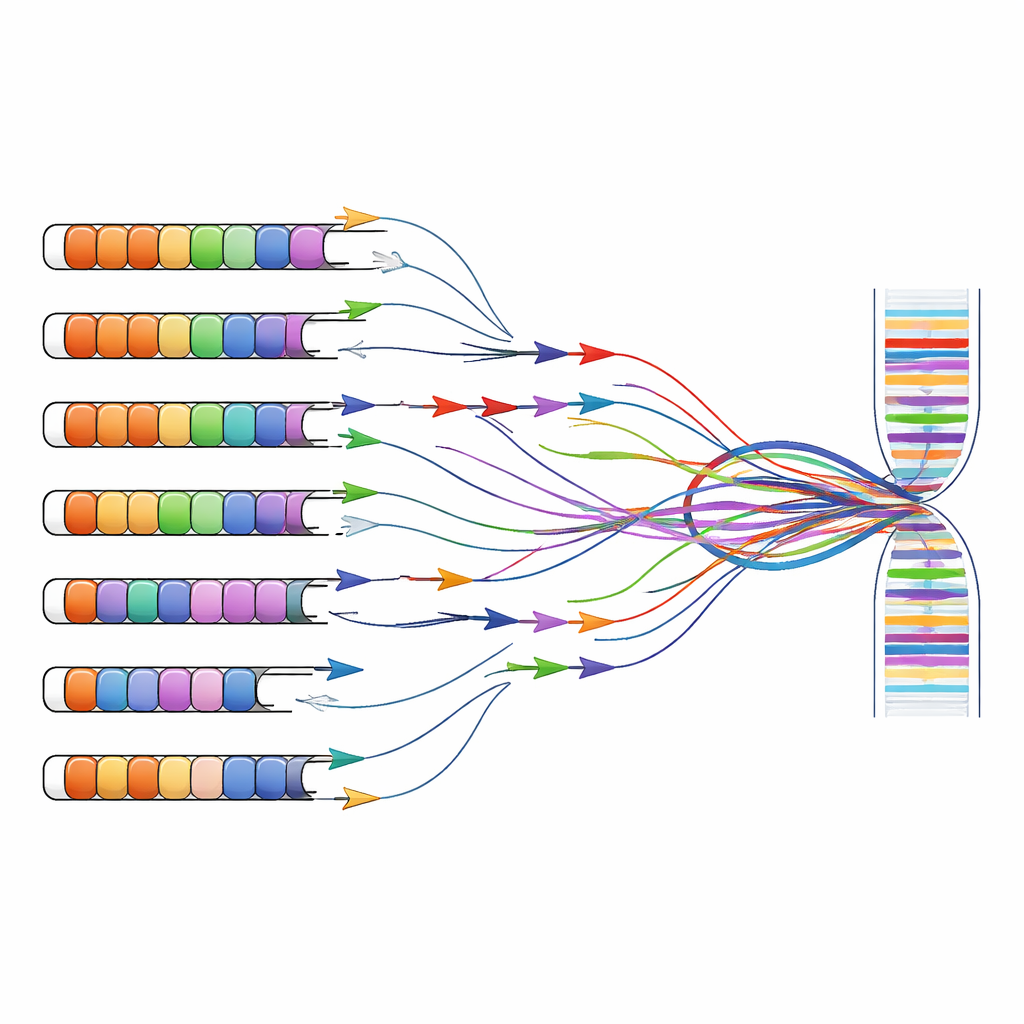
Replantear herramientas diagnósticas y de investigación
Este problema de múltiples ubicaciones se extiende más allá de la investigación básica hasta la clínica. Pruebas más recientes que miden la metilación del ADN (una marca química asociada al silenciamiento génico) o que usan secuenciación de lecturas cortas a menudo agrupan señales de muchas repeticiones casi idénticas. Como resultado, las mediciones de la “metilación de D4Z4” o de los “transcritos de DUX4” en conjuntos de datos públicos pueden reflejar en realidad una mezcla de contribuciones del cromosoma 4, del cromosoma 10 y de otros sitios. Los autores sostienen que, para vincular correctamente cambios genéticos con síntomas, los científicos deben ahora adoptar métodos conscientes de las repeticiones que distingan loci individuales—por ejemplo, la secuenciación de lecturas largas que pueda abarcar bloques de repeticiones enteros y capturar sus patrones de metilación y productos de ARN en su totalidad.
Qué significa esto para los pacientes y las terapias futuras
El estudio no invalida el papel central de la región D4Z4 acortada en el cromosoma 4 en la FSHD, pero muestra que esa región vive en un vecindario concurrido de secuencias similares. Señales que antes se asumía que probaban actividad en el locus de la enfermedad pueden de hecho proceder en parte de sus primos genómicos. Para los pacientes, esto significa que las herramientas diagnósticas más fiables serán aquellas que resuelvan físicamente el cromosoma exacto y el arreglo de repeticiones implicado, en lugar de confiar únicamente en lecturas indirectas. Para investigadores y desarrolladores de fármacos, subraya la necesidad de diseños altamente específicos que eviten dirigir por accidente repeticiones inocuas en otras partes del genoma. En la era del telómero a telómero, entender y tratar la FSHD dependerá de ver el paisaje completo de repeticiones, no solo un único punto de referencia.
Cita: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Palabras clave: distrofia muscular facioescapulohumeral, repeticiones D4Z4, DUX4, genoma telómero a telómero, diagnóstico genético