Clear Sky Science · es
Moléculas superatómicas: uniones entre superátomos, naturales y no naturales, que se comportan como átomos
Bloques diminutos que se comportan como átomos
La mayoría aprendemos que los átomos son los bloques constructores básicos de la materia. Este artículo de revisión muestra que, a escalas muy pequeñas, agrupaciones de decenas de átomos metálicos pueden comportarse como “super‑átomos” y que estos superátomos pueden unirse para formar “moléculas superatómicas”. Al comprender y diseñar estos inusuales bloques, los científicos esperan crear materiales con propiedades ópticas, electrónicas y catalíticas finamente sintonizadas que las moléculas ordinarias no pueden proporcionar.
Cúmulos que imitan átomos individuales
Los superátomos son cúmulos metálicos ultras pequeños, a menudo de oro, plata o cobre, cuyos electrones se organizan en patrones ordenados en capas, al igual que las capas que aparecen en los diagramas de un átomo en los libros de texto. Cuando esas capas están completamente llenas, en ciertos “números mágicos” de electrones, el cúmulo se vuelve especialmente estable. Los químicos pueden estabilizarlos aún más envolviéndolos con moléculas orgánicas llamadas ligandos, convirtiéndolos en nano‑objetos precisos con tamaños y formas bien definidos. Muchos de estos superátomos son casi esféricos, y su estabilidad puede explicarse mediante un modelo simple en el que los electrones libres del metal giran en el interior como si hubiera una gota positiva y cargada de forma uniforme.
Cuando los superátomos se enlazan como las moléculas ordinarias
Algunos cúmulos metálicos no son esféricos en absoluto. En cambio, parecen dos o más superátomos fusionados, formando lo que el autor denomina moléculas superatómicas. Para explicar estas estructuras, los investigadores desarrollaron la teoría de “superenlace de valencia”, que trata a cada superátomo como un átomo gigante con sus propios orbitales y describe cómo estos orbitales se mezclan para crear orbitales moleculares superatómicos compartidos. En muchos casos estas combinaciones se comportan como enlaces químicos familiares. Por ejemplo, pares de superátomos de oro pueden formar versiones superatómicas del enlace en la molécula de flúor, mientras que fusiones más complejas dan análogos de moléculas de oxígeno con órdenes de enlace más altos o incluso enlaces de tres centros que recuerdan al ozono. Estas disposiciones generan patrones ricos de enlace—simples, múltiples y multicírculares—que evocan las reglas de enlace de la química ordinaria, pero ahora a la escala de cúmulos que contienen decenas de átomos. 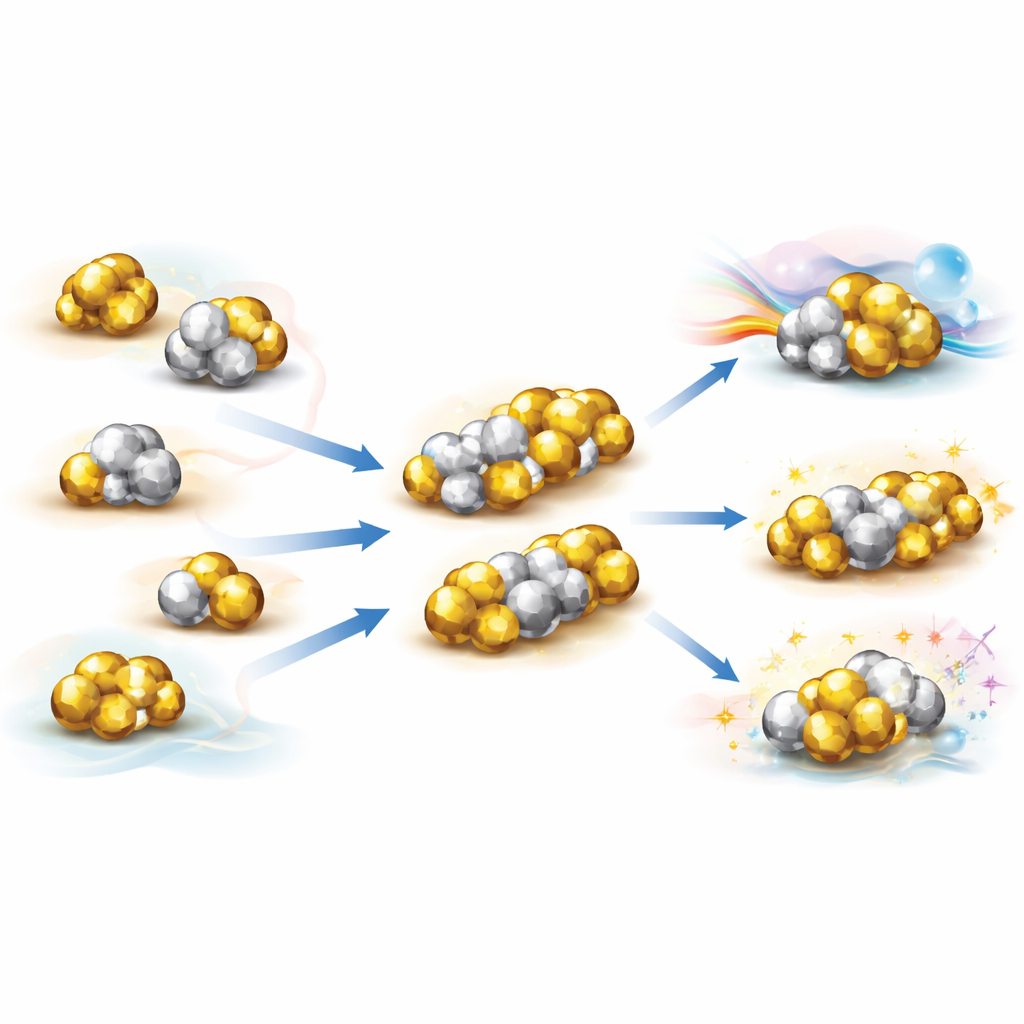
Enlaces extraños con unidades tipo gases nobles
Las moléculas superatómicas no se limitan a análogos ordenados de enlaces cotidianos. La revisión destaca motivos de enlace “no naturales” en los que superátomos con capas electrónicas cerradas—similares en espíritu a gases nobles como el helio o el neón—se combinan en estructuras mayores aun cuando, según las reglas convencionales de contabilización electrónica, no debería existir enlace alguno. En estos sistemas, los superátomos pueden compartir un único átomo metálico, apoyarse borde con borde o enlazarse en ensamblajes cíclicos y en forma de varilla. Formalmente, su orden de enlace es cero, sin embargo las interacciones entre sus nubes electrónicas y los ligandos circundantes estabilizan la estructura global. De forma notable, estos ensamblajes muestran nuevas bandas de absorción y otras características electrónicas ausentes en los superátomos aislados, lo que revela que interacciones orbitales sutiles pueden producir respuestas ópticas totalmente nuevas.
De superanillos a supercadenas
El artículo también examina ejemplos más exóticos donde los superátomos forman anillos y cadenas con comportamiento colectivo. Un caso destacado es un cúmulo de oro construido a partir de cinco superátomos icosaédricos dispuestos en un anillo; estudios teóricos sugieren que, con el número adecuado de electrones, este “superanillo” puede volverse aromático, distribuyendo sus electrones alrededor del lazo de manera directamente análoga a moléculas aromáticas clásicas como el benceno o el ion ciclopentadienilo. Otra familia de estructuras enlaza diminutas unidades de oro de tres átomos en cadenas en forma de varilla. Aunque las conexiones entre unidades vecinas son débiles y parcialmente antibonding, el patrón repetido de orbitales interactuantes actúa como un “polímero superatómico”, dando lugar a una fuerte absorción en la región del infrarrojo cercano y apuntando a aplicaciones en dispositivos fototérmicos y optoelectrónicos. 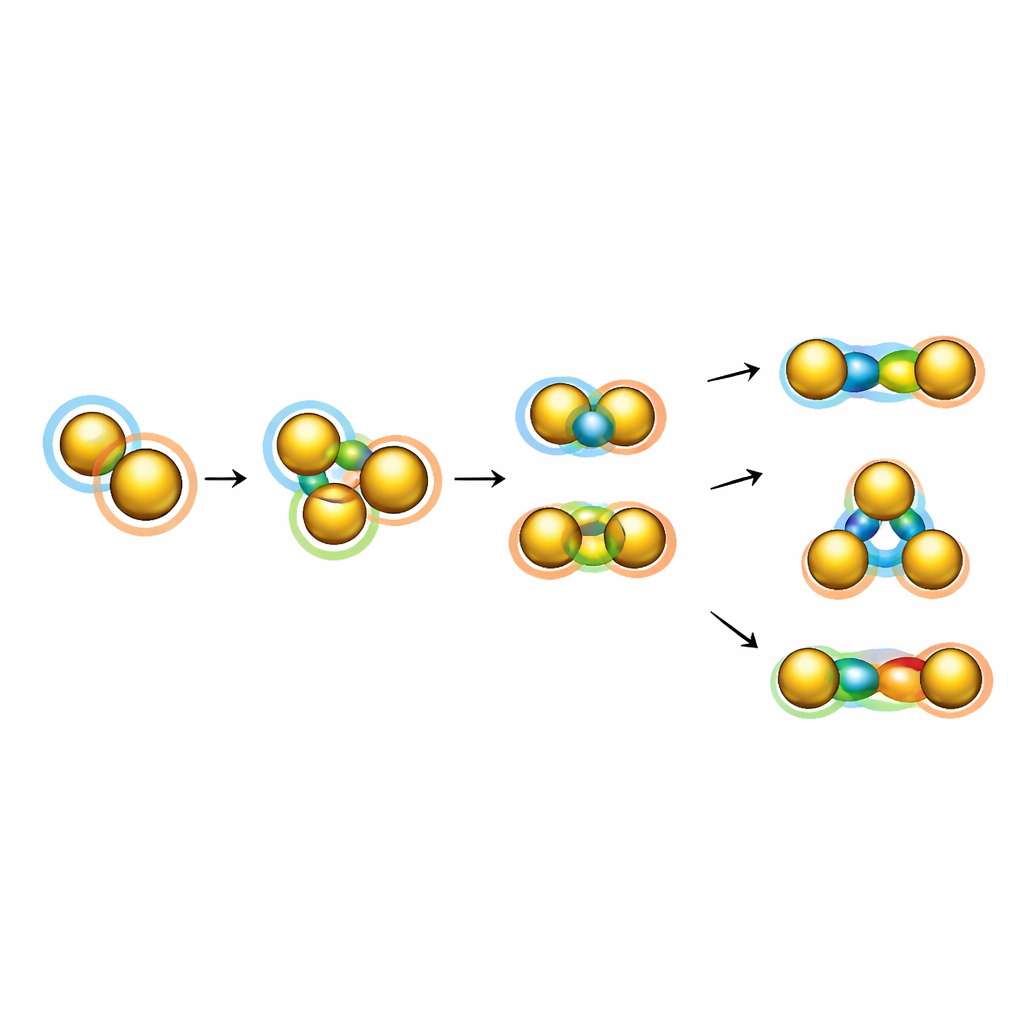
Por qué importan estas super‑moléculas diminutas
En conjunto, la revisión argumenta que tratar a los cúmulos metálicos como unidades con comportamiento atómico que pueden enlazarse en moléculas superatómicas ofrece un lenguaje de diseño potente para nuevos materiales. Al elegir cuántos electrones porta cada superátomo, cómo se enlazan y qué ligandos los rodean, los científicos pueden diseñar no solo la estabilidad sino también la absorción de luz, el transporte de carga, el magnetismo y la actividad catalítica. El enlace de estilo natural aporta reglas de diseño familiares, mientras que los ensamblajes no naturales y débilmente enlazados desbloquean comportamientos sin análogo directo en la química ordinaria. A medida que este entendimiento madura, las moléculas superatómicas podrían convertirse en una caja de herramientas para fabricar catalizadores de próxima generación, sistemas de captura de luz y componentes electrónicos construidos a partir de cúmulos de átomos dispuestos con precisión.
Cita: Isozaki, K. Superatomic molecules: natural and non-natural atom-like bonding between superatoms. NPG Asia Mater 18, 9 (2026). https://doi.org/10.1038/s41427-026-00636-9
Palabras clave: superátomos, nanocúmulos metálicos, moléculas superatómicas, nanomateriales, propiedades optoelectrónicas