Clear Sky Science · es
El virus oncolítico M1 reaviva la inmunidad de células T CD8+ contra el glioblastoma mediante la presentación cruzada de antígeno dependiente de células B en el bazo
Reactivar el sistema inmune
El glioblastoma es uno de los cánceres cerebrales más letales, en parte porque es extraordinariamente eficaz en apagar las defensas del organismo. Este estudio explora una nueva forma de volver a encender esas defensas mediante un virus diseñado específicamente, administrado por vía intravenosa, que a la vez ataca las células tumorales y moviliza a las células inmunitarias para combatir el cáncer. El trabajo revela una protagonista inesperada en esta respuesta: células inmunitarias del bazo que ayudan a despertar a las células T que matan tumores.
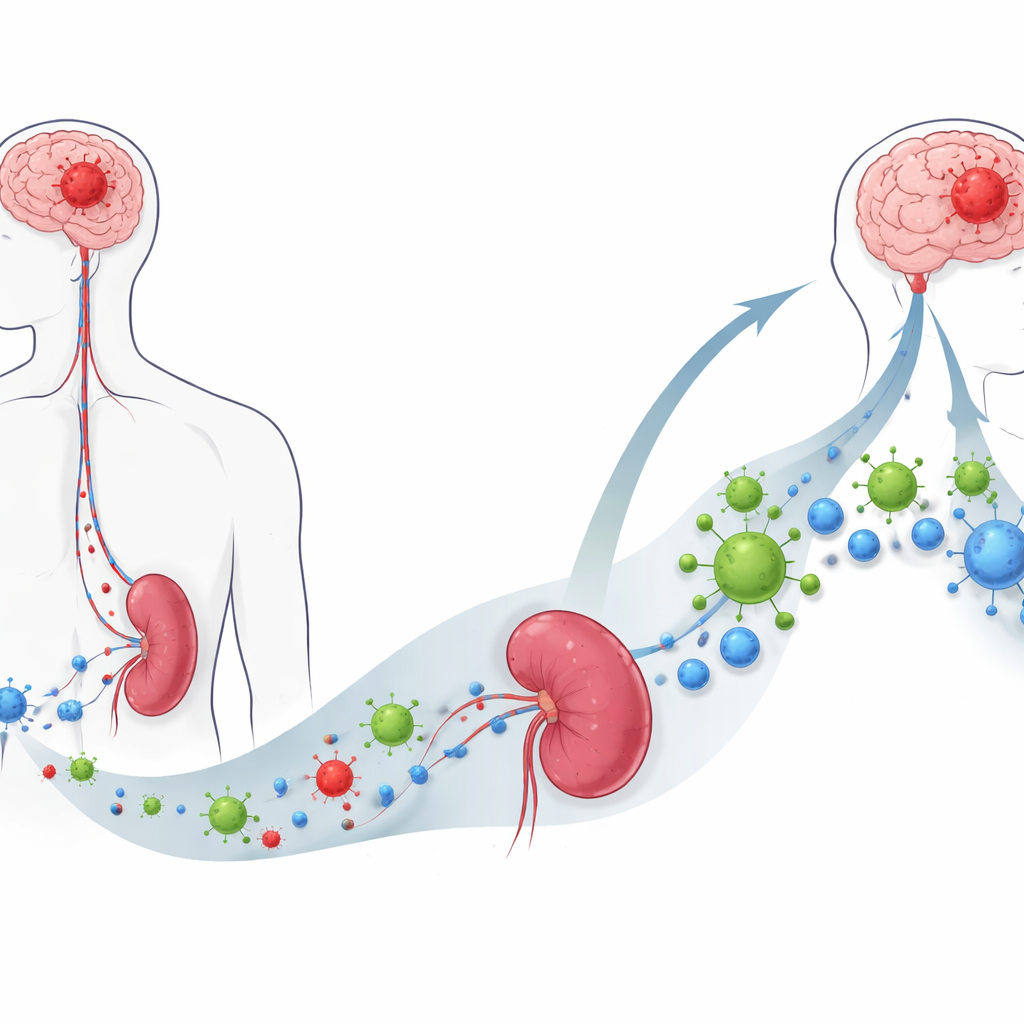
Un virus que prefiere las células cancerosas
Los investigadores estudiaron una terapia experimental llamada virus oncolítico M1, u OVM, un alfavirus modificado que prefiere infectar y matar células cancerosas mientras respeta el tejido sano. En placas de cultivo, OVM invadió con eficacia una variedad de líneas celulares de glioblastoma de ratón y humano y las indujo a una forma de muerte celular que deja señales moleculares de “peligro”. Al probarse en fragmentos tumorales humanos recién extraídos, OVM se replicó con fuerza en tejido de glioblastoma pero no en muestras cerebrales no cancerosas adyacentes, lo que sugiere que puede distinguir células malignas de sanas mejor que la quimioterapia estándar, que dañó a ambas.
Revirtiendo la supresión inmune sistémica
Más allá del cerebro, el glioblastoma provoca un colapso inmune generalizado: pacientes y modelos murinos muestran bazo reducido y una marcada pérdida de células T circulantes. Tras el tratamiento intravenoso con OVM en ratones con tumor, este panorama cambió drásticamente. Los bazos recuperaron su tamaño, los niveles en sangre de células T CD4 y CD8 se recuperaron, y moléculas inmunosupresoras como IL-10 y TGF-beta disminuyeron. En el sitio tumoral, más células T—especialmente las CD8 “asesinas” que reconocen un antígeno tumoral modelo—se desplazaron al cerebro, convirtiendo un entorno tumoral previamente “frío” en uno lleno de combatientes inmunitarios.
Por qué el bazo importa
De forma sorprendente, el bazo resultó ser esencial para el éxito de OVM. Cuando se extirpó quirúrgicamente el bazo, el virus dejó de ralentizar el crecimiento tumoral y de prolongar la supervivencia, y el aumento de células T en sangre y cerebro desapareció en gran parte. El secuenciamiento de ARN unicelular de las células inmunitarias esplénicas mostró que tras el tratamiento con OVM, las células B en el bazo establecieron redes de comunicación especialmente fuertes con las células T. En cultivos, las células B de ratones tratados con OVM hicieron proliferar y activar a las células T CD8 mucho más eficazmente que las células B de animales no tratados, mientras que las células dendríticas no mostraron ese aumento, lo que señala a las células B como intermediarias clave.
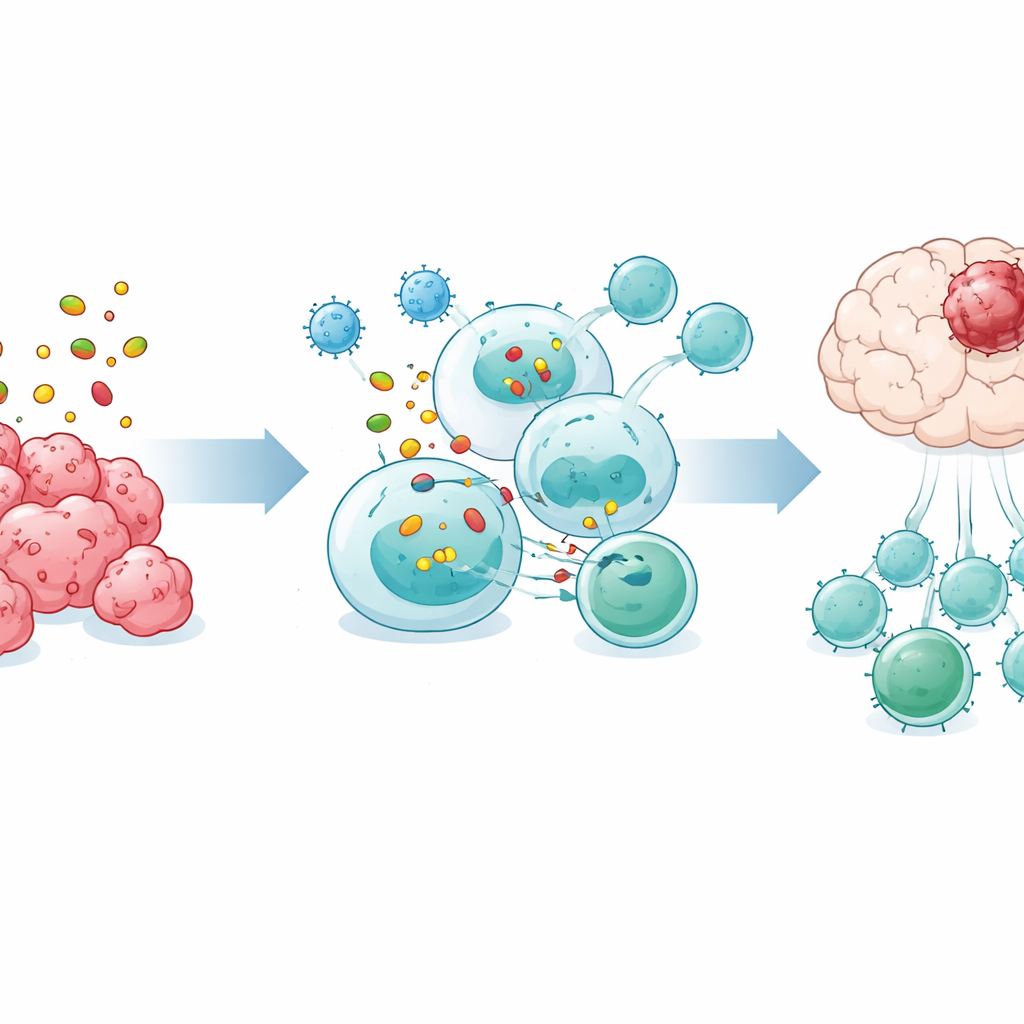
Células B especiales que activan a los asesinos tumorales
Profundizando más, el equipo descubrió un subgrupo distintivo de células B marcado por una molécula de superficie llamada Bst2 que se expandió en el bazo tras el tratamiento con OVM. Estas células B Bst2-positivas presentaban mayor expresión de genes implicados en la captura de material tumoral, su procesamiento intracelular y la presentación de fragmentos en la superficie de modo que las células T CD8 puedan “verlos”. Los experimentos mostraron que estas células captaban antígenos tumorales con más eficiencia, formaban zonas de contacto estrecho con las células T CD8 y requerían contacto celular directo y una vía específica de procesamiento de proteínas para activar a las T. Cuando se transfirieron células B purificadas Bst2-positivas a ratones carentes de células B con tumores cerebrales, prolongaron significativamente la supervivencia, mientras que otros tipos de células B no lo hicieron.
Potenciando la terapia con inhibidores de punto de control
Las inmunoterapias líderes en la actualidad—inhibidores de punto de control que bloquean PD-1 o PD-L1—han dado resultados decepcionantes en glioblastoma. En los modelos murinos utilizados aquí, los anticuerpos contra PD-1 o PD-L1 por sí solos hicieron poco. Sin embargo, la combinación de OVM con un anticuerpo bloqueador de PD-1 aumentó sustancialmente el número de células T CD8 en los tumores cerebrales, desplazó a las células T circulantes de un estado naïve a uno activado, restauró el tamaño del bazo y prolongó la supervivencia. El tratamiento con OVM también elevó los niveles de PD-1 en las células T CD8 infiltrantes del tumor, haciéndolas más susceptibles a ser rescatadas por el bloqueo de PD-1.
Qué podría significar esto para los pacientes
En conjunto, este trabajo sugiere que un virus oncolítico administrado por vía intravenosa puede hacer más que simplemente infectar y lisar células de glioblastoma. Al reclutar a un grupo especializado de células B en el bazo para procesar material tumoral y mostrárselo a las células T CD8, OVM reconstruye la inmunidad sistémica y conduce a las células T asesinas de vuelta al cerebro para atacar el tumor. En modelos preclínicos, esta estrategia no solo suprime el crecimiento tumoral por sí sola, sino que también hace que tumores cerebrales resistentes respondan a la terapia con inhibidores de PD-1. Si estos hallazgos se trasladan a humanos, OVM y las células B Bst2-positivas podrían formar la columna vertebral de nuevas terapias combinadas—e incluso vacunas personalizadas—que por fin den al sistema inmune una oportunidad de combatir el glioblastoma.
Cita: Han, Y., Guo, C., Chen, C. et al. Oncolytic virus M1 reinvigorates CD8+ T-cell immunity against glioblastoma through B-cell-dependent antigen cross-presentation in the spleen. Cell Mol Immunol 23, 349–366 (2026). https://doi.org/10.1038/s41423-026-01396-w
Palabras clave: glioblastoma, virus oncolítico, inmunología tumoral, células B, terapia con inhibidores de punto de control inmunitario