Clear Sky Science · es
Afrontando la cuproptosis: del reprogramado metabólico a la explotación terapéutica en el cáncer
Cuando un metal útil se vuelve contra el cáncer
El cobre es más conocido como componente de cables eléctricos y tuberías, pero también circula silenciosamente por nuestras células, ayudando a las enzimas a generar energía y a protegernos del daño. Este artículo de revisión explora un giro sorprendente: en las condiciones adecuadas, el exceso de cobre puede empujar a las células cancerosas hacia una forma particular de muerte. Comprender este proceso—denominado “cuproptosis”—podría abrir nuevas vías para tratar tumores que han eludido las terapias estándar.
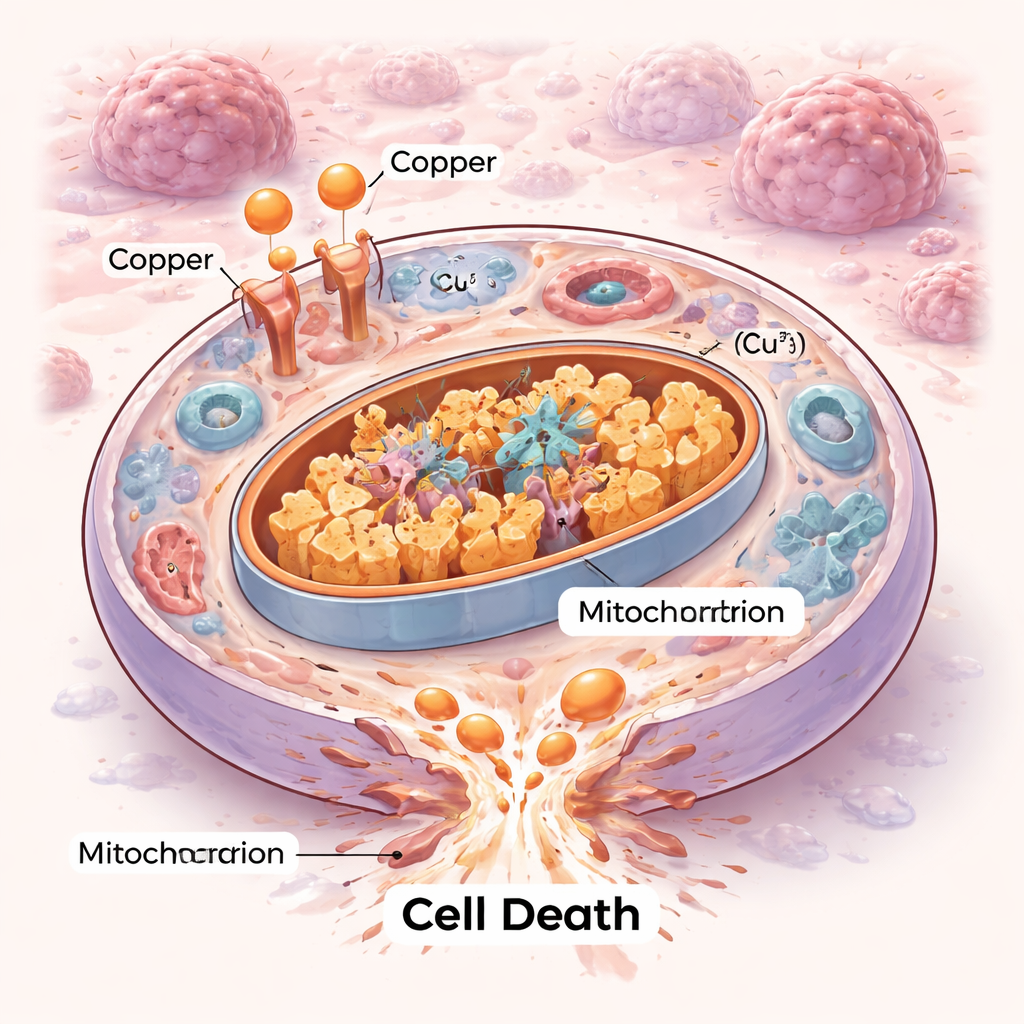
Una nueva forma en que las células pueden morir
Las células no mueren todas de la misma manera. Durante décadas, los científicos han cartografiado programas ordenados de autodestrucción como la apoptosis y formas más recientes como la ferroptosis. La cuproptosis añade un capítulo nuevo. Aquí, el exceso de cobre inunda las centrales energéticas de la célula—las mitocondrias—y se une a enzimas metabólicas específicas que normalmente ayudan a quemar combustible. Esta unión provoca que esas enzimas se agreguen y desestabiliza pequeños componentes de hierro‑azufre que las mitocondrias necesitan para funcionar. El resultado es una especie de atasco interno y una avería mecánica que la célula no puede reparar, terminando en muerte por estrés proteotóxico en lugar de por las rutas clásicas de suicidio celular.
Cómo las células cancerosas controlan el cobre y la energía
Puesto que el cobre es a la vez esencial y peligroso, las células mantienen una red logística elaborada para moverlo con seguridad. Transportadores dedicados introducen cobre en la célula, proteínas chaperonas lo escortan hacia las mitocondrias y otros destinos, y moléculas de almacenamiento como las metalotioneínas y el glutatión absorben el exceso. Los tumores suelen reprogramar este sistema. Algunos aumentan los importadores o las chaperonas para alimentar sus altas demandas energéticas; otros incrementan exportadores o proteínas de almacenamiento para evitar la sobrecarga de cobre. Al mismo tiempo, muchos cánceres desplazan su metabolismo—conmutando entre la quema de azúcares en la superficie celular y una respiración mitocondrial más profunda. La revisión explica que la cuproptosis afecta con mayor fuerza a las células que aún dependen en gran medida de las mitocondrias, lo que hace que los tumores con este perfil metabólico sean especialmente vulnerables.
Interruptores maestros que modulan la sensibilidad al cobre
Grandes “decisores” celulares influyen en si la cuproptosis puede ocurrir. El supresor tumoral p53, por ejemplo, tiende a alejar a las células de la fermentación rápida de azúcares hacia un uso mitocondrial del combustible más ordenado. Al hacerlo, y al alterar el manejo de enzimas que se unen al cobre, p53 puede hacer que los cánceres sean más susceptibles a la muerte inducida por cobre—mientras que formas mutantes de p53 suelen provocar el efecto contrario. En contraste, el factor de hipoxia HIF‑1α, activado en los núcleos tumorales pobremente oxigenados, ayuda a las células a escapar de la cuproptosis al reducir enzimas mitocondriales clave y aumentar escudos que se unen al cobre. Otras vías, como Wnt/β‑catenina y AKT, promueven la resistencia al impulsar la exportación de cobre o modificar químicamente proteínas cruciales para que ya no respondan a la sobrecarga de cobre. En conjunto, estas redes actúan como termostatos, elevando o reduciendo la sensibilidad de un tumor a los tratamientos basados en cobre.
El cobre, el sistema inmune y una administración de fármacos más inteligente
El papel del cobre no se limita a matar directamente a las células cancerosas; también moldea el paisaje inmunitario alrededor de los tumores. Un estrés controlado por cobre puede hacer que las células cancerosas en proceso de muerte sean más “visibles”, liberando señales de peligro que reclutan y activan linfocitos T, células dendríticas y macrófagos. El cobre también puede influir en los niveles de puntos de control inmunitario como PD‑L1, que los tumores usan para desactivar a los linfocitos T anticancerígenos, lo que sugiere oportunidades para combinar fármacos dirigidos al cobre con inmunoterapias modernas. Dado que el cobre libre puede dañar tejidos sanos, los investigadores están desarrollando herramientas de precisión—ionóforos de pequeña molécula que transportan cobre selectivamente a las células cancerosas, y plataformas de nanomedicina que empaquetan cobre o fármacos activados por cobre dentro de partículas dirigidas o hidrogeles. Estas tecnologías buscan elevar el cobre a niveles letales dentro de los tumores manteniendo el resto del organismo dentro de un rango seguro.
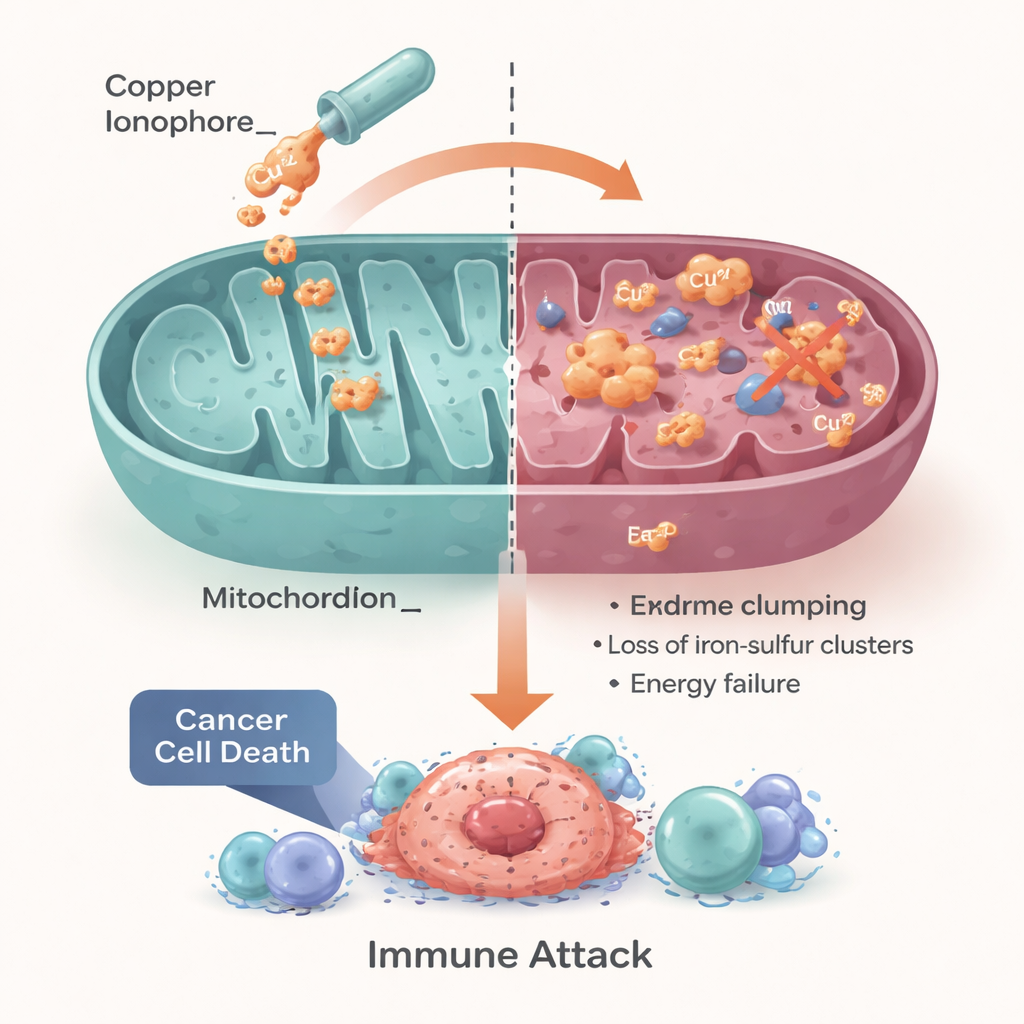
Convertir una debilidad celular en un tratamiento
Los autores concluyen que la cuproptosis convierte una necesidad celular básica—la gestión cuidadosa del cobre y la energía—en un posible talón de Aquiles para el cáncer. Los tumores con manejo perturbado del cobre o una dependencia excesiva de la respiración mitocondrial pueden ser especialmente sensibles a estrategias basadas en cobre, incluyendo fármacos reposicionados como disulfiram y elesclomol, así como nanopartículas de próxima generación. Sin embargo, subrayan que el éxito dependerá de emparejar a los pacientes adecuados con el enfoque correcto, usando biomarcadores que informen sobre los transportadores de cobre, la actividad mitocondrial y el estado inmunitario y de oxigenación del tumor. Si se superan estos obstáculos, aprovechar la cuproptosis podría proporcionar a los oncólogos una nueva palanca impulsada por metales para tratar tumores que actualmente tienen pocas opciones eficaces.
Cita: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Palabras clave: cuproptosis, metabolismo del cobre, terapia contra el cáncer, metabolismo tumoral, inmunoterapia contra el cáncer