Clear Sky Science · es
La fuerza magneto‑mecánica dinámica en lisosomas induce una repolarización duradera de macrófagos para la inmunidad antitumoral
Usar fuerzas suaves para despertar al sistema inmunitario
El cáncer a menudo sobrevive haciendo que las defensas del cuerpo se adormezcan. Este estudio explora una forma inesperada de despertarlas: tirando físicamente de pequeños compartimentos dentro de las células inmunitarias con nanopartículas accionadas por campos magnéticos. En lugar de confiar únicamente en fármacos, los investigadores emplean fuerzas mecánicas cuidadosamente calibradas dentro de las células para reprogramar macrófagos en combatientes tumorales duraderos.
Por qué los tumores sólidos son difíciles de tratar
Las inmunoterapias contra el cáncer modernas, como los anticuerpos que bloquean puntos de control y las células inmunitarias modificadas, han transformado el tratamiento de algunos cánceres hematológicos. Sin embargo, para muchas personas con tumores sólidos, como el cáncer de pulmón, estos enfoques solo benefician a una minoría. Una razón importante es el microambiente tumoral. Los tumores están rodeados por un nicho protector lleno de células y señales que suprimen la inmunidad. Los macrófagos, que pueden atacar tumores (un estado similar a M1) o apoyarlos (un estado similar a M2), a menudo se ven empujados hacia el modo M2 que favorece al tumor. Revertir esta programación “mala” de forma duradera ha sido difícil usando solo fármacos bioquímicos convencionales.
Convertir nanopartículas en pequeños motores mecánicos
El equipo diseñó nanomotores magnéticos: partículas a escala nanométrica de óxido de hierro dopado con zinc recubiertas con un polímero cargado positivamente, que son fácilmente fagocitadas por macrófagos y terminan concentradas en los lisosomas, los centros de reciclaje y señalización de la célula. Una vez dentro, un campo magnético rotatorio externo hace que estas partículas se alineen en cadenas con forma de varilla y giren, agitando el fluido viscoso dentro de los lisosomas y creando pequeños vórtices. Simulaciones por ordenador y experimentos con membranas modelo mostraron que, al ajustar cuidadosamente la frecuencia de rotación, el esfuerzo cortante sobre la membrana lisosomal puede situarse en un punto óptimo: lo bastante fuerte como para hacer que la membrana quede brevemente permeable, pero no tan intenso como para destruirla de forma permanente.
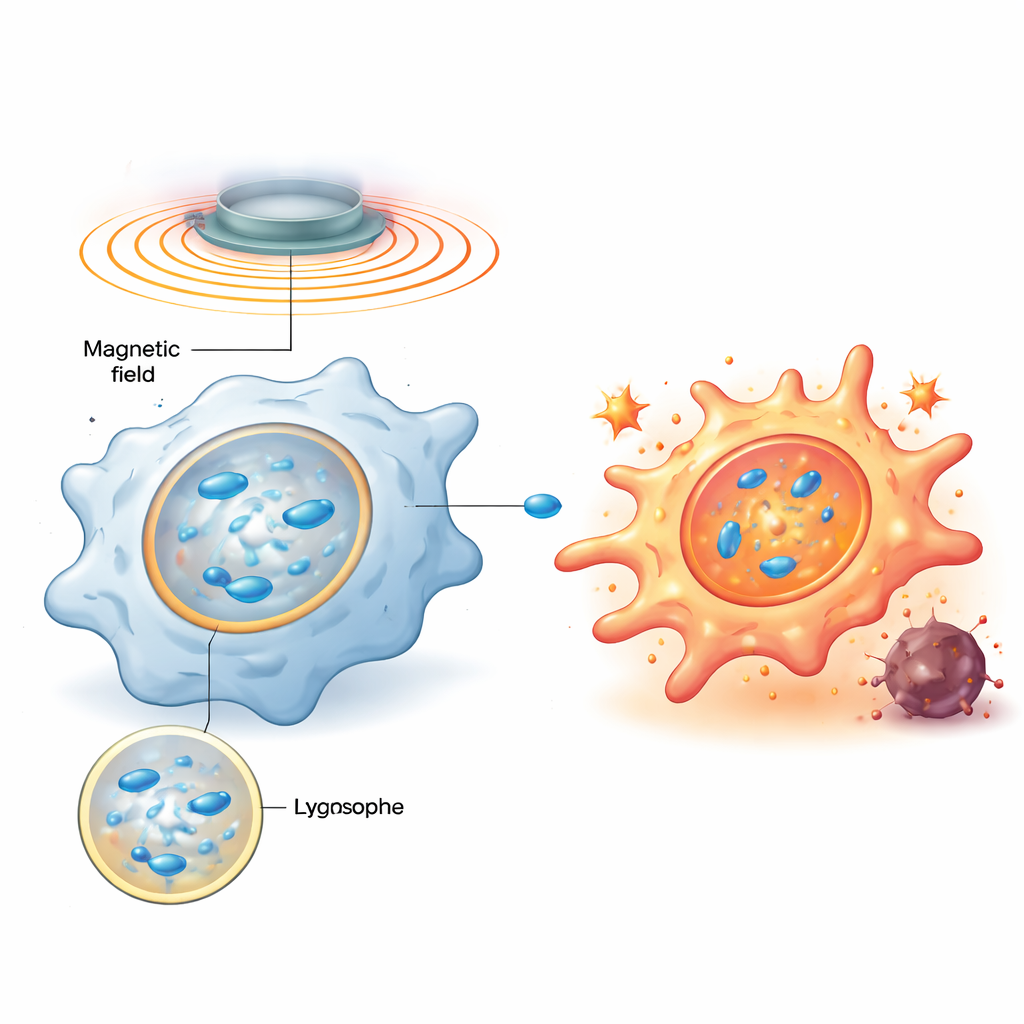
Un empujón mecánico desencadena una alarma bioquímica
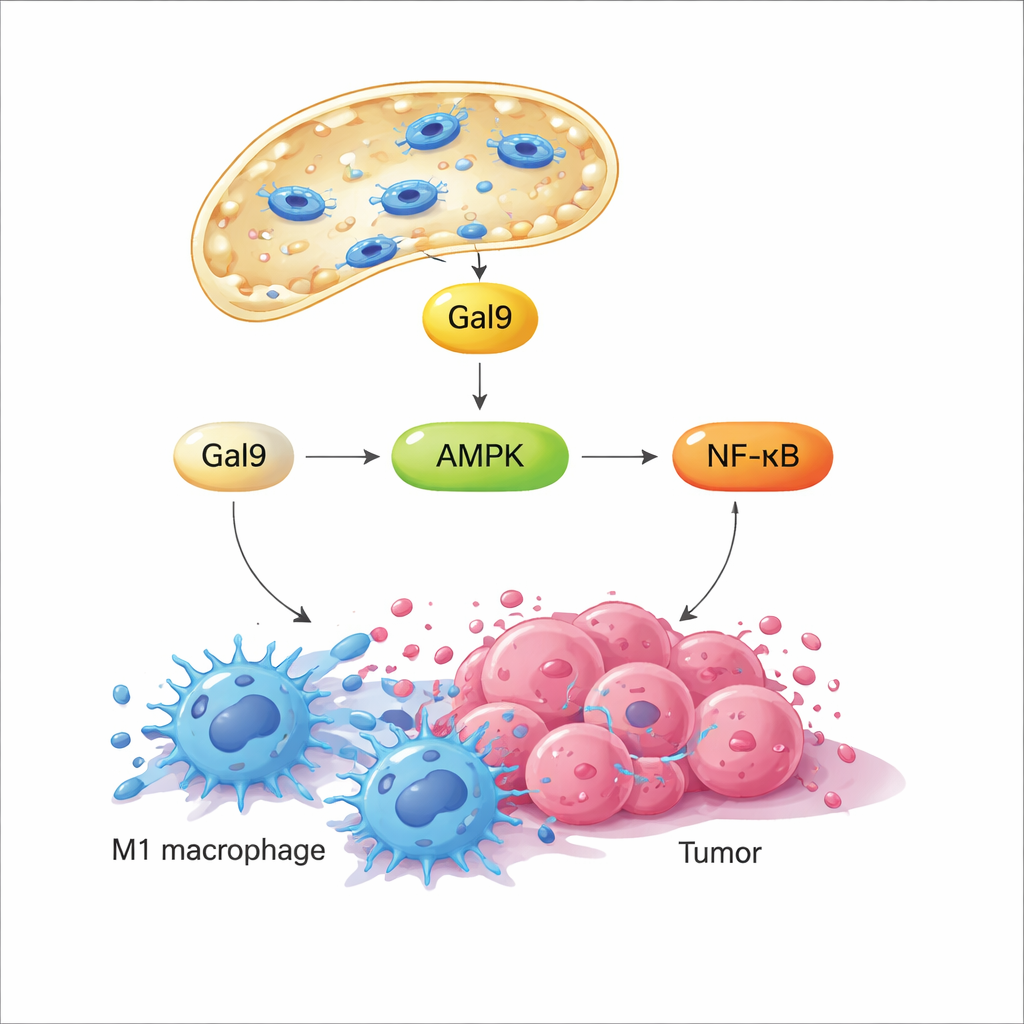
Cuando la membrana lisosomal se ve perturbada brevemente, una proteína que se une a azúcares llamada galectina‑9 acude a las zonas dañadas, actuando como sensor de este estrés mecánico. El estudio muestra que esto, a su vez, activa una enzima clave que detecta la energía, AMPK, la cual potencia la vía de señalización NF‑κB —bien conocida por impulsar respuestas inflamatorias y antimicrobianas. Juntas, estas señales reconducen el metabolismo del macrófago alejándolo de un estado silencioso y eficiente en combustible hacia una glucólisis rápida, un patrón asociado con un comportamiento hostil similar a M1. Es importante destacar que, cuando se apaga el campo magnético, el lisosoma se repara y la señalización disminuye; cuando el campo se reactiva más tarde, la misma vía vuelve a activarse. Este ciclo programable de encendido‑apagado permite a los investigadores “tocar” repetidamente el mismo interruptor mecánico sin matar a las células.
Reeducar macrófagos para combatir tumores
En cultivos celulares, esta permeabilización lisosomal inducida magnéticamente —denominada MagLMP— reconvirtió macrófagos empujados hacia un estado similar a M2 que favorece al tumor de vuelta a un estado proinflamatorio similar a M1. Estas células reprogramadas produjeron más citocinas inflamatorias y mantuvieron su perfil M1 durante días, incluso en medios de cultivo derivados de tumores que normalmente los inducen hacia M2. En modelos murinos de tumor, la implantación de nanomotores magnéticos en los tumores y la aplicación de ciclos diarios del campo rotatorio ralentizaron el crecimiento de varios tipos de cáncer. Cuando los macrófagos fueron experimentalmente agotados, el beneficio desapareció en gran medida, mostrando que estas células son centrales para el efecto del tratamiento. El secuenciamiento de ARN de célula única del tejido tumoral reveló además que MagLMP aumentó la proporción de macrófagos de tipo M1, potenció neutrófilos antitumorales y células T CD8 efectoras, y reguló al alza genes relacionados con NF‑κB y la glucólisis dentro de los macrófagos.
Del control local a la terapia sistémica
Los investigadores se preguntaron entonces si este enfoque podría funcionar más como un tratamiento del mundo real, administrado por vía sanguínea. Inyectaron los nanomotores por vía intravenosa y usaron un imán externo simple para concentrarlos en los tumores, demostrando una captación eficiente por parte de los macrófagos en la cama tumoral. El tratamiento MagLMP posterior volvió a desplazar a los macrófagos hacia el estado similar a M1 y limitó el crecimiento tumoral. En un modelo murino de cáncer de pulmón en estadio temprano que crece dentro del propio pulmón, la combinación de guiado magnético con ciclos de MagLMP condujo a una supervivencia notablemente prolongada: aproximadamente un tercio de los ratones tratados vivieron más de 300 días, en comparación con solo semanas en los animales control. Combinar MagLMP con un inhibidor del punto de control PD‑1 mejoró aún más el control tumoral en modelos de difícil tratamiento.
Una nueva forma de controlar la inmunidad desde dentro hacia fuera
Este trabajo demuestra que pequeñas fuerzas mecánicas bien controladas dentro de un orgánulo específico pueden aprovecharse para dirigir el comportamiento inmunitario en animales vivos. Al “pinchar” repetida y reversiblemente los lisosomas, MagLMP activa un eje galectina‑9–AMPK–NF‑κB que reprograma los macrófagos en combatientes tumorales duraderos sin dañar ampliamente las células. Para los no especialistas, la idea clave es que las señales físicas —entregadas por nanomotores impulsados magnéticamente— pueden actuar como una perilla en el sistema inmunitario, ofreciendo una nueva clase de herramientas para complementar a los fármacos en futuras inmunoterapias contra el cáncer.
Cita: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Palabras clave: inmunoterapia contra el cáncer, reprogramación de macrófagos, nanopartículas magnéticas, mecanotransducción, señalización lisosomal