Clear Sky Science · es
Activación mecánica transitoria del canal Piezo1 facilita la expansión ex vivo de células madre hematopoyéticas
Producir más células madre sanguíneas que salvan vidas
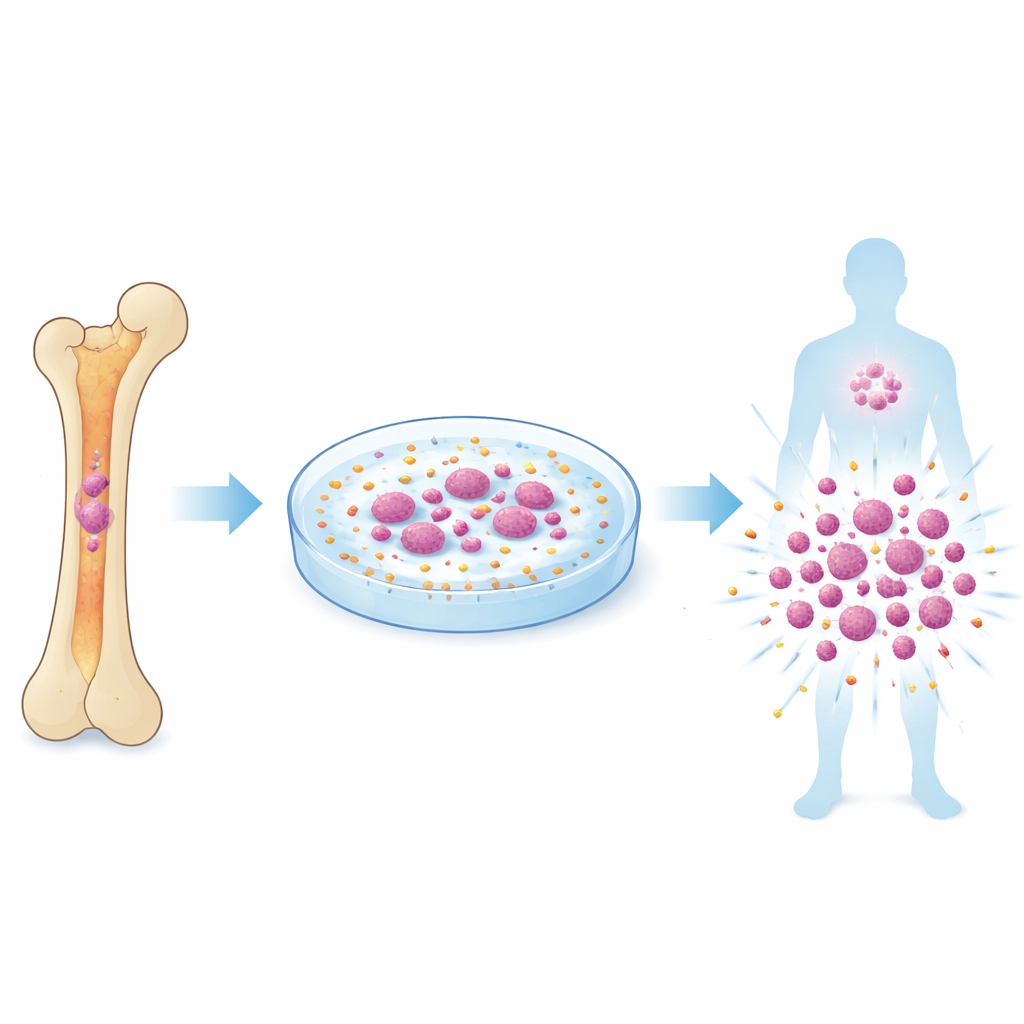
Los trasplantes de médula ósea pueden curar ciertos cánceres de la sangre y trastornos hereditarios, pero los médicos a menudo están limitados por la escasez de verdaderas células formadoras de sangre que pueden obtener de un donante. Este estudio revela una forma sorprendente de cultivar estas células raras fuera del cuerpo al «tocar» suavemente ellas con pequeñas bolitas de plástico que activan un sensor mecánico en su superficie. El trabajo sugiere una nueva vía, potencialmente más segura, para generar suficientes células madre y que más pacientes puedan beneficiarse del trasplante.
Por qué es tan difícil hacer crecer células madre sanguíneas
Las células madre sanguíneas se encuentran en lo profundo de nuestros huesos y suministran silenciosamente todas nuestras células rojas, células blancas y plaquetas durante toda la vida. Trasplantar estas células puede restablecer un sistema sanguíneo dañado, como en el tratamiento de la leucemia, pero solo si hay suficientes células madre sanas disponibles y mantienen su funcionalidad plena. Los esfuerzos por expandirlas en platos de laboratorio a menudo han fracasado: las células tienden a dejar de renovarse o pierden su capacidad a largo plazo para reconstruir el sistema sanguíneo. La mayoría de los métodos actuales dependen de cócteles de factores de crecimiento y modificaciones genéticas, pero no recrean por completo el complejo entorno físico de la médula ósea, donde las células madre sienten constantemente empujes, tirones y presiones.
Un interruptor mecánico oculto en las células madre
Los investigadores se centraron en una proteína llamada Piezo1, un pequeño canal en forma de válvula en la membrana celular que se abre cuando la membrana se dobla o estira, permitiendo que los iones de calcio entren y desencadenen señales internas. Al examinar muchos tipos de células sanguíneas, encontraron que Piezo1 es especialmente abundante en las verdaderas células madre hematopoyéticas. Cuando eliminaron Piezo1 genéticamente, o lo bloquearon con un fármaco, las células madre cultivadas en platos ya no pudieron expandirse bien ni repoblar la sangre de ratones tras el trasplante. Curiosamente, estimular Piezo1 de forma continua con activadores químicos también resultó perjudicial: las células acumulaban calcio en exceso, producían especies reactivas dañinas y tenían menos capacidad de injerto. Estos resultados sugieren que las células madre necesitan una activación mecánica breve y bien sincronizada de Piezo1, no un estímulo químico constante.
Aprovechar pequeñas bolitas para tocar el sensor
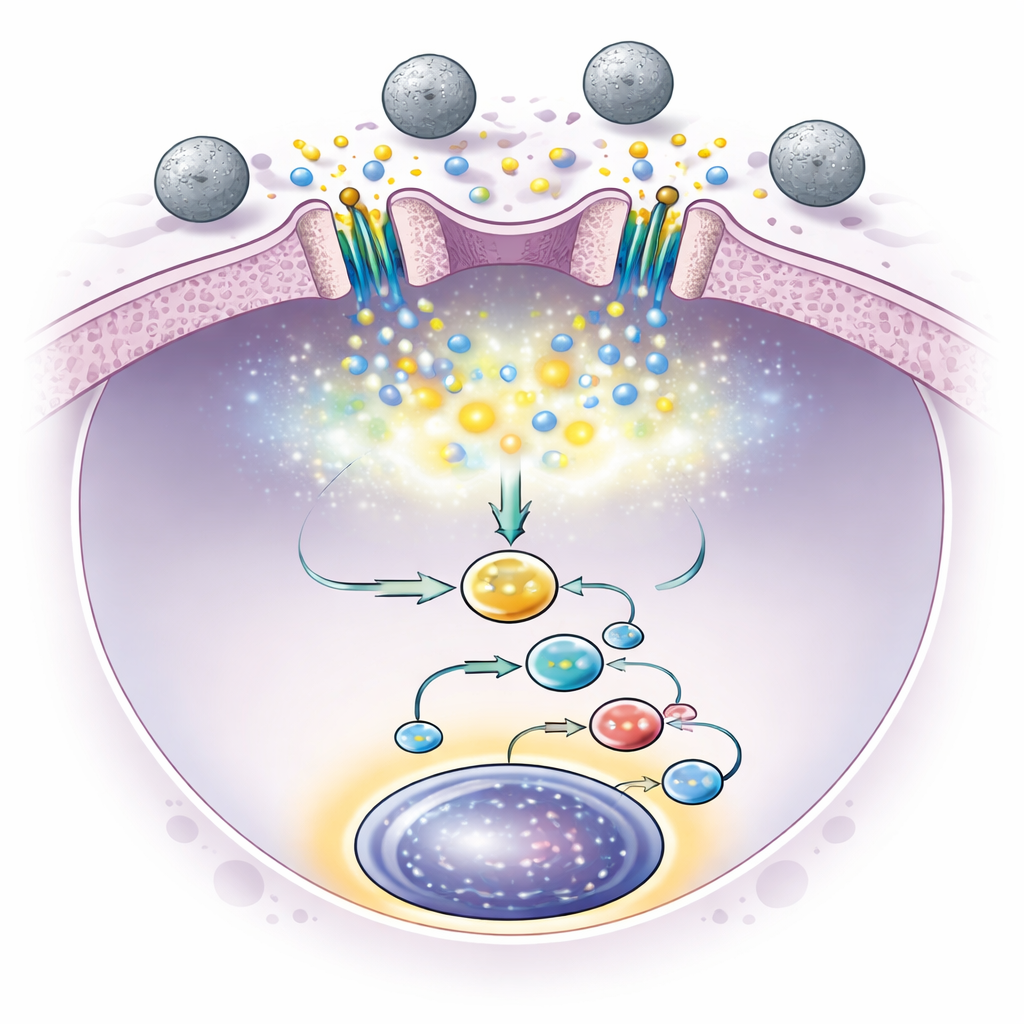
Para proporcionar el empujón mecánico adecuado, el equipo recurrió a esferas poliméricas microscópicas, esencialmente pequeñas perlas de plástico lisas, que podían rozar las células madre en cultivo. Probaron esferas de distintos tamaños y rigideces y descubrieron que las esferas de poliestireno de 500 nanómetros —denominadas PS500— eran notablemente efectivas. Cuando células de médula ósea de ratón se cultivaron junto con estas bolitas, el número de células madre aumentó drásticamente, y estas células mantuvieron una fuerte capacidad de repoblación a largo plazo en trasplantes seriales a través de múltiples generaciones de ratones. Imágenes cuidadosas y medidas mecánicas mostraron que las bolitas indentaban repetidamente la membrana de la célula madre con fuerzas minúsculas, lo bastante para abrir los canales Piezo1 en breves pulsos sin abrumar a las células.
Del toque mecánico a las señales de crecimiento
La breve apertura de los canales Piezo1 provocó pequeños pulsos de entrada de calcio en las células madre. Esto, a su vez, activó vías internas que llevaron a las células a producir ciertas proteínas señalizadoras, en particular el factor de crecimiento interleucina-6. La interleucina-6 luego retroalimentó a las células madre y activó una proteína llamada Stat3 en sus núcleos, conocida por apoyar la supervivencia y la autorrenovación de las células madre. Cuando los investigadores bloquearon esta vía de Stat3, el efecto beneficioso de las bolitas desapareció, confirmando que esta cadena de eventos—toque mecánico, pulso de calcio, liberación de interleucina-6 y activación de Stat3—era crucial para la expansión. Es importante destacar que, tras un breve periodo de exposición a las bolitas, la señalización permaneció activa y el número de células madre continuó aumentando, lo que subraya que la estimulación constante no era necesaria.
Promesa para los trasplantes humanos
El equipo aplicó a continuación el mismo enfoque a células madre sanguíneas humanas recolectadas de sangre de cordón umbilical, una fuente habitual pero a menudo limitada para el trasplante. Con las bolitas PS500, estas células humanas se expandieron varias veces más que con los métodos líderes basados solo en pequeñas moléculas, y aun así conservaron su capacidad de repoblar de forma permanente la sangre de ratones inmunodeficientes. Estudios de seguridad en ratones sugirieron que las bolitas no penetran en las células madre, pueden eliminarse eficientemente mediante centrifugación o filtración simples, y no causan daños orgánicos evidentes ni anomalías sanguíneas en las dosis probadas. Esto posiciona el sistema basado en bolitas como una tecnología práctica y potencialmente escalable para bancos de sangre y centros de trasplante.
Qué podría significar esto para los pacientes
En esencia, el estudio muestra que una señal mecánica suave—entregada por bolitas en deriva a escala nanométrica—puede inducir a las células madre sanguíneas a multiplicarse mientras conserva su potencia, al activar brevemente un sensor de presión incorporado en lugar de sobreestimularlo. Si se traduce a la clínica, este enfoque podría facilitar la generación de suficientes células madre de alta calidad a partir de una pequeña unidad de sangre de cordón o de un donante parcial, ampliando el acceso a trasplantes curativos para muchas más personas. También destaca cómo prestar atención no solo al «caldo» químico que rodea a las células, sino también a las sensaciones físicas que experimentan, puede desbloquear nuevas maneras de controlar el destino celular.
Cita: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Palabras clave: células madre hematopoyéticas, canales iónicos mecanosensibles, Piezo1, microesferas de poliestireno, trasplante de células madre