Clear Sky Science · es
La bilirrubina activa directamente RIPK3 para inducir necroptosis no clásica
Cuando una molécula útil se vuelve dañina
La bilirrubina es más conocida como el pigmento amarillo detrás de la ictericia neonatal y del color familiar de los moratones. A niveles bajos, en realidad ayuda a proteger nuestras células del daño. Pero cuando la bilirrubina se acumula en el organismo y se filtra al cerebro, puede causar lesiones duraderas, especialmente en recién nacidos y personas con enfermedad hepática grave. Este estudio descubre una forma sorprendente en que el exceso de bilirrubina puede activar directamente un “interruptor de muerte” molecular dentro de las células cerebrales, impulsando una forma destructiva de muerte celular y ofreciendo un nuevo objetivo para futuras terapias.
Del pigmento sanguíneo a la amenaza cerebral
La bilirrubina se produce cuando nuestro cuerpo recicla los glóbulos rojos. Normalmente, el hígado la modifica y elimina, manteniendo los niveles bajos y relativamente seguros. En ciertas condiciones —como la ictericia neonatal, infecciones graves o insuficiencia hepática— la bilirrubina no procesada puede acumularse. Debido a que se disuelve fácilmente en grasas, esta forma “libre” puede cruzar la barrera hematoencefálica, sobre todo cuando esa barrera está debilitada por la enfermedad o la inflamación. Una vez dentro del cerebro, se sabe que la bilirrubina es tóxica, pero los pasos exactos por los que daña las neuronas habían permanecido poco claros.
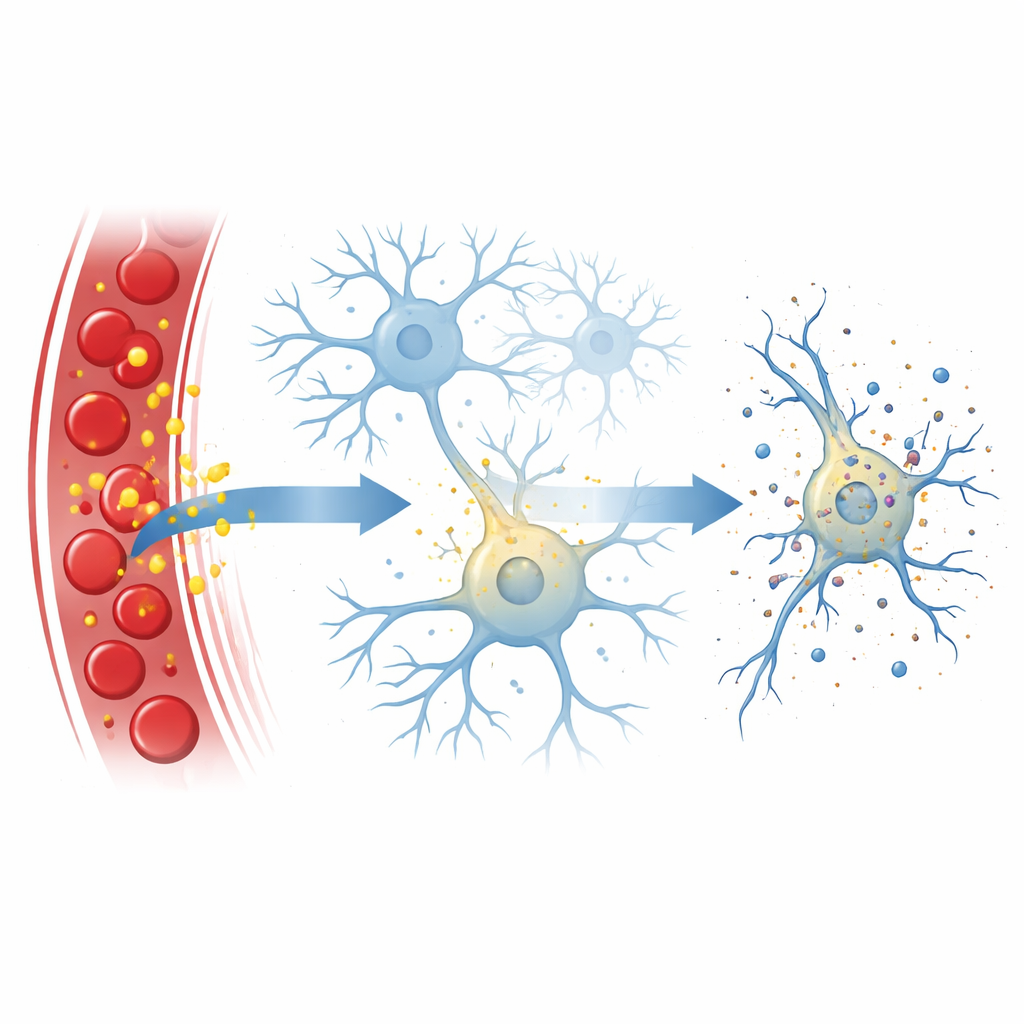
Una explosión celular controlada
Los investigadores se centraron en la necroptosis, una forma regulada de muerte celular que recuerda a una pequeña explosión: la célula se hincha, su membrana externa se rompe y su contenido se derrama, a menudo desencadenando inflamación. Este proceso normalmente lo impulsa una cadena de proteínas, con una llamada RIPK3 actuando como un centro neurálgico y otra, MLKL, perforando la membrana celular. En las vías clásicas de los manuales, RIPK3 se activa por proteínas socias que reconocen señales de peligro como moléculas inflamatorias o material genético viral. Aquí, el equipo encontró que la bilirrubina puede eludir a esos socios habituales y aun así provocar necroptosis en las neuronas.
La bilirrubina toma el interruptor de muerte de la célula
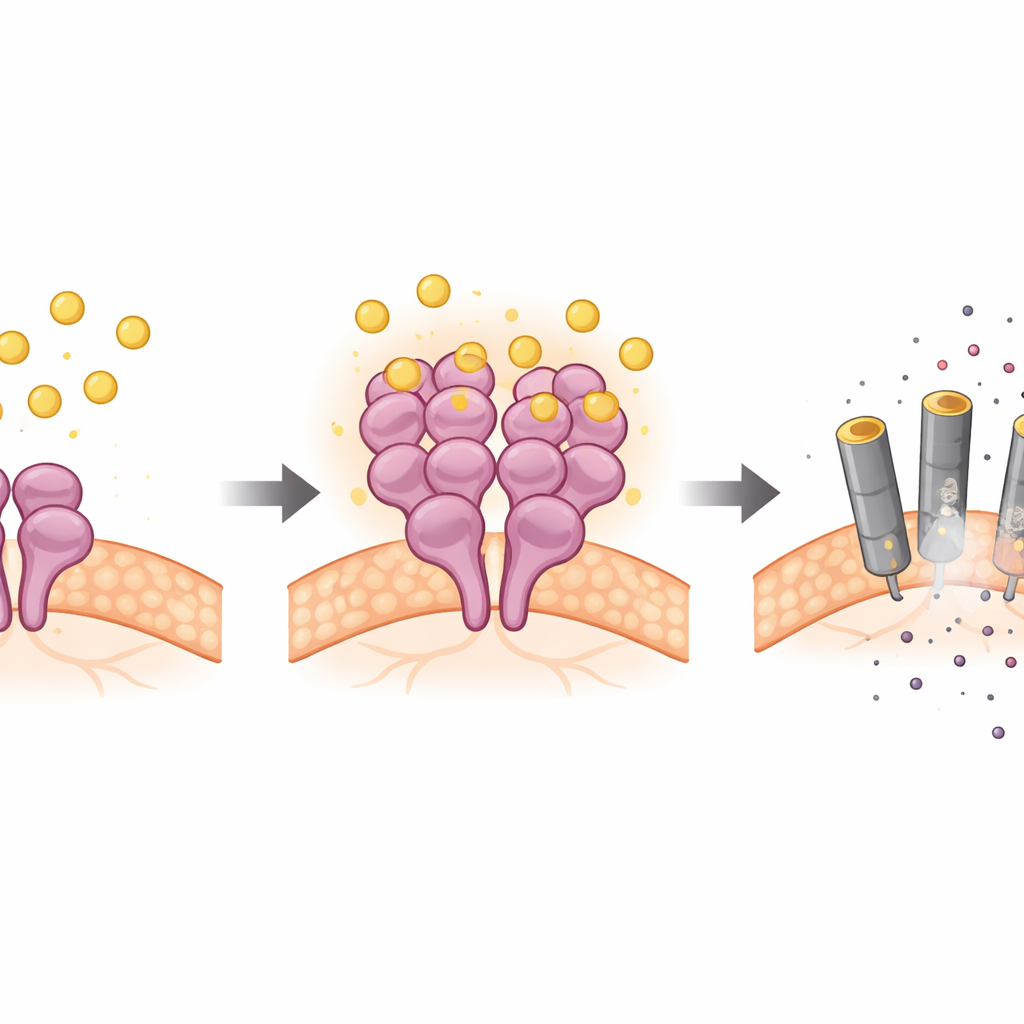
Usando neuronas en cultivo, cortes cerebrales y modelos murinos, los científicos demostraron que la bilirrubina activa selectivamente RIPK3 y su socio descendente MLKL en las células nerviosas, mientras que las proteínas habituales aguas arriba permanecen en gran medida sin cambios. Experimentos genéticos revelaron que cuando se eliminaba RIPK3 o MLKL, la bilirrubina ya no podía matar neuronas de manera eficiente. Pruebas bioquímicas fueron más allá: la bilirrubina se unía físicamente a RIPK3 en dos puntos específicos dentro de su núcleo activo, fomentaba la agregación de moléculas de RIPK3 y aumentaba su actividad quinasa —la función química que enciende la vía de muerte. Este agarre directo sobre RIPK3 no dependía de la superficie de interacción típica de la proteína (el dominio RHIM) ni de otros adaptadores, marcando una vía no clásica hacia la necroptosis.
Evidencia desde el cerebro vivo
Para comprobar si este mecanismo importa en animales enteros, el equipo elevó los niveles de bilirrubina en ratones ya fuera inyectándola en el cerebro o provocando lesión e inflamación hepática de modo que la bilirrubina entrara al cerebro de forma natural. En ratones normales, esto condujo a una marcada activación de RIPK3 y MLKL en regiones cerebrales vulnerables, aumento de marcadores de muerte celular y pérdida visible de neuronas sanas. Ratones diseñados para carecer de RIPK3 estuvieron protegidos: sus neuronas mostraron mucho menos daño, menos señales de muerte y respuestas inflamatorias reducidas, a pesar de que los niveles de bilirrubina eran igualmente altos. Es importante destacar que una forma procesada y soluble en agua de la bilirrubina, que normalmente se considera inocua, ni activó RIPK3 ni provocó lesiones cerebrales similares, subrayando que la forma no modificada y liposoluble es la verdadera culpable.
Qué significa esto para los pacientes
Este trabajo revela que el exceso de bilirrubina no conjugada puede activar directamente RIPK3, desencadenando una ruptura controlada pero destructiva de las células cerebrales mediante necroptosis. En lugar de actuar solo como un veneno general o fuente de estrés oxidativo, la bilirrubina se comporta como un activador de pequeña molécula de un programa de muerte específico en neuronas y células inmunitarias cerebrales. Para pacientes con ictericia severa o insuficiencia hepática, esto sugiere que bloquear RIPK3 o MLKL —especialmente con fármacos capaces de penetrar el cerebro— podría algún día ayudar a limitar el daño neurológico. En términos simples, el estudio muestra cómo un pigmento normalmente útil puede convertirse en un asesino molecular preciso y apunta a nuevas formas de desactivarlo sin alterar sus funciones protectoras cotidianas.
Cita: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Palabras clave: neurotoxicidad de la bilirrubina, necroptosis, RIPK3, insuficiencia hepática y lesión cerebral, vías de muerte celular