Clear Sky Science · es
Las variantes de pérdida de función en ODAD1 alteran el acoplamiento de los ODA e inducen una remodelación del citoesqueleto de actina en la discinesia ciliar primaria
Cuando los cepillos microscópicos del cuerpo fallan
Cada respiración depende de ejércitos de diminutas estructuras similares a pelos llamadas cilios, que barrean moco, gérmenes y polvo fuera de las vías respiratorias. En personas con una rara enfermedad hereditaria llamada discinesia ciliar primaria, o DCP, estos cepillos microscópicos no funcionan correctamente, lo que provoca tos persistente, infecciones pulmonares y, a veces, una inversión en la colocación de los órganos en el cuerpo. Este estudio descubre cómo los cambios dañinos en un solo gen, ODAD1, no solo desactivan los motores internos de los cilios, sino que también reorganizan de forma inesperada el andamiaje de las células que los albergan, revelando un nuevo punto débil de la enfermedad potencialmente abordable con fármacos.
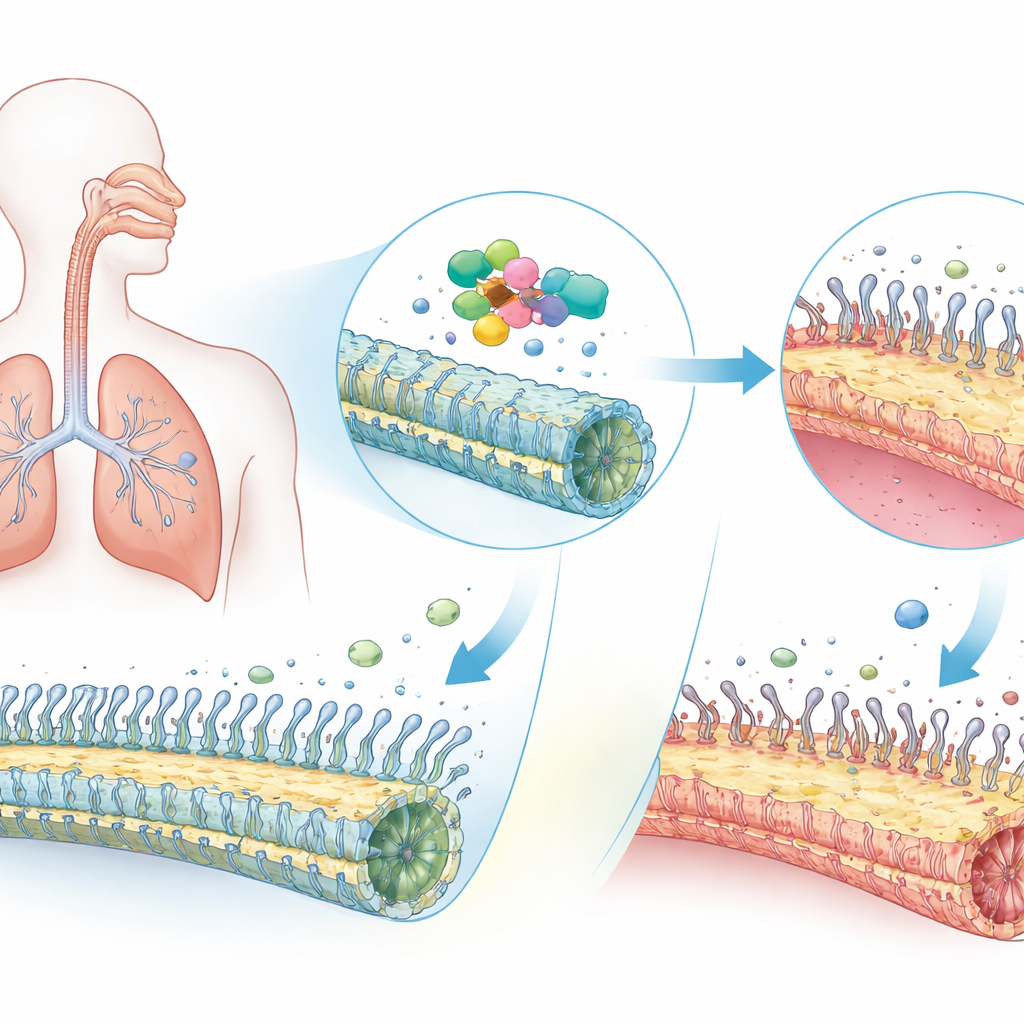
Una enfermedad pulmonar poco común con grandes consecuencias
La DCP afecta a aproximadamente una de cada varios miles de personas en todo el mundo y suele manifestarse en la infancia. Como los cilios que recubren la nariz y los pulmones no pueden latir eficazmente, el moco y los microbios atrapados persisten, provocando sinusitis crónica, infecciones de oído y daño pulmonar progresivo. Muchos pacientes también presentan “situs inversus”, en el que el corazón y otros órganos quedan volteados de izquierda a derecha, un indicio de que los cilios no guiaron correctamente el plan corporal temprano del embrión. Los médicos saben desde hace tiempo que fallos en docenas de genes diferentes pueden causar DCP. ODAD1 es uno de esos genes y ayuda a anclar los motores moleculares que impulsan el movimiento parecido a un látigo de cada cilio. Pero los científicos aún no comprendían del todo cómo se manifiestan los defectos de ODAD1 en el tejido respiratorio humano.
Rastreando un gen defectuoso en las células de pacientes
Los investigadores estudiaron a nueve personas de siete familias han chinas que mostraban signos clásicos de DCP: problemas respiratorios neonatales, tos húmeda toda la vida, infecciones pulmonares frecuentes y niveles inusualmente bajos de óxido nítrico en el aire exhalado, un sello clínico de la enfermedad. Las pruebas genéticas revelaron cuatro versiones dañinas del gen ODAD1, incluida una nunca antes descrita. Todas las variantes defectuosas redujeron drásticamente o eliminaron la proteína ODAD1 normal en las células de la mucosa nasal. Cuando el equipo filmó los cilios de las muestras de los pacientes a alta velocidad, observaron que el habitual latido suave y ondulatorio se reemplazó por un parpadeo débil y desorganizado. Los cultivos de laboratorio derivados de estas células, que recrean un delgado revestimiento ciliado de las vías aéreas en una interfaz aire‑líquido, mostraron el mismo movimiento lento y descoordinado.
Dentro de las micromáquinas rotas
Para ver qué fallaba físicamente, los científicos recurrieron a potentes técnicas de imagen. La microscopía electrónica convencional y la criomicroscopía electrónica de última generación revelaron que las unidades motoras externas y sus sitios de anclaje estaban completamente ausentes en los cilios de los pacientes. En algunos casos, otras estructuras clave en el núcleo ciliar también estaban descolocadas o malformadas. Estos defectos explican por qué los cilios no pueden generar suficiente fuerza para mover el moco. Sin embargo, el daño iba más allá de los propios cilios. La superficie de las vías aéreas en los cultivos derivados de los pacientes albergaba muchas menos células multiciliadas, y las restantes estaban espaciadas de forma extraña y agrandadas, con sus cilios apuntando en direcciones mixtas. Sorprendentemente, el número de “cuerpos basales” internos por célula —las semillas de las que brotan los cilios— era normal, lo que sugiere que el problema residía en cómo se organizaban estas células en la superficie del tejido más que en cuántos cilios intentaban construir.
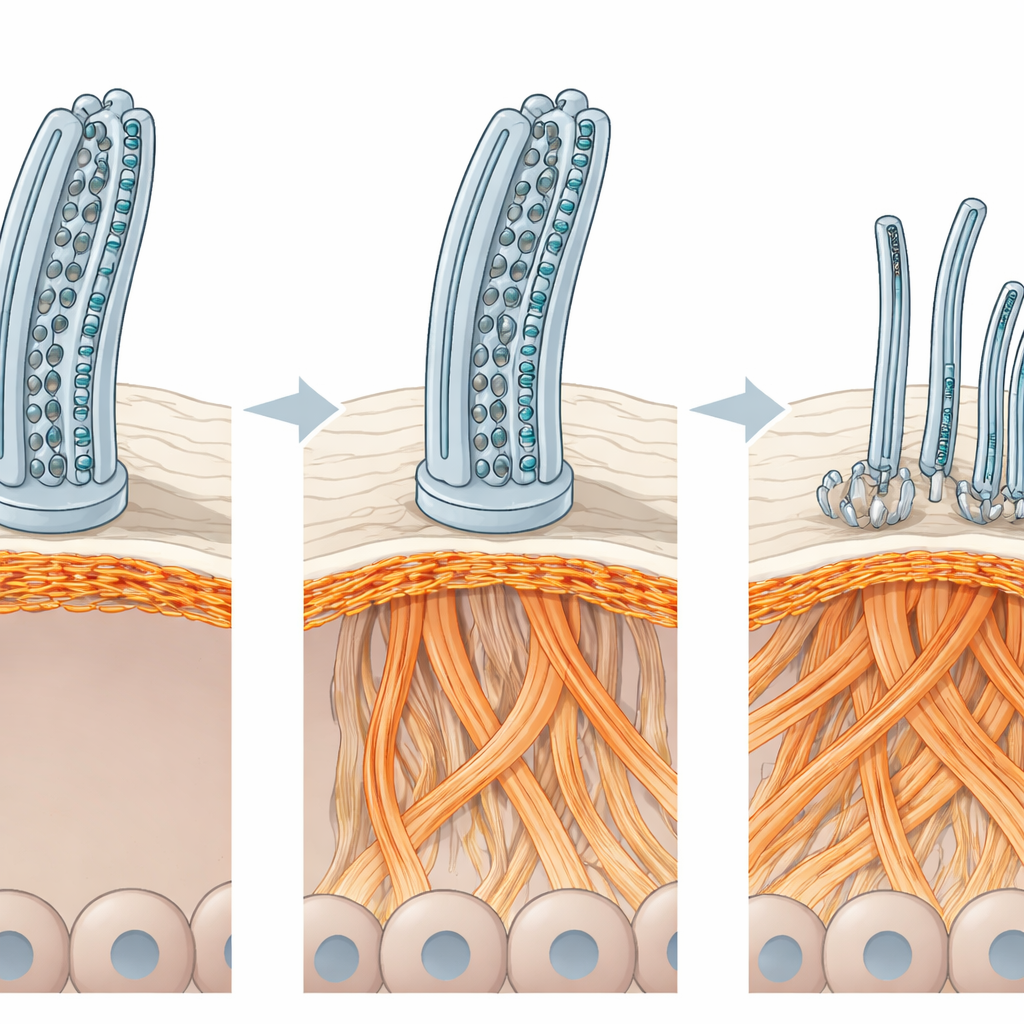
El andamiaje interior de la célula se reprograma
Para precisar qué interrumpía esa organización, el equipo midió miles de proteínas en los cultivos de las vías aéreas derivados de los pacientes. Si bien muchas proteínas relacionadas con los cilios estaban reducidas, varias proteínas vinculadas a la actina —las fibras versátiles que forman gran parte del andamiaje interno de la célula— eran más abundantes. La imagen de los filamentos de actina confirmó una remodelación drástica de ese andamiaje: haces de actina engrosados en la parte superior de las células multiciliadas, redes comprimidas en los bordes celulares y parches agrupados más profundos en el tejido. Estos cambios no eran exclusivos del trasfondo genético de los pacientes; generar por ingeniería un knockout de ODAD1 en células sanas produjo la misma reprogramación de la actina y la pérdida de células multiciliadas. Cuando los investigadores perturbaron suavemente el ensamblaje de la actina con un fármaco de pequeña molécula, el número de células multiciliadas y su distribución superficial se recuperaron parcialmente, y los cilios se volvieron más numerosos y mejor organizados, aunque seguían sin poder latir normalmente sin el papel de acoplamiento motor de ODAD1.
Restaurar la pieza que falta y mirar al futuro
Finalmente, los investigadores evaluaron si reemplazar ODAD1 podía devolver el movimiento ciliar. Cultivaron organoides de las vías aéreas “apical‑out”: esferas huecas en miniatura de tejido respiratorio con los cilios orientados hacia el exterior, a partir de células de los pacientes, y utilizaron un vector lentiviral para introducir una copia funcional de ODAD1. La proteína introducida se integró correctamente en los cilios, restauró los sitios de acoplamiento de los motores que faltaban y devolvió el latido ciliar a una velocidad y patrón cercanos a la normalidad. En conjunto, estos resultados muestran que la pérdida de ODAD1 perjudica las vías aéreas de dos maneras: desactiva directamente el sistema motor de los cilios y, de forma indirecta, desordena el andamiaje de actina que configura la superficie ciliada. Para los pacientes, esta doble perspectiva sugiere un futuro terapéutico con dos frentes: terapias génicas para corregir el defecto motor primario y estrategias más seguras que modulen la actina para ayudar a reconstruir un tapiz saludable de cilios que vuelva a mantener los pulmones limpios.
Cita: Huo, C., Luo, T., Yang, S. et al. Loss-of-function variants in ODAD1 disrupt ODA docking and induce actin cytoskeletal remodeling in primary ciliary dyskinesia. Cell Discov 12, 25 (2026). https://doi.org/10.1038/s41421-026-00875-8
Palabras clave: discinesia ciliar primaria, ODAD1, cilios móviles, citoesqueleto de actina, terapia génica