Clear Sky Science · es
Tubería integradora de perfilado espacial para determinar arquitecturas del TME en muestras clínicas archivadas usando la tecnología superplex CmTSA
Por qué importa el paisaje oculto alrededor de los tumores
Los cánceres no crecen aislados. Están rodeados por un vecindario activo de células inmunitarias, células de soporte, vasos sanguíneos y tejido con aspecto cicatricial que, en conjunto, forman el “microambiente” tumoral. Este artículo presenta una forma práctica de cartografiar ese paisaje oculto con detalle usando muestras de tejido estándar de los hospitales. Al revelar qué tipos de células se sitúan unas junto a otras y cómo se organizan en vecindarios útiles o dañinos, el método podría ayudar a los médicos a predecir mejor el comportamiento del cáncer de un paciente y qué tratamientos tienen más probabilidad de funcionar.
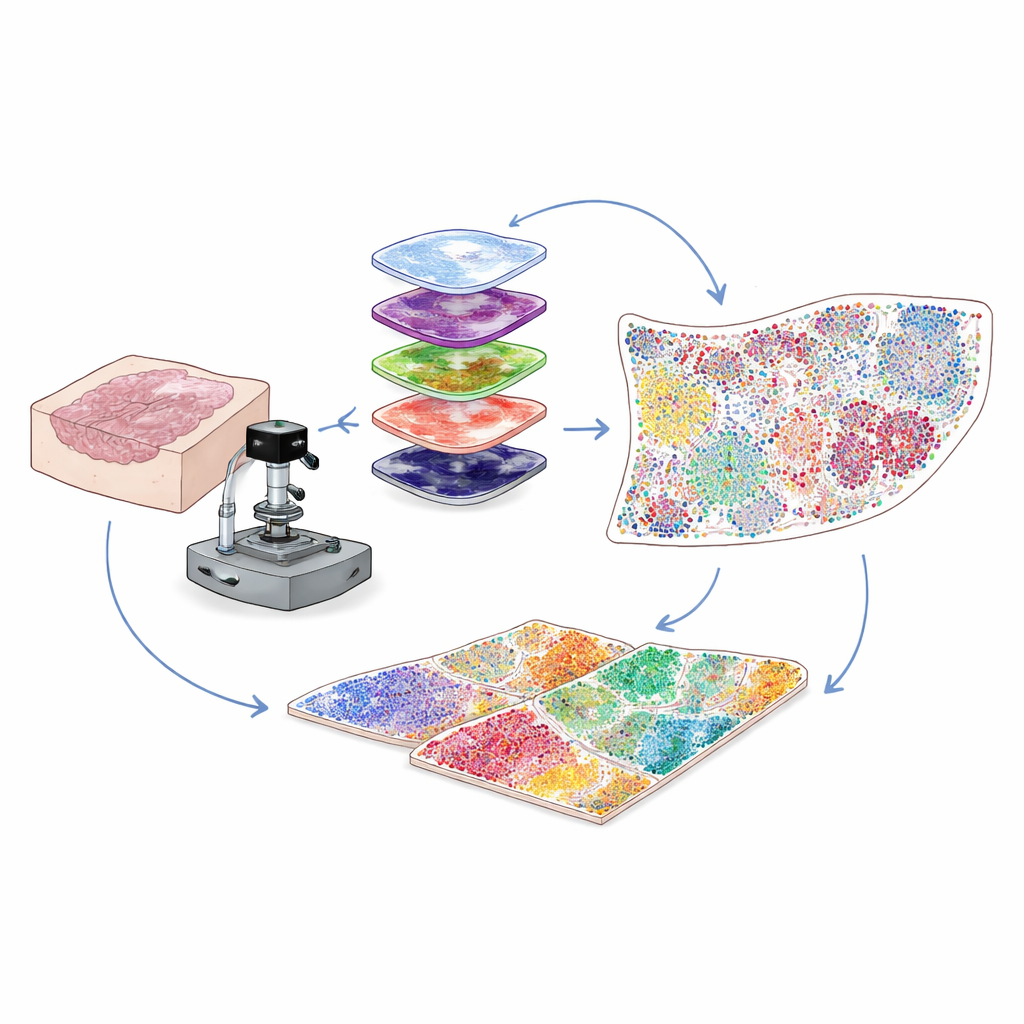
Ver más en las muestras rutinarias de hospital
La mayoría de las muestras clínicas de cáncer se conservan como finas láminas de tejido embebido en parafina, conocidas como bloques FFPE, que pueden almacenarse durante años. Son una mina de oro para la investigación, pero un problema técnico ha limitado a los científicos: estas muestras emiten fluorescencia de fondo natural que ahoga las señales tenues de muchas proteínas importantes. Los autores resolvieron esto combinando luz intensa cuidadosamente ajustada con un tratamiento químico suave para borrar selectivamente ese resplandor de fondo sin dañar el tejido ni los objetivos protéicos. Este paso híbrido de “blanqueamiento” óptico y químico mejora notablemente la claridad de la imagen, permitiendo detectar señales proteicas débiles que de otro modo se perderían.
Pintar docenas de marcas proteicas en la misma lámina
Para entender qué células están presentes y qué están haciendo, los científicos tiñen los tejidos con anticuerpos que se unen a proteínas específicas. Los métodos multiplex tradicionales o bien tienen problemas de baja intensidad de señal para proteínas raras o solo pueden seguir un número limitado de marcadores a la vez. Aquí, el equipo utiliza un enfoque llamado amplificación cíclica de señal por tirosina (cyclic tyramide signal amplification). En cada ronda, se tiñe un pequeño conjunto de marcadores y se “desarrollan” enzimáticamente en puntos fluorescentes brillantes y permanentes. Luego los anticuerpos se eliminan suavemente mientras la señal permanece, se vuelve a blanquear el fondo y se añade el siguiente conjunto de marcadores. Repitiendo este ciclo muchas veces y alineando las imágenes usando la señal constante de los núcleos celulares, pueden visualizar de forma fiable entre 30 y 60 proteínas diferentes en una sola lámina de tejido, a lo largo de todo el portaobjetos, con resolución de célula individual.
Convertir imágenes coloridas en un atlas célula por célula
Las imágenes de alto número de plex contienen millones de píxeles, mucho más de lo que un humano podría analizar a simple vista. Por eso los autores construyen una canalización de visión por ordenador que primero encuentra y delimita cada núcleo celular usando herramientas de aprendizaje profundo desarrolladas originalmente para segmentación celular general. Luego, en función de dónde aparece la fluorescencia de cada proteína —en la membrana, en el citoplasma o en el núcleo— y de conjuntos de reglas lógicas, cada célula se asigna a un tipo o subtipo, como célula tumoral, célula T cooperadora, célula T citotóxica, célula B, fibroblasto u otros. El resultado es una tabla digital que enumera, para cada célula en la lámina, su identidad y sus coordenadas exactas. Esto transforma una imagen compleja en un mapa cuantitativo de quién está dónde dentro del microambiente tumoral.
Revelando vecindarios celulares que moldean el pronóstico
Las células rara vez actúan solas; lo que importa son sus vecinos. Para capturar esto, los investigadores prueban distintas formas de definir vecindarios locales alrededor de cada célula y se decantan por un enfoque de red basado en radios. Imaginen dibujar un pequeño círculo —aproximadamente el grosor de un cabello humano— alrededor de cada célula y listar quién vive dentro de él. Agrupando células cuyos círculos circundantes tienen mezclas similares de vecinos, el método identifica “nichos funcionales” recurrentes, como zonas ricas en células inmunitarias, barreras dominadas por fibroblastos o regiones dominadas por el tumor. Aplicando esta estrategia al tejido de colon, muestran que los vecindarios basados en radios se alinean mejor con estructuras anatómicas conocidas que otros métodos. En muestras de cáncer de cuello uterino de pacientes con buenos frente a malos resultados, el equipo encuentra que los nichos ricos en células inmunitarias se agrupan cerca del borde tumoral en pacientes con buen pronóstico, mientras que los pacientes con peores resultados muestran zonas densas en fibroblastos que envuelven las células tumorales y parecen aislar a las células inmunitarias atacantes.
De mapas espaciales a tratamiento a medida
Combinando tinciones de alta calidad y asequibles para muchas proteínas con un análisis de imagen robusto, este trabajo ofrece una canalización integral que puede aplicarse a grandes cantidades de muestras hospitalarias estándar. El método convierte tejido preservado en mapas detallados de cómo se organizan e interactúan células tumorales, inmunitarias y estromales. Para el lector general, la conclusión es que no solo importan los tipos de células, sino sus patrones de vecindario precisos a la hora de determinar cómo se comporta un cáncer. Esta plataforma puede ayudar a los investigadores a localizar puntos inmunitarios protectores, identificar barreras celulares supresoras y, en última instancia, respaldar pronósticos más precisos y estrategias de inmunoterapia más finamente ajustadas.
Cita: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Palabras clave: microambiente tumoral, proteómica espacial, imagen multiplex, inmunología del cáncer, análisis de una sola célula