Clear Sky Science · es
Cronobiología de los virus neurotrópicos: entrada vírica rítmica y relojes hospedadores arrítmicos
Por qué el momento del día importa en las infecciones cerebrales
Muchos virus peligrosos, entre ellos la rabia y el herpes, tienen especial habilidad para invadir el cerebro y los nervios. Este estudio plantea una pregunta sorprendentemente simple pero con grandes implicaciones: ¿cambia la facilidad con la que estos virus “neurotrópicos” acceden a nuestro sistema nervioso según la hora del día, y pueden los propios virus desajustar nuestros relojes internos? Comprender este diálogo bidireccional entre los relojes biológicos y los virus podría abrir nuevas formas de programar vacunas, antivirales e incluso turnos de trabajo para reducir el riesgo.
Relojes corporales diarios y las puertas de entrada virales
Casi todas las células del cuerpo cuentan con un sistema de temporización interno de 24 horas, a menudo llamado reloj circadiano. Está impulsado por un conjunto de proteínas centrales del reloj, entre ellas BMAL1 y REV-ERBα, que activan y silencian miles de genes en olas rítmicas. Los autores se centraron en las “manillas” de las puertas que los virus usan para entrar en las células —proteínas receptoras en la superficie celular— para docenas de virus que se dirigen o invaden el cerebro. Al examinar organoides con características cerebrales derivados de células madre, líneas celulares de origen nervioso y tejidos de ratón, encontraron que la mayoría de estos receptores virales aumentan y disminuyen a lo largo del día. Estos ritmos seguían de cerca la actividad de componentes del reloj, lo que sugiere que nuestro sistema de temporización diario controla de forma silenciosa cuántos puntos de entrada virales están disponibles en cada hora.
Un factor del ciclo celular se convierte en mensajero del reloj
Al profundizar, los investigadores preguntaron cómo encaja en esta red temporal una proteína conocida habitualmente por controlar la división celular, llamada E2F8. Descubrieron que E2F8 está bajo control circadiano y actúa como un relevo entre el reloj y al menos un receptor clave de la rabia, p75NTR. Cuando la proteína del reloj REV-ERBα está activa, suprime E2F8. A su vez, niveles bajos de E2F8 liberan la represión sobre el gen p75NTR, permitiendo que se produzca más de este receptor y haciendo las células más receptivas al virus de la rabia. De forma llamativa, E2F8 también retroalimenta sobre el reloj: puede unirse directamente a las regiones de control de genes centrales del reloj como REV-ERBα y PER2 y amortiguar su actividad. Esto crea un bucle de retroalimentación en el que un regulador del ciclo celular ayuda a esculpir los ritmos diarios y, a través de ellos, la vulnerabilidad de las células nerviosas a la infección.
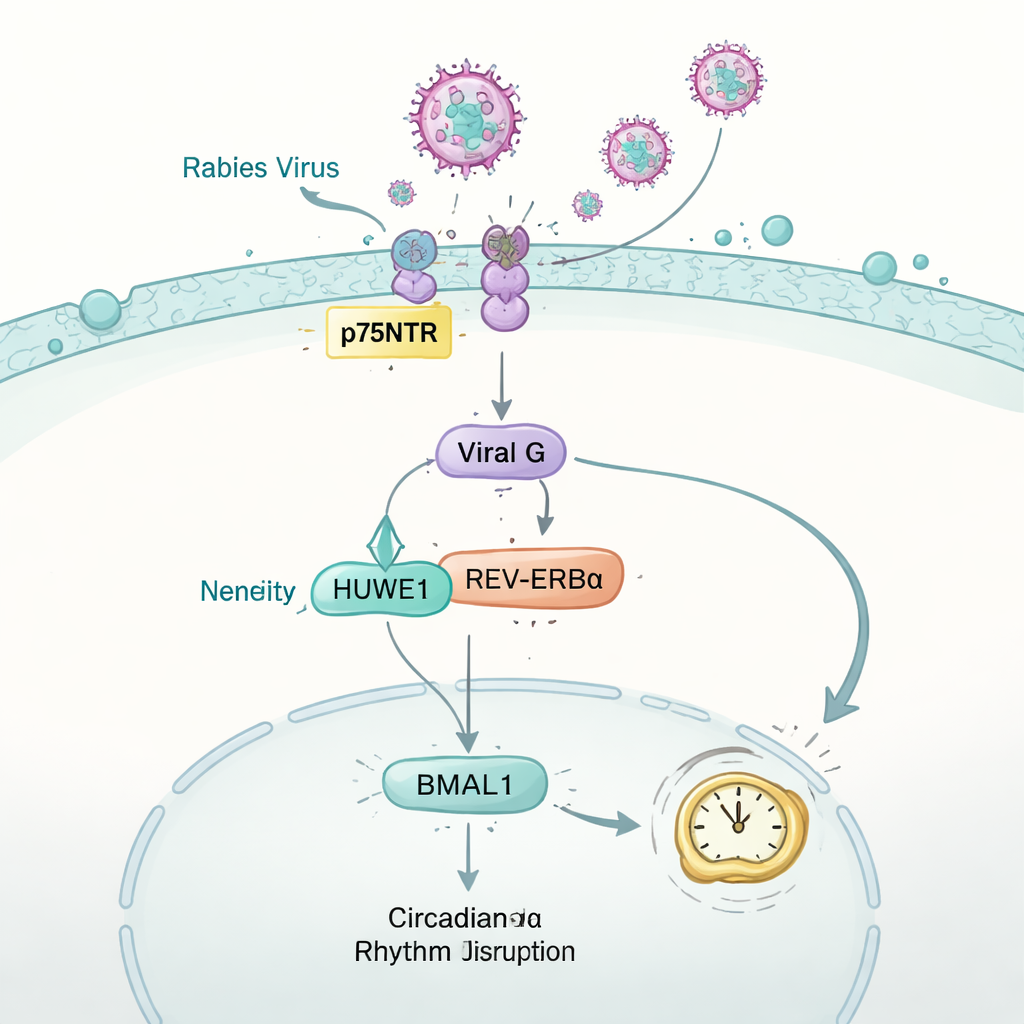
Cómo el virus de la rabia descarrila el reloj
El estudio invirtió luego la pregunta: ¿puede un virus contraatacar al reloj? Usando ratones infectados con el virus de la rabia, el equipo monitorizó la actividad al correr, el metabolismo y la química respiratoria. A pesar de una ingesta de alimento normal al inicio de la infección, los animales perdieron gradualmente los patrones regulares de día y noche que muestran los ratones sanos. En el cerebro y varios otros órganos, los niveles de la crucial proteína del reloj BMAL1 cayeron bruscamente. En células de tipo nervioso, este efecto pudo rastrearse hasta la glicoproteína “G” de la rabia, una proteína de superficie que normalmente ayuda al virus a fusionarse con las células. G secuestró a una enzima hospedadora llamada HUWE1, que suele marcar para su eliminación a otra proteína del reloj, REV-ERBα. Al competir por HUWE1, la proteína viral G estabilizó REV-ERBα, lo que condujo a una supresión adicional de BMAL1 y, en última instancia, a la perturbación del mecanismo reloj que mantiene la fisiología en un ciclo de 24 horas.
Momento, desfase horario y gravedad de la infección
Para comprobar si estos cambios moleculares importan a nivel del organismo completo, el equipo infectó ratones con rabia en distintos momentos del día, bajo ciclos luz‑oscuridad regulares, en condiciones crónicas de “jet lag” y en animales genéticamente carentes de REV-ERBα. Los ratones infectados al comienzo de su fase activa (noche), cuando el receptor de la rabia p75NTR alcanza su pico, perdieron peso más rápido, presentaron cargas virales mayores en múltiples regiones cerebrales, más inflamación cerebral y murieron antes que los ratones infectados al inicio de su fase de reposo. Los ratones expuestos a cambios de fase repetidos que imitan el trabajo por turnos rotativos perdieron los ritmos normales del reloj en el cerebro, mostraron niveles persistentemente más altos de p75NTR, tuvieron señales antivirales basales más débiles y sufrieron una enfermedad más grave. En contraste, los ratones sin REV-ERBα expresaron menos p75NTR, presentaron cargas virales más bajas y sobrevivieron más tiempo tras la infección, lo que indica que este componente del reloj es un guardián crítico de la gravedad de la rabia.
Qué significa esto para las personas
En términos sencillos, el estudio muestra que nuestros relojes internos no solo fijan los horarios de sueño; también abren y cierran puertas moleculares que usan los virus que invaden el cerebro, y esos mismos virus pueden contraatacar desordenando el reloj. Un único factor, REV-ERBα, se sitúa en una intersección clave: junto con E2F8 moldea tanto los niveles de receptores como la temporización diaria, mientras que el virus de la rabia lo manipula en su propio beneficio. Estos hallazgos sugieren vías prácticas. Las vacunas o los antivirales podrían funcionar mejor en ciertos momentos del día, cuando los receptores son bajos o las respuestas inmunitarias son más fuertes. Las personas con ritmos crónicamente alterados —como trabajadores por turnos o viajeros frecuentes— podrían enfrentar mayores riesgos frente a algunas infecciones neurotrópicas. Apuntar a REV-ERBα o a vías relacionadas podría ayudar a inclinar la balanza a favor del hospedador, haciendo las infecciones menos graves y mejorando los resultados.
Cita: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Palabras clave: reloj circadiano, virus neurotrópicos, rabia, receptores virales, cronoterapia