Clear Sky Science · es
Cambios dinámicos del microambiente inmune en el cáncer de ovario tras la quimioterapia neoadyuvante
Por qué esta investigación importa a las mujeres con cáncer de ovario
El cáncer de ovario avanzado suele tratarse con quimioterapia potente antes o después de la cirugía, sin embargo muchas mujeres ven cómo su enfermedad reaparece y deja de responder a los fármacos. Este estudio plantea una pregunta urgente: ¿cómo remodela la quimioterapia, de forma silenciosa, las defensas propias del cuerpo alrededor del tumor, y podemos ajustar esa respuesta para que el tratamiento funcione durante más tiempo? Al analizar células individuales y probar nuevas combinaciones de fármacos en ratones, los investigadores revelan un papel oculto de unas moléculas grasas similares a hormonas, llamadas prostaglandinas, en la ayuda que reciben los tumores para evadir al sistema inmune tras la quimioterapia.
Un campo de batalla cambiante alrededor del tumor
Los tumores de ovario no crecen aislados: se asientan en un “vecindario” concurrido de células inmunes, tejido conectivo y líquido abdominal. Antes del tratamiento, este entorno ya está inclinado a favor del cáncer, con pocas células T citotóxicas activas y muchas células que atenúan el ataque inmunitario. El equipo analizó datos de secuenciación de ARN unicelular publicados anteriormente en mujeres con cáncer seroso de alto grado, comparando muestras tomadas antes y después de la quimioterapia neoadyuvante (quimioterapia administrada antes de la cirugía). Encontraron que la quimioterapia no se limitó a matar células tumorales; también agitó temporalmente la actividad inmune, aumentando señales vinculadas a la estimulación de las células T y la inflamación, mientras reducía algunas células T reguladoras que normalmente suprimen el ataque.
Cuando los cambios útiles se vuelven perjudiciales
A pesar de este impulso breve, la mayoría de las pacientes recae y desarrolla resistencia a fármacos con platino como el cisplatino. Para entender por qué, los investigadores indagaron más en cómo se comunican entre sí los distintos tipos celulares después del tratamiento. Descubrieron que la quimioterapia aumentó marcadamente los genes implicados en la síntesis de prostaglandinas en macrófagos asociados al tumor y fibroblastos, y potenció la comunicación entre estas células y las células T. Utilizando herramientas matemáticas avanzadas, demostraron que el entorno global se desplazó hacia un estado proinflamatorio pero en última instancia supresor, con niveles crecientes de quimioquinas que atraen células mieloides y vías reforzadas que pueden agotar las células T con el tiempo. Esto sugiere que las prostaglandinas podrían actuar como un interruptor molecular, convirtiendo una oleada inmune inicialmente útil en un freno duradero sobre la inmunidad antitumoral.
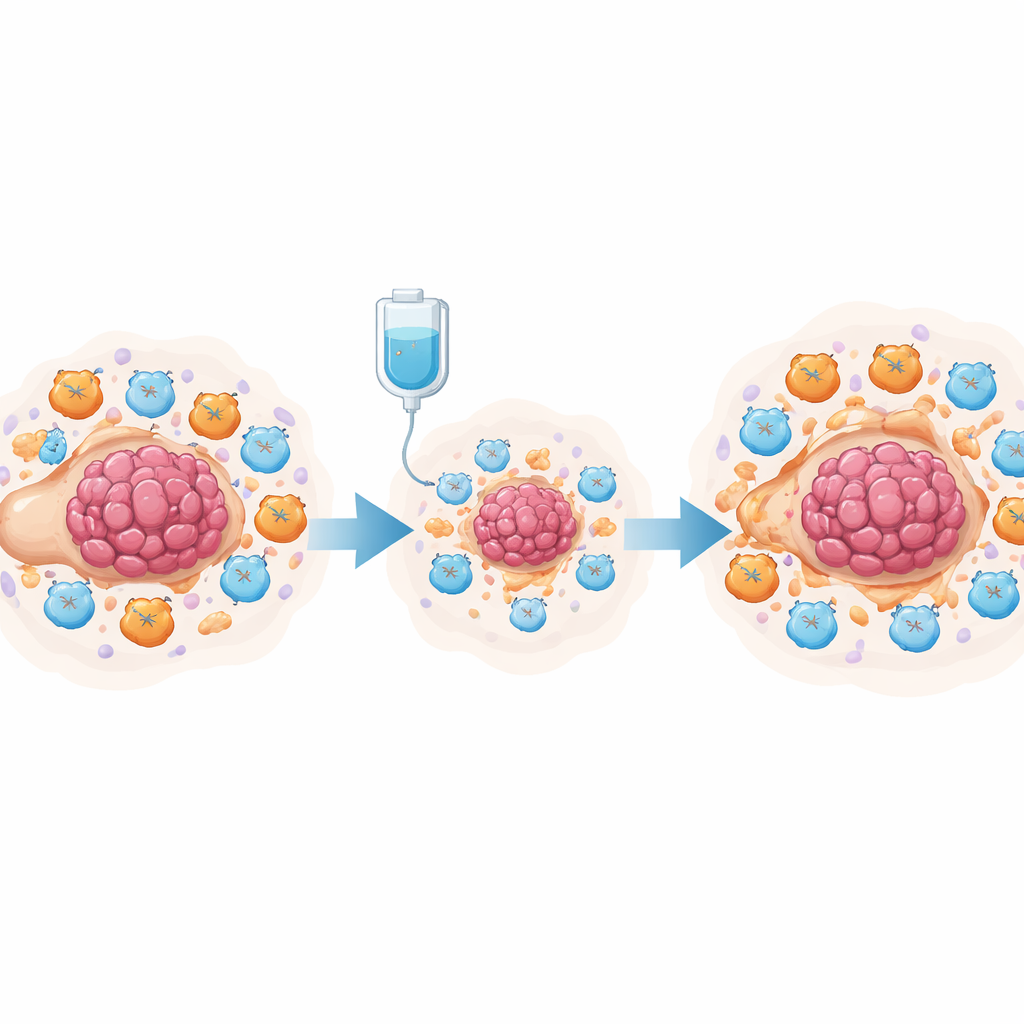
Quimioterapia, prostaglandinas y células T silenciadas
Para poner a prueba esta idea experimentalmente, el equipo usó un modelo murino de cáncer de ovario tratado con cisplatino. El análisis unicelular de decenas de miles de células del cavidad abdominal mostró que el cisplatino redujo las células tumorales e incrementó el total de células T, pero también expandió de forma marcada las células supresoras derivadas de la médula (MDSC) y las células T citotóxicas exhaustas. Tanto las células tumorales como estas células supresoras producían altos niveles de las enzimas para fabricar prostaglandinas. En cultivos mixtos, las células tumorales tratadas con cisplatino inducían a las células de médula ósea a adoptar un estado similar a MDSC y debilitaban la actividad y proliferación de las células T CD8+ citotóxicas. Los investigadores trazaron este efecto hasta la vía de señalización NF-κB en las células tumorales, que activó el gen PTGES, un paso clave en la producción de prostaglandina E2. Bloquear esta vía redujo los niveles de PTGES y la producción de prostaglandinas.
Girar la marea con terapia combinada
La cuestión más práctica era si bloquear las prostaglandinas podría mejorar la eficacia de la quimioterapia. En ratones, los científicos utilizaron la eliminación genética de Ptges en las células tumorales, anticuerpos que neutralizan la prostaglandina E2, o fármacos de pequeña molécula que inhiben la prostaglandina E sintasa. Todos estos enfoques disminuyeron los niveles de prostaglandinas, redujeron la acumulación de MDSC y restauraron la capacidad citotóxica y la resiliencia con características de célula madre de las células T CD8+. Cuando se combinaron con cisplatino, o con el régimen estándar cisplatino-paclitaxel, los inhibidores de prostaglandinas ralentizaron el crecimiento y la diseminación tumoral con más eficacia que la quimioterapia sola. Los datos indican que la supresión inmune impulsada por prostaglandinas no es una nota al margen, sino una razón central por la que los tumores escapan tras una respuesta inicial.
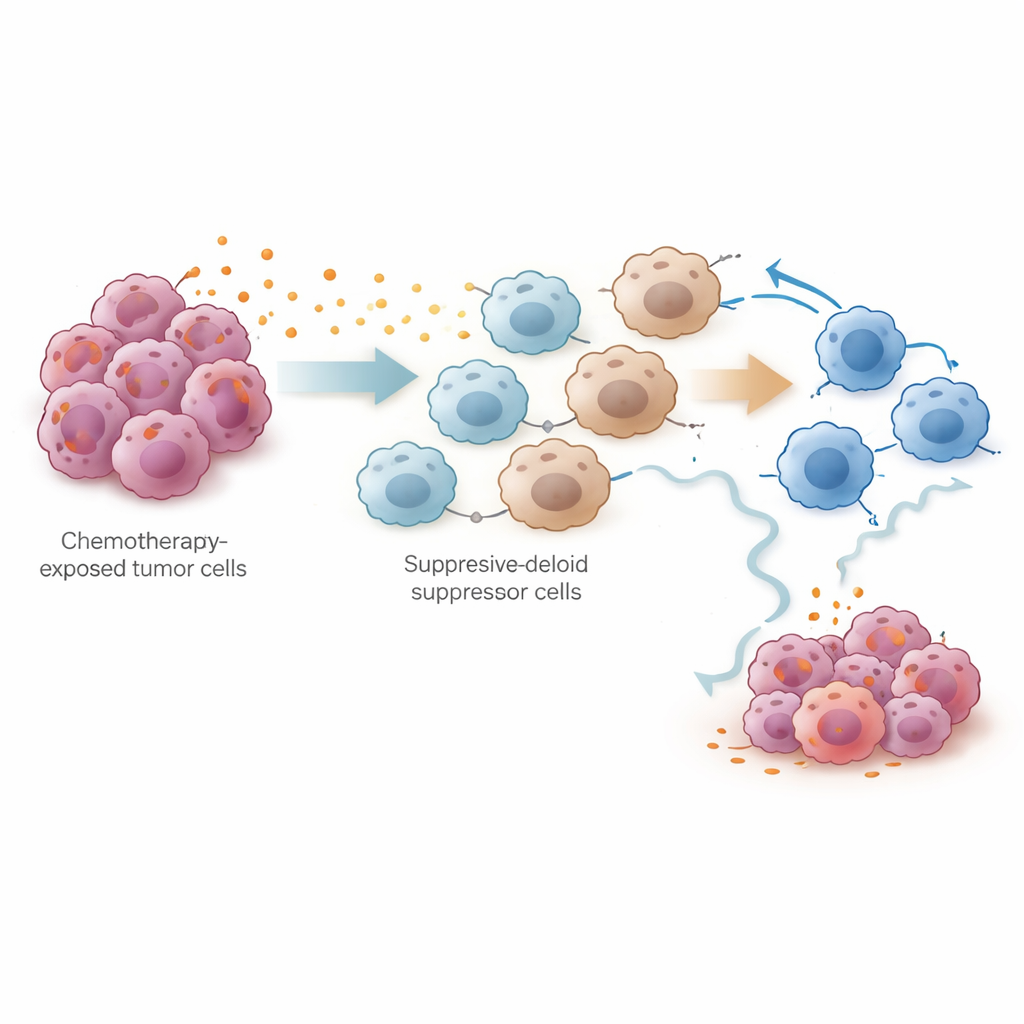
Un nuevo enfoque para mantener la eficacia del tratamiento
En términos cotidianos, este trabajo sugiere que la quimioterapia cambia el entorno del tumor en dos fases: primero debilita el cáncer y moviliza brevemente al sistema inmune, pero luego desencadena una oleada de prostaglandinas que reclutan células supresoras y agotan las fuerzas naturales del organismo para matar tumores. Al identificar la producción de prostaglandinas dirigida por PTGES como un culpable clave, el estudio apunta a una estrategia tangible: combinar la quimioterapia estándar con platino con fármacos que bloqueen las vías de las prostaglandinas podría ayudar a mantener un ataque inmunitario sostenido y retrasar o prevenir la recaída en el cáncer de ovario. Aunque aún son necesarios ensayos clínicos, este enfoque combinado ofrece una dirección esperanzadora para prolongar el beneficio de los tratamientos existentes.
Cita: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Palabras clave: cáncer de ovario, microambiente tumoral, resistencia a la quimioterapia, prostaglandinas, inmunoterapia