Clear Sky Science · es
ATP6V1B2 alivia la esteatosis hepática al promover la acidificación lisosomal en los hepatocitos
Por qué importa un hígado graso
Mucha gente acumula grasa en el hígado sin darse cuenta. Esta condición, ahora denominada enfermedad hepática esteatósica asociada a la disfunción metabólica (MASLD), afecta aproximadamente a una cuarta parte de la población mundial y puede progresar silenciosamente hacia la fibrosis, insuficiencia hepática y otras enfermedades graves. Sin embargo, los médicos aún carecen de buenas herramientas para predecir quién empeorará y hay pocos tratamientos que apunten directamente a los problemas celulares de raíz. Este estudio revela cómo una poco conocida «bomba ácida» celular ayuda a las células hepáticas a eliminar el exceso de grasa y sugiere una nueva dirección para el diagnóstico y la terapia.
Un ayudante oculto dentro de las células hepáticas
Dentro de cada hepatocito hay pequeños centros de reciclaje llamados lisosomas. Dependen de un baño ácido interno para descomponer piezas desgastadas y el exceso de grasa. El ácido se mantiene gracias a una bomba molecular conocida como V-ATPasa, formada por varias subunidades proteicas. Los autores se centraron en una pieza crucial, ATP6V1B2, que es especialmente importante para mantener la acidez lisosomal. Se preguntaron si los cambios en esta proteína podrían ayudar a explicar por qué se acumula grasa en la MASLD y si sus niveles en sangre podrían señalar la enfermedad.
Pistas de pacientes y modelos animales
Al examinar bases de datos genéticos públicas y muestras de sangre de pacientes, los investigadores hallaron que los niveles de ATP6V1B2 eran consistentemente más bajos en personas con MASLD y aún más bajos en quienes tenían cirrosis, una forma grave de daño hepático. Niveles reducidos de ATP6V1B2 en el hígado se asociaron con más inflamación, peor fibrosis y mayores marcadores de lesión hepática en sangre. En modelos murinos alimentados con dietas ricas en grasas o deficientes en nutrientes —formas estándar de reproducir la MASLD— el suministro hepático de ATP6V1B2 también disminuyó. En conjunto, estos hallazgos sugieren que la pérdida de esta proteína no es solo un efecto secundario, sino que puede estar estrechamente ligada a la progresión de la enfermedad.
Qué falla dentro de las células hepáticas estresadas
Para ver qué sucede cuando ATP6V1B2 se altera, el equipo recurrió a hepatocitos en cultivo sobrecargados de ácidos grasos, imitando un entorno «lipotóxico». Cuando redujeron artificialmente ATP6V1B2, las gotas de grasa en las células se agrandaron, los subproductos oxidativos nocivos aumentaron y las centrales energéticas de la célula (mitocondrias) comenzaron a fallar. Las señales de estrés intracelular se dispararon y una enzima clave sintetizadora de grasas llamada sintasa de ácidos grasos (FASN) se elevó de forma notable. En contraste, cuando ATP6V1B2 se aumentó, las células manejaron mucho mejor la carga de grasa: las gotas lipídicas se redujeron, el estrés oxidativo disminuyó y las mitocondrias se recuperaron. Estos experimentos muestran que ATP6V1B2 actúa como un freno protector frente a la acumulación de grasa y el daño celular.
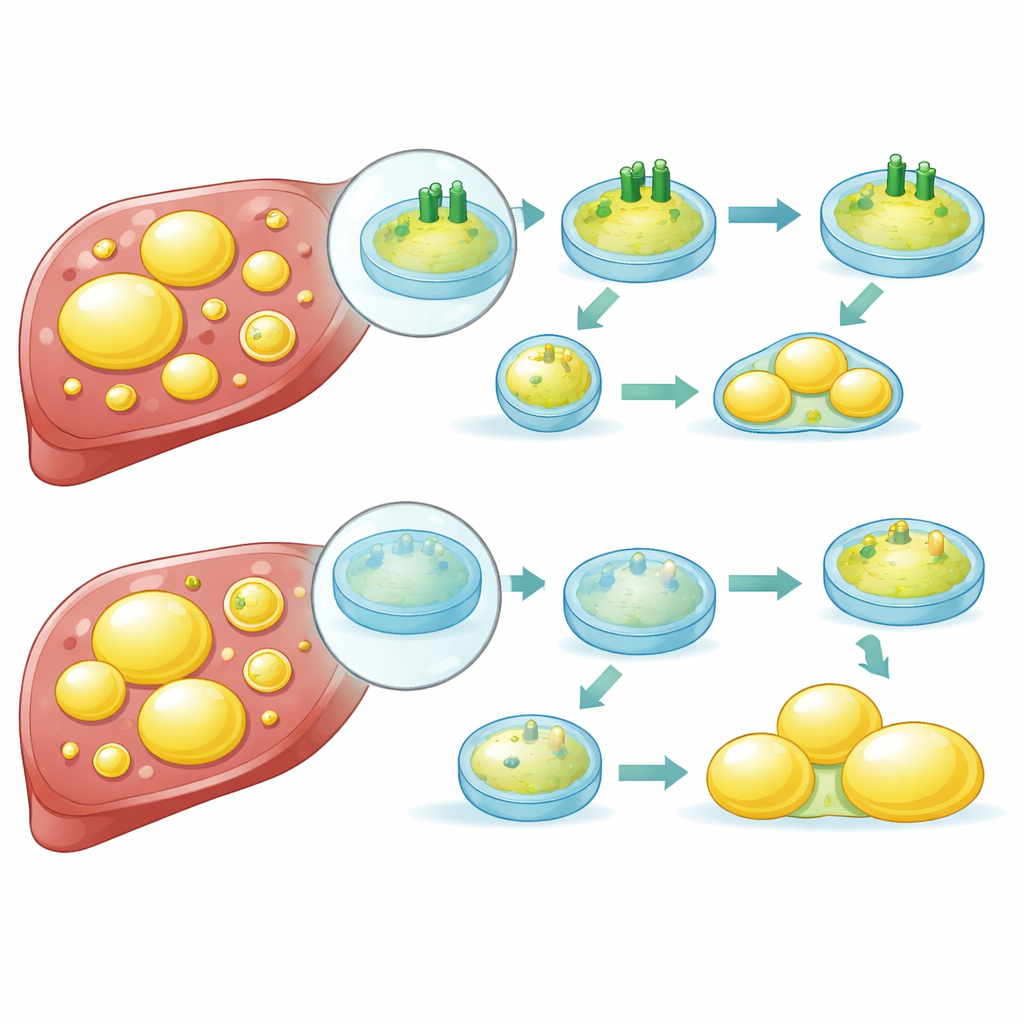
Cómo el reciclaje roto impulsa la acumulación de grasa
Ahondando más, los investigadores descubrieron que ATP6V1B2 controla cuán ácidos y activos permanecen los lisosomas. Cuando la proteína se reducían, los lisosomas perdían acidez, su capacidad para degradar contenido disminuía y el flujo de material a través del sistema de reciclaje celular (autofagia) se bloqueaba. En condiciones normales, FASN puede ser enviado a los lisosomas para su destrucción. Con niveles saludables de ATP6V1B2, esta vía funciona de forma eficiente, manteniendo a raya los niveles de FASN y limitando la producción de nueva grasa. Pero cuando ATP6V1B2 escasea, los lisosomas no pueden degradar correctamente a FASN. La enzima se acumula, la célula aumenta la síntesis de lípidos y las gotas de grasa siguen creciendo. El estudio también sugiere que las vías de estrés intracelular incrementan aún más la producción de FASN cuando ATP6V1B2 es baja, creando un círculo vicioso.
Lo que esto significa para la atención futura
Para lectores no especializados, el mensaje es claro: una sola proteína que ayuda a mantener la acidez lisosomal puede influir de forma decisiva en si las células hepáticas almacenan o eliminan grasa. Niveles bajos de ATP6V1B2, observados tanto en pacientes como en modelos de MASLD, debilitan el sistema interno de reciclaje del hígado, permitiendo que se acumule grasa y daño. Medir esta proteína en sangre podría ayudar a los médicos a evaluar la gravedad de la enfermedad, y estrategias que restauren la acidez lisosomal o aumenten la actividad de ATP6V1B2 podrían constituir la base de nuevos tratamientos. Al arrojar luz sobre esta “bomba ácida” y su control sobre enzimas manejadoras de lípidos, el estudio señala las terapias centradas en los lisosomas como una vía prometedora para frenar o revertir la enfermedad del hígado graso.
Cita: Xu, R., Yang, F., Zhang, Z. et al. ATP6V1B2 alleviates hepatic steatosis by promoting lysosomal acidification in hepatocytes. Cell Death Discov. 12, 170 (2026). https://doi.org/10.1038/s41420-026-03052-8
Palabras clave: enfermedad del hígado graso, lisosomas, autofagia, metabolismo de lípidos, inflamación hepática